
【题目】三氟化氮(NF3)常用于微电子工业,可用以下反应制备:4NH3+3F2=NF3+3NH4F,下列说法中,正确的是( )
A.NF3的电子式为![]()
B.NH4F分子中仅含离子键
C.在制备NF3的反应中,NH3表现出还原性
D.在制备NF3的反应方程式中,各物质均为共价化合物
 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源: 题型:
【题目】根据所学知识,回答下列问题:
(1)“元时,南安有黄长者,为宅煮糖,宅垣忽坏,去土而糖白,后人遂效之。”泥土能将红糖变白糖,其表现的性质是__________。
(2)用鸡蛋壳膜和蒸馏水可除去淀粉胶体中的食盐,其原理是______________。
(3)欲使![]() 全部转化为
全部转化为![]() ,则需要氧化剂
,则需要氧化剂![]() (还原产物为
(还原产物为![]() )至少_______
)至少_______![]() 。
。
(4)下列变化为化学变化的是_________(填字母)。
A.![]() 的潮解 B.铁的生锈 C.新制氯水久置后颜色变浅
的潮解 B.铁的生锈 C.新制氯水久置后颜色变浅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子反应方程式正确的是
A. 实验室用固体氯化铵和熟石灰共热制取NH3:2NH4++Ca(OH)2![]() 2NH3↑+ Ca2++2H2O
2NH3↑+ Ca2++2H2O
B. 铜与浓硝酸反应: 3Cu + 8H+ + 2NO3-=3Cu2+ + 2NO↑ + 4H2O
C. 氨水与FeCl3溶液反应:3OH-+ Fe3+ =Fe(OH)3↓
D. Na2O2投入水中:2Na2O2+2H2O = 4Na++4OH-+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式的书写及评价均合理的是( )
选项 | 离子方程式 | 评价 |
A | 将2 mol Cl2通入到含1 mol FeI2的溶液中:2Fe2++2I-+2Cl2=2Fe3++4Cl-+I2 | 正确; Cl2过量,Fe2+、I-均被氧化 |
B | Mg(HCO3)2溶液与足量的NaOH溶液反应:Mg2++2HCO | 正确;Mg(OH)2比MgCO3更难溶 |
C | 过量SO2通入到NaClO溶液中:SO2+H2O+ClO-=HClO+HSO | 正确;H2SO3的酸性强于HClO |
D | 将Na2O2固体溶于水:2Na2O2+2H2O=4Na++4OH-+O2↑ | 正确; Na2O2是碱性氧化物 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】决定物质性质的重要因素是物质结构。请回答下列问题:
(1)元素K的焰色反应呈紫红色,其中紫色对应的辐射波长为_______nm(填标号)。
A.404.4 B.553.5 C.589.2 D.670.8 E.766.5
(2)基态K原子中,核外电子占据最高能层的符号是________,占据该能层电子的电子云轮廓图形状为________________。
(3)已知元素M是组成物质Ca5(PO4)3F的一种元素。元素M的气态原子逐个失去第1个至第5个电子所需能量(即电离能,用符号I1至I5表示)如表所示:
I1 | I2 | I3 | I4 | I5 | |
电离能(kJ/mol) | 589.8 | 1145.4 | 4912.4 | 6491 | 8153 |
元素M化合态常见化合价是________价,其基态原子电子排布式为____________
(4)PO43-的中心原子的杂化方式为__________,键角为_______________
(5)Ca3(PO4)3F中非金属元素电负性由大到小的顺序为________________
(6)下列元素或化合物的性质变化顺序正确的是__________________
A.第一电离能:Cl>S>P>Si B.共价键的极性:HF>HCI>HBr>HI
C.晶格能:NaF>NaCl>NaBr>NaI D.热稳定性:MgCO3>CaCO3>SrCO3>BaCO3
(7)CaF2晶胞结构如图所示,则CaF2晶体中与Ca2+最近且等距离的Ca2+数目为_____________;已知Ca2+和F-半径分别为a cm、b cm,阿伏加德罗常数为NA,M为摩尔质量,则晶体密度为___________________g·cm-3(不必化简)。
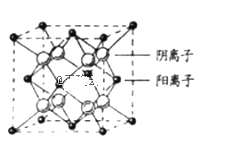
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种易溶于水的化合物只由表中的八种离子组成,且四种化合物中阴、阳离子各不相同。
阴离子 | Cl-、SiO32-、OH-、NO3- |
阳离子 | H+、Ag+、Na+、K+ |
已知:A溶液呈强酸性,且A溶液与B、C溶液混合均产生白色沉淀,B的焰色反应呈黄色。
回答下列问题:
(1)写出A、B、C、D的化学式:A______,B_____,C____,D____。
(2)写出A溶液与B溶液反应的离子方程式: __________。
(3)请选出适合存放A、C、D溶液的试剂瓶的序号:

溶液 | A | C | D |
试剂瓶序号 | ___ | ___ | ___ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国首架国产大飞机C919采用的先进材料主要有第三代铝锂合金、碳纤维复合材料及钛合金等。回答下列问题:
![]() 基态原子核外电子排布式为______,其核外电子占据最高能层的符号是______。
基态原子核外电子排布式为______,其核外电子占据最高能层的符号是______。
![]() 电子结合能是指在中性原子中当其他电子均处在可能的最低能态时,某电子从指定的轨道上电离时所需能量的负值。Li的2s轨道电子结合能比1s轨道的______
电子结合能是指在中性原子中当其他电子均处在可能的最低能态时,某电子从指定的轨道上电离时所需能量的负值。Li的2s轨道电子结合能比1s轨道的______![]() 填“大”或“小”
填“大”或“小”![]() ,原因是______。
,原因是______。
![]() 基碳纤维是以聚丙烯腈纤维为原料的碳纤维。丙烯腈
基碳纤维是以聚丙烯腈纤维为原料的碳纤维。丙烯腈![]() 分子中
分子中![]() 键和
键和![]() 键的个数比为______,碳原子间共价键的键角约为______。
键的个数比为______,碳原子间共价键的键角约为______。
![]() 工业上用镁还原
工业上用镁还原![]() 的方法制备金属钛,元素Mg、Ti、Cl的电负性分别为
的方法制备金属钛,元素Mg、Ti、Cl的电负性分别为![]() 、
、![]() 、
、![]() ,
,![]() 的熔点______
的熔点______![]() 的熔点
的熔点![]() 填“高于”或“低于”
填“高于”或“低于”![]() 。
。
![]() 钛存在两种同素异构体,
钛存在两种同素异构体,![]() 采纳六方最密堆积,
采纳六方最密堆积,![]() 采纳体心立方堆积,鉴别两种钛晶体可以用______法,由
采纳体心立方堆积,鉴别两种钛晶体可以用______法,由![]() 转变为
转变为![]() 晶体体积______
晶体体积______![]() 填“膨胀”或“收缩”
填“膨胀”或“收缩”![]() 。
。
![]() 由Ba、Ti和O组成的三元离子晶体中,晶胞的顶点被
由Ba、Ti和O组成的三元离子晶体中,晶胞的顶点被![]() 占据,体心被
占据,体心被![]() 占据,面心被
占据,面心被![]() 占据,晶胞参数
占据,晶胞参数![]() ,该晶体的化学式为______。
,该晶体的化学式为______。![]() 为140pm,则
为140pm,则![]() 为______
为______![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(Ga)与铝同主族,曾被称为“类铝”,其氧化物、氢氧化物均为两性化合物。工业制备镓的流程如图所示。下列判断不合理的是( )
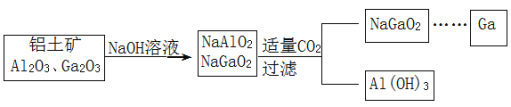
A.Al、Ga均处于ⅢA族
B.Ga(OH)3可与NaOH反应生成 NaGaO2
C.酸性:Al(OH)3>Ga(OH)3
D.Ga2O3可与盐酸反应生成GaCl3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com