
【题目】根据所学知识,回答下列问题:
(1)“元时,南安有黄长者,为宅煮糖,宅垣忽坏,去土而糖白,后人遂效之。”泥土能将红糖变白糖,其表现的性质是__________。
(2)用鸡蛋壳膜和蒸馏水可除去淀粉胶体中的食盐,其原理是______________。
(3)欲使![]() 全部转化为
全部转化为![]() ,则需要氧化剂
,则需要氧化剂![]() (还原产物为
(还原产物为![]() )至少_______
)至少_______![]() 。
。
(4)下列变化为化学变化的是_________(填字母)。
A.![]() 的潮解 B.铁的生锈 C.新制氯水久置后颜色变浅
的潮解 B.铁的生锈 C.新制氯水久置后颜色变浅
【答案】吸附性脱色 淀粉胶体不能通过半透膜(鸡蛋壳膜),而食盐溶液可以 0.5 BC
【解析】
(1)红糖变白糖的原因是利用黄泥的吸附作用,故答案为:吸附性脱色;
(2)胶体不能通过半透膜(鸡蛋壳膜),而溶液能通过半透膜(鸡蛋壳膜),所以用鸡蛋壳膜和蒸馏水可以除去淀粉胶体中的食盐,故答案为:淀粉胶体不能通过半透膜(鸡蛋壳膜),而食盐溶液可以;
(3)![]() 中钒元素为+4价,
中钒元素为+4价,![]() 中钒元素为+5价,
中钒元素为+5价,![]() 变为
变为![]() ,失去
,失去![]() ,
,![]() 中氯元素化合价为+5价,
中氯元素化合价为+5价,![]() 作氧化剂,还原产物为
作氧化剂,还原产物为![]() ,
,![]()
![]() 得到
得到![]() ,所以将
,所以将![]() 全部转化为
全部转化为![]() ,消耗
,消耗![]()
![]() ;故答案为:0.5;
;故答案为:0.5;
(4)A.![]() 的潮解,没生成新物质,不是化学变化,不选A;
的潮解,没生成新物质,不是化学变化,不选A;
B. 铁的生锈,生成氧化铁,生成了新物质,是化学变化,选B;
C. 新制的氯水呈浅黄绿色,久置的氯水,由于次氯酸分解,促进氯气和水的反应,不断消耗氯气,颜色变浅,有新物质生成,属于化学变化,选C;故答案为:BC。


 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:高中化学 来源: 题型:
【题目】在一定条件下,将![]() 体积NO和
体积NO和![]() 体积O2同时通入倒立于水中且盛满水的容器中,充分反应后,容器内残留
体积O2同时通入倒立于水中且盛满水的容器中,充分反应后,容器内残留![]() 体积的气体,该气体与空气接触变为红棕色,则
体积的气体,该气体与空气接触变为红棕色,则![]() 为( )
为( )
A. 3:2 B. 2:3 C. 8:3 D. 3:8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将足量稀盐酸加到下列固体混合物中,只能发生一种反应的是( )
A.NaOH、NaCl、NaAlO2B.KNO3、NaCl、CH3COONa
C.Na2S、(NH4)2SO3、AgNO3D.KNO3、Na2SO3、NH4HCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在体积为3L的密闭容器中化学反应CO(g)+2H2(g)![]() CH3OH(g)达到平衡状态。
CH3OH(g)达到平衡状态。
(1)该反应的平衡常数表达式K=__;根据图,升高温度,K值将__(填“增大”、“减小”或“不变”)。
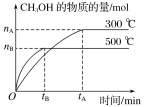
(2)500℃时,从反应开始到化学平衡状态,以H2的浓度变化表示的化学反应速率是__(用nB、tB表示)。
(3)判断该可逆反应达到化学平衡状态的标志是__(填字母,下同)。
a.υ生成(CH3OH)=υ消耗(CO) b.混合气体的密度不再改变
c.混合气体的平均相对分子质量不再改变 d.CO、H2、CH3OH的浓度均不再变化
(4)300℃时,将容器的容积压缩到原来的![]() ,在其他条件不变的情况下,对平衡体系产生的影响是____。
,在其他条件不变的情况下,对平衡体系产生的影响是____。
a.c(H2)减小 b.正反应速率加快,逆反应速率减慢
c.CH3OH的物质的量增加 d.重新平衡时![]() 减小
减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温条件下将一定量X和Y的混合气体通入一容积为2L的密闭容器中,X和Y两物质的浓度随时间变化情况如图。

(1)该反应的化学方程式为(反应物或生成物用符号X、Y表示):_________________________。
(2)a、b、c、d四个点中,表示化学反应处于平衡状态的点是________________。
素材1:某温度和压强下,2L容器中,发生反应2SO2+O2![]() 2SO3,不同时间点测得密闭体系中三种物质的物质的量如下:
2SO3,不同时间点测得密闭体系中三种物质的物质的量如下:

素材2:反应在不同条件下进行时SO2的转化率:(SO2的转化率是反应的SO2占起始SO2的百分数,SO2的转化率越大,化学反应的限度越大)

根据以上的两个素材回答问题:
(3)根据素材1中计算20~30s期间,用二氧化硫表示的化学反应平均速率为________。
(4)根据素材2中分析得到,提高该化学反应限度的途径有_______________。
(5)根据素材1、素材2中分析得到,要实现素材1中SO2的转化率需控制的反应具体条件是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.实验室欲用质量分数为36.5%的浓盐酸(密度为![]() )来配制
)来配制![]() 稀盐酸。请回答下列问题:
稀盐酸。请回答下列问题:
(1)需要用到的仪器除量筒烧杯外,还需用到的仪器有_________。
(2)在上述仪器选定的情况下,需要量取浓盐酸________![]() 。
。
(3)对于容量瓶来说除洗净外还必须进行的一项操作是_____________。
(4)配制溶液过程中,下列操作对溶液中溶质的物质的量浓度有何影响?(在横线上填“偏高”“偏低”或“无影响”)
①烧杯和玻璃棒洗净后没有烘干即进行实验:________________。
②溶解液转移后没有用蒸馏水洗涤烧杯2~3次:________________。
③定容时,俯视刻度线:__________________。
Ⅱ.取出配制好的盐酸![]() 与足量的锌粒反应。试计算:
与足量的锌粒反应。试计算:
(5)产生的氢气在标准状况下的体积为_________![]() 。
。
(6)转移的电子的物质的量为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年,一些药物引起的不良反应引起了人们的关注。因此在开发新药时如何减少毒副作用是一个很重要的课题。在下列结构简式中,Ⅰ是扑热息痛,Ⅱ是阿司匹林,它们都是临床应用广泛的解热镇痛药,但Ⅰ易导致肾脏中毒,Ⅱ对胃黏膜有刺激性,多用会引起胃溃疡。Ⅲ是扑炎痛,它是根据药物合成中“拼合原理”的方法,设计并合成出的解热镇痛药。这三种物质的结构简式如下:

试回答:
(1)为什么阿司匹林会有上述的毒副作用?___________
(2)合成扑炎痛的反应属于有机化学中的哪一类反应?_________
(3)扑炎痛本身并无解热镇痛的功效,但口服进入人体内后会产生上述药理作用,且毒副作用没有Ⅰ和Ⅱ那么明显,试加以解_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氟化氮(NF3)常用于微电子工业,可用以下反应制备:4NH3+3F2=NF3+3NH4F,下列说法中,正确的是( )
A.NF3的电子式为![]()
B.NH4F分子中仅含离子键
C.在制备NF3的反应中,NH3表现出还原性
D.在制备NF3的反应方程式中,各物质均为共价化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com