
【题目】七铝十二钙 (12CaO·7Al2O3)是一种新型的超导材料和发光材料,它是用一定量的CaCO3溶解于酸性AlCl3溶液,再用氨水沉淀,然后煅烧沉淀制备。工业上制备七铝十二钙的流程如下图: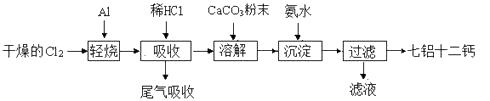
(1)轻烧后产生的AlCl3蒸气易凝华,为防止堵塞导气管可采取的措施为。
(2)吸收时用稀盐酸溶解的原因是。
(3)AlCl3溶液溶解CaCO3时,要控制碳酸钙和AlCl3的量,要求n(CaCO3)∶n(AlCl3)> 12∶14,其原因是。但若加入CaCO3过多,会产生的后果是。
(4)沉淀、过滤后的滤液主要成分是。
(5)以工业碳酸钙(含有少量Al2O3、Fe3O4杂质)生产二水合氯化钙(CaCl2·2H2O)的方法为:将工业碳酸钙溶于盐酸,加入双氧水, , 冰水洗涤,干燥,得到CaCl2·2H2O(实验中需用到的试剂和仪器有:盐酸,双氧水,氢氧化钙,冰水,pH计)。
已知:几种离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol/L计算):
开始沉淀的pH | 完全沉淀的pH | |
Fe3+ | 1.1 | 3.2 |
Al3+ | 3.5 | 4.7 |
【答案】
(1)加热导管、加粗导管
(2)抑制铝离子水解
(3)氢氧化钙微溶于水,造成损失;产生氢氧化铝沉淀
(4)NH4Cl(少量 CaCl2)
(5)加入氢氧化钙,搅拌,用pH计调节溶液的pH为4.7,过滤,向滤液中加盐酸酸化,蒸发浓缩,冷却结晶,过滤
【解析】解: (1) AlCl3易凝华,为了防止AlCl3蒸气凝华堵塞导气管,轻烧后的气体用水处理前导气管要保温或加粗处理;(2)AlCl3易水解,为抑制铝离子水解,用吸收时用盐酸吸收,(3)七铝十二钙(12CaO·7Al2O3)中钙、铝元素的物质的量比12:14,氢氧化钙微溶于水,造成损失,所以AlCl3溶液溶解CaCO3时要求n(CaCO3):n(AlCl3)>12:14。若碳酸钙加入过多,会导致铝离子水解生成氢氧化铝沉淀;(4)根据元素守恒用氨水沉淀、过滤后的滤液主要成分是NH4Cl; (5)将工业碳酸钙溶于盐酸,加入双氧水,把Fe2+氧化为Fe3+ , 加入氢氧化钙,搅拌,用pH计调节溶液的pH为4.7,过滤,向滤液中加盐酸酸化,蒸发浓缩,冷却结晶,过滤,冰水洗涤,干燥得到CaCl2·2H2O。


科目:高中化学 来源: 题型:
【题目】已知常温下氯酸钾与浓盐酸反应放出氯气,现按下图进行卤素的性质实验。玻璃管内装有分别滴有不同溶液的白色棉花球,反应一段时间后,对下图中指定部位颜色描述正确的是( ) 
① | ② | ③ | ④ | |
A | 黄绿色 | 棕黄色 | 蓝色 | 白色 |
B | 无色 | 棕黄色 | 紫色 | 白色 |
C | 黄绿色 | 棕黄色 | 蓝色 | 无色 |
D | 黄绿色 | 无色 | 紫色 | 白色 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
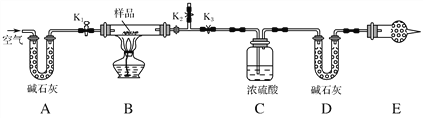
【题目】有一含NaCl、Na2CO3·10H2O和NaHCO3的混合物,某同学设计如图所示的实验装置,通过测量反应产生的CO2和H2O的质量,来确定该混合物中各组分的质量分数。
(1)实验步骤:
①按图(夹持仪器未画出)组装好实验装置后,首先进行的操作是_________。
②称取样品,并将其放入硬质玻璃管中;称量装浓硫酸的洗气瓶C的质量和装碱石灰的U形管D的质量。
③打开活塞K1、K2,关闭K3,缓缓鼓入空气数分钟,其目的是________________。
④关闭活塞K1、K2,打开K3,点燃酒精灯加热至不再产生气体。装置B中发生反应的化学方程式为_________________________________________。
⑤打开活塞K1,缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C的质量和U形管D的质量。
(2)关于该实验方案,请回答下列问题。
①若加热反应后不鼓入空气,对测定结果的影响是___________________。
②E处干燥管中盛放的药品是________,其作用是__________________ ________________,如果实验中没有该装置,则会导致测量结果NaHCO3的质量________(填“偏大”、“偏小”或“无影响”)。
③若样品质量为w g,反应后C、D装置增加的质量分别为m1 g、m2 g,则混合物中Na2CO3·10H2O的质量分数为________(用含w、m1、m2的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关,下列生活中的常见物质按酸碱性的一定顺序依次排列正确的是( )
A.厕所清洁剂、醋、肥皂、厨房清洁剂
B.厕所清洁剂、厨房清洁剂、醋、肥皂
C.醋、厕所清洁剂、肥皂、厨房清洁剂
D.厨房清洁剂、醋、肥皂、厕所清洁剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学实验兴趣小组为了验证在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明Cl2的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略)。

请按要求回答下列问题:
(1)写出烧瓶中发生反应的离子方程式_______________________________。
(2)①装置B中盛放的试剂名称是____________,作用是___________,现象是______________;
②装置D和E出现的不同现象说明的问题是__________________________________;
③写出G中发生反应的离子方程式____________________________。
(3)乙同学认为甲同学的实验有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液中的气体只有一种,乙同学提出应该在装置
___________之间(填装置字母序号)增加一个装置,所增加装置里面的试剂可以为_______(填字母序号)
a. 湿润的碘化钾淀粉试纸 b. 浓硫酸
c. 湿润的红色布条 d. 饱和食盐水
(4)A装置中分液漏斗内所用溶液浓度为12 mol/L,现欲用其配制100 mL 2 mol/L的稀溶液。则需量取________ mL浓溶液,量取所用量筒的规格是________(选填“10mL”、“25mL”或“50mL”)。若所配制的稀溶液浓度偏大,则下列可能的原因分析中正确的是__________
a. 配制前,容量瓶中有少量蒸馏水 b. 量取浓溶液时,仰视液面
c. 未经冷却,立即转移至容量瓶定容 d. 定容时,仰视液面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生想制作一种家用环保型消毒液发生器,用石墨作电极电解饱和氯化钠溶液,通电时,为使Cl2被完全吸收,制得有较强杀菌能力的消毒液,设计了如右图的装置,对此,下列有关电源电极名称和消毒液的主要成分的判断正确的是()。 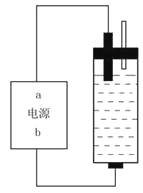
A.a为正极,b为负极;NaClO和NaCl
B.a为负极,b为正极;NaClO和NaCl
C.a为阳极,b为阴极;HClO和NaCl
D.a为阴极,b为阳极;HClO和NaCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FeCl3、CuCl2的混合溶液中加入铁粉,充分反应后仍有固体存在,则下列判断不正确的是
A. 加入KSCN溶液一定不变红色 B. 溶液中一定含Fe2+
C. 溶液中一定不含Cu2+ D. 剩余固体中一定含Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数,下列说法正确的是( )
A.标准状况下,11.2L的戊烷所含的分子数为0.5NA
B.28g乙烯所含共用电子对数目为4NA
C.现有乙烯、丙烯、丁烯的混合气体共14g,其原子数为3NA
D.标准状况下,11.2 L二氯甲烷所含分子数为0.5 NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com