
【题目】分别燃烧等物质的量的下列各组物质,其中消耗氧气的量相等的是( )
①C2H2与C2H4O ②C4H8与C6H12O6 ③C7H8与C6H12 ④HCOOCH3与CH3COOH.
A.①③④
B.①②③④
C.①④
D.①②④
【答案】B
【解析】解:①1molC2H2 完全燃烧消耗氧气的物质的量为2+ ![]() =2.5;1molC2H4O完全燃烧消耗氧气的物质的量为2+
=2.5;1molC2H4O完全燃烧消耗氧气的物质的量为2+ ![]() ﹣
﹣ ![]() =2.5,二者相等,故选;
=2.5,二者相等,故选;
②1moC4H8完全燃烧消耗氧气的物质的量为4+ ![]() =6;与C6H12O6完全燃烧消耗氧气的物质的量为6+
=6;与C6H12O6完全燃烧消耗氧气的物质的量为6+ ![]() ﹣
﹣ ![]() =6,二者相等,故选;
=6,二者相等,故选;
③1moC7H8完全燃烧消耗氧气的物质的量为7+ ![]() =9;与1molC6H12 完全燃烧消耗氧气的物质的量为6+
=9;与1molC6H12 完全燃烧消耗氧气的物质的量为6+ ![]() =9,二者相等,故选;
=9,二者相等,故选;
④HCOOCH3与CH3COOH互为同分异构体,1mol完全燃烧耗氧量相等,故选;
故选:B.
设所给物质的通式为CxHyOz,则其燃烧方程式为:CxHyOz+(x+ ![]() ﹣
﹣ ![]() )O2
)O2 ![]() xCO2+
xCO2+ ![]() H2O,所以1mol物质消耗氧气的量多少取决于(x+
H2O,所以1mol物质消耗氧气的量多少取决于(x+ ![]() ﹣
﹣ ![]() ),据此解答.
),据此解答.


 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列叙述中不正确的是( )
①12.4g白磷晶体中含有的P﹣P键数约是0.6NA;
②电解精炼铜时转移了NA个电子,阳极溶解32g铜;
③7.8g Na2S和Na2O2的混合物中含有的阴离子数大于0.1NA;
④2mol SO2和1mol O2混合在V2O5存在的条件下于密闭容器中加热反应后,容器内物质分子数大于2NA;
⑤2.9g 2CaSO4H2O含有的结晶水分子数为0.02NA(2CaSO4H2O式量为290);
⑥含0.2mol H2SO4的浓硫酸与足量铜反应,生成SO2的分子数为0.1NA;
⑦含0.1mol溶质Na2CO3的溶液中,所含阴离子总数大于0.1NA .
A.①②③④⑤⑦
B.②③⑤⑥
C.①③④⑤⑥
D.③④⑤⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.1L水中溶解了58.5g NaCl,该溶液的物质的量浓度为1mol/L
B.V L Fe2(SO4)3溶液中含a g SO42﹣ , 取此溶液 ![]() ?L用水稀释成2V L,则稀释后溶液的c(Fe3+)为
?L用水稀释成2V L,则稀释后溶液的c(Fe3+)为 ![]() ?mol/L
?mol/L
C.已知某NaCl溶液的密度是1.17 g/cm3 , 可求出此溶液的物质的量浓度
D.把100mL20%的NaOH溶液跟100mL10%的NaOH 混合后,可判断NaOH混合溶液的质量分数等于15%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4mol A气体和2mol B气体在2L的密闭容器内混合,并在一定条件下发生如下反应:2A(g)+B(g)2C(g),若经2s后测得C的浓度为0.6molL﹣1 , 现有下列几种说法: ①用物质A表示的反应的平均速率为0.3molL﹣1s﹣1
②用物质B表示的反应的平均速率为0.6molL﹣1s﹣1
③2s时物质A的转化率为70%
④2s时物质B的浓度为0.7molL﹣1
其中正确的是( )
A.①③
B.①④
C.②③
D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】600℃时,在一密闭容器中,将二氧化硫和氧气混合发生反应:2SO2(g)+O2(g)2SO3(g);△H>0.反应过程中SO2、O2、SO3物质的量的变化如图所示,下列说法中不正确的是( ) 
A.反应从0min开始,到第一次平衡时,二氧化硫的转化率为40%
B.反应进行到10min至15min时,曲线发生变化可能是因为升高了温度
C.反应进行至20min时,曲线发生变化是因为通入了氧气
D.在15min~20min、25min~30min内时反应处于平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了测定含有H2C2O42H2O、KHC2O4和K2SO4的试样中各物质的质量分数,进行如下实验:
①称取6.0g试样,加水溶解,配成250mL试样溶液.
②用酸式滴定管量取25.00mL试样溶液放入锥形瓶中,并加入2~3滴酚酞试液,用0.2500mol/L NaOH溶液滴定,消耗NaOH溶液20.00mL.
③再取25.00mL试样溶液放入另一锥形瓶中,用0.1000mol/L的酸性高锰酸钾溶液滴定,消耗高锰酸钾溶液16.00mL.
回答下列问题:
(1)已知:0.10mol/L KHC2O4溶液pH约为3,其中含碳元素的粒子浓度由大到小的顺为 .
(2)步骤①所需要的玻璃仪器有烧杯、玻璃棒、 .
(3)完成并配平下列离子方程式:C2O42﹣+MnO4﹣+H+=CO2↑+Mn2++
(4)步骤③中判断滴定终点的方法是 .
(5)步骤②中量取试样溶液时,酸式滴定管用蒸馏水洗过后没有润洗,则测得的H2C2O42H2O的质量分数 . (填“偏大”、“偏小”或“无影响”)
(6)试样中H2C2O42H2O的质量分数为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以铁为阳极、铜为阴极,对足量的NaOH溶液进行电解,一段时间后得到2molFe(OH)3沉淀,此时消耗水的物质的量共为( )
A.2mol
B.3mol
C.4mol
D.5mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】决定物质性质的重要因素是物质结构.请回答下列问题. 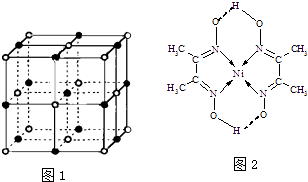
(1)已知A和B为第三周期元素,其原子的第一至第四电离能如表所示:
电离能/kJmol﹣1 | I1 | I2 | I3 | I4 |
A | 578 | 1817 | 2745 | 11578 |
B | 738 | 1451 | 7733 | 10540 |
A通常显价,B元素的核外电子排布式为 .
(2)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(如图1所示),已知3种离子晶体的晶格能数据如表:
离子晶体 | NaCl | KCl | CaO |
晶格能/kJmol﹣1 | 786 | 715 | 3401 |
则该4种离子晶体(不包括NaCl)熔点从高到低的顺序是 . 其中MgO晶体中一个Mg2+周围和它最邻近且等距离的Mg2+有个.
(3)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好.离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是 .
(4)某配合物的分子结构如图2所示,其分子内不含有(填序号).
A.离子键
B.极性键
C.金属键
D.配位键
E.氢键
F.非极性键.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com