
【题目】用括号中注明的方法分离下列各组混合物,其中不正确的是( )
A.氮气和氧气(液化蒸馏)
B.食盐中的沙砾(溶解过滤,蒸发结晶)
C.氢氧化铁胶体中的少量食盐(渗析)
D.除去乙醇中溶解的微量食盐(过滤)
科目:高中化学 来源: 题型:
【题目】目前世界上60%的镁是从海水提取的。海水提镁的主要流程如下:
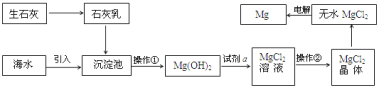
提示: ①MgCl2晶体的化学式为MgCl26H2O;
②MgO的熔点为2852℃,无水MgCl2的熔点为714℃。
(1)操作①的名称是 ________, 操作②的名称___________、冷却结晶、过滤。
(2)试剂a的名称是_____________。
(3)用氯化镁电解生产金属镁的化学方程式为:_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙三位同学分别用如下三套实验装置及化学药品(其中碱石灰为固体氢氧化钠和生石灰的混合物)制取氨气。请你回答下列问题:
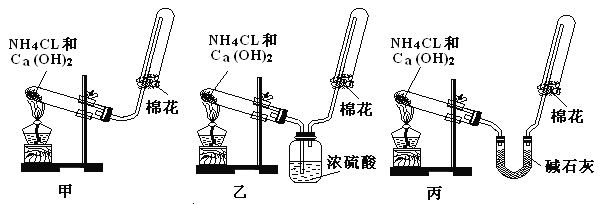
(1)三位同学制取氨气的化学方程式为:___________________。
(2)三位同学都用向下排空气法收集氨气,其原因是_____________________。
(3)三位同学用上述装置制取氨气时,其中有一位同学没有收集到氨(如果他们的实验操作都正确),你认为没有收集到氨气的同学是_______ 填(“甲”、“乙”或“丙”),收集不到氨气的主要原因是_________________(用化学方程式表示)。
(4)检验氨气是否收集满的方法是(简述操作方法、现象和结论)__________________。
(5)三位同学都认为他们的实验装置也可用于加热碳酸氢铵固体制取纯净的氨气,你判断能够达到实验目的的是_______ (填“甲”、“乙”或“丙”),该装置中的NH4HCO3固体能否用NH4Cl固体代替?_______ (填“能”或“不能”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】气体的体积主要由以下什么因素决定的:①气体分子的直径 ②气体物质的量的多少 ③气体分子间的平均距离 ④气体分子的相对分子质量( )
A.①②
B.①③
C.②③
D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素单质及其化合物有广泛用途,请根据周期表中第三周期元素相关知识回答下列问题:
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是_______。
a.单质的熔点降低
b.原子半径和简单离子半径均减小
c.元素的金属性减弱,非金属性增强
d.氧化物对应的水化物碱性减弱,酸性增强
(2)氧化性最弱的简单阳离子是_______;热稳定性:H2O____H2S(填>、<、=)。
(3)写出SiCl4的电子式:________。
(4)已知化合物M由第三周期的两种相邻元素按原子个数比1:1组成,不稳定,遇水反应生成谈黄色沉淀A和两种无色有刺意性气味气体B、C,相应物质的转化关系如图:

①已知M的摩尔质量为135g/mol,写出M的化学式_____。
②任选一种合适的氧化剂Y,写出C的浓溶液与Y反应生成D的离子反应方程式_______。
③M中的一种元素可形成化合物KXO3,可用于实验室制O2。若不加催化剂,400℃时KXO3分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1:1。写出该反应的化学方程式:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.在恒温、体积为1.0L的密闭容器中通入1.0molN2和xmolH2发生如下反应N2(g)+3H2(g)![]() 2NH3(g),20min后达到平衡,测得反应放出的热量为18.4kJ,混合气体的物质的量为1.6mol,容器内的压强变为原来的80%。请回答下列问题:
2NH3(g),20min后达到平衡,测得反应放出的热量为18.4kJ,混合气体的物质的量为1.6mol,容器内的压强变为原来的80%。请回答下列问题:
(1)20min内,V(N2)=______。
(2)该反应的热化学方程式为____________。
(3)下列叙述中能表示该反应达到平衡状态的是_______(填序号)。
①N2体积分数保持不变
②单位时间断裂03tmolH-H键,同时生成0.6molN-H键
③混合气体的密度不再改变
④2v正(H2)=3v逆(NH3)
⑤混合气体的平均摩尔质量不再改变
II.1883年,瑞典化学家阿伦尼乌斯创立了电离学说,在水溶液范围内对酸、碱作出了严密的概括。请回答下列有关水溶液的问题:
(4)①用电离方程式表示氨水溶液是碱性的原因________;
②用离子方程式表示碳酸钠溶液显碱性的原因__________。
(5)25℃时,在含HA和A-的溶液中,HA和A-两者中各自所占的物质的量分数(a)随溶液pH变化的关系如下图所示。请比较下列大小关系(填编号)
①在pH<4.76的溶液中,c(A-)____(HA);
②在pH>4.76的溶波中,c(A-)+(OH-)_____c(H+)。
A.大于 B.小于 C.等于 D.可能大于,也可能等于 E.可能小于,也可能等于

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下述实验方案能达到实验目的的是( )
编号 | A | B | C | D |
实验方案 |
|
|
|
|
实验目的 | 实验室制备乙酸乙酯 | 分离乙酸和水 | 验证溴乙烷在氢氧化钠乙醇溶液中发生消去反应产生的乙烯 | 收集乙烯并验证它与溴水发生加成反应 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作错误的是( )
A.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶支管口处
B.蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热
C.从碘水中萃取碘时,萃取剂应不溶于水,且比水更容易使碘溶解
D.分液时,分液漏斗内的下层液体从下口放出,上层液体从上口倒出
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com