
【题目】氧化还原是一类重要的反应。
(1)已知反应2I-+2Fe3+=I2+2Fe2+,反应中还原剂是_________,氧化性Fe3+______I2 (填“ < ”或“ > ”) 。
(2)在2Na2O2+2CO2=2Na2CO3+O2反应中,若转移3mol电子,则所产生的氧气在标准状况下的体积为___________L。
(3)在xR2++yH++O2═mR3++nH2O的离子方程式中,对系数m和R2+、R3+判断正确的是__。
A.m=y,R3+是还原剂 B.m=2y,R2+被氧化
C.m=2,R3+是氧化剂 D.m=4,R2+是还原剂
(4)用双线桥标出反应2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O中电子转移的方向和数目_________。
(5)氯气和石英砂、碳粉共热可发生反应:SiO2+2C+2Cl2![]() SiCl4+2CO当反应消耗6g碳时,生成还原产物_________mol。
SiCl4+2CO当反应消耗6g碳时,生成还原产物_________mol。
【答案】 I- > 33.6 D  0.25
0.25
【解析】(1)碘离子氧化为碘单质,反应中做还原剂;Fe3+价态降低,发生还原反应,做氧化剂,碘单质为氧化产物,因此氧化性:Fe3+>I2;正确答案:I- ; >。
(2)在2Na2O2+2CO2=2Na2CO3+O2反应中,转移电子的量为2mol,生成氧气1 mol;若转移3mol电子,则所产生的氧气在标准状况下的体积为1.5×22.4= 33.6 L;
(3)在xR2++yH++O2═mR3++nH2O的离子方程式中,R2+→R3+,发生氧化反应,O2→H2O,发生还原反应,因此R2+是还原剂,被氧化,根据原子守恒规律可知:x=m, y=2n, 又知n=2,所以y=4,根据电荷守恒规律可知:2m+ y=3m,m=y=4,因此m=4,R2+是还原剂正确,正确答案:D。
(4)KMnO4中Mn元素为+7价降低到MnCl2中的+2价,2molKMnO4转移电子的量为2×5=10 mol;16molHCl(浓)中有10molHCl被氧化5mol Cl2,转移电子用双线桥标出电子转移的方向和数目如下: ;正确答案:
;正确答案: 。
。
(5)该反应中碳做还原剂,被氧化,对应氧化物产物为CO;氯气做氧化剂,被还原,对应还原产物为SiCl4,根据反应关系:2C--- SiCl4可知当反应消耗6g碳时(即0.5 mol)时, 生成SiCl4的量为0.25 mol,正确答案:0.25。


科目:高中化学 来源: 题型:
【题目】已知短周期元素的四种离子A2+、B+、C3-、D-具有相同的电子层结构,则下列叙述中正确的是
A. 原子序数:D>C>B>A B. 原子半径:B>A>C>D
C. 离子半径:C3->D->A2+>B+ D. 氧化性:A2+>B+,还原性:C3-<D-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.氧化还原反应的实质是电子的转移
B.置换反应不一定是氧化还原反应
C.氧化剂发生氧化反应
D.有单质参加或者生成的反应一定属于氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合物甲中含有明矾[KAl(SO4)2·12H2O]、Al2O3和Fe2O3。在一定条件下由甲可实现下图所示的物质之间的转化:
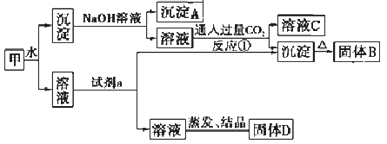
请回答下列问题:
(1)写出A、B的化学式:A________ B_________。
(2)试剂a最好选用下列试剂中的_________。
A.NaOH溶液 B.稀盐酸 C.二氧化碳 D.氨水
请写出相应的离子方程式___________。
(3)写出反应①(生成溶液C和沉淀)的离子方程式_________。
(4)固体D可以作为复合性的化学肥料,D中所含物质的化学式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各表述与示意图一致的是( ) 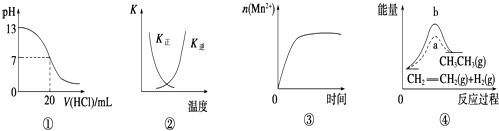
A.图①表示25℃时,用0.1 mol/L盐酸滴定20 mL 0.1 mol/L NaOH溶液,溶液的pH随加入酸体积的变化
B.图②中曲线表示反应2SO2(g)+O2(g)2SO3(g)△H<0正、逆反应的平衡常数K随温度的变化
C.图③表示10 mL 0.01 mol/L KMnO4酸性溶液与过量的0.1 mol/L H2C2O4溶液混合时,n(Mn2+)随时间的变化
D.图④中a、b曲线分别表示反应:CH2═CH2(g)+H2(g)→CH3CH3(g)△H<0使用和未使用催化剂时,反应过程中的总能量变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。据此下列说法错误的是( )
硫酸化学纯(CP)
(500mL)
品名:硫酸
化学式:H2SO4
相对分子质量:98
密度:1.84g/cm3
质量分数:98%
A. 该硫酸试剂的物质的量浓度为18.4mol·L-1
B. 该硫酸与等体积的水混合所得溶液的质量分数大于49%
C. 配制200.0mL4.6mol·L-1的稀硫酸需取该硫酸50.0mL
D. 常温下,将2.7gAl投入足量该硫酸中可得到标准状况下的氢气3.36L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】六种短周期元素a、b、c、d、e、f其原子序数与其最高正价或最低负价的关系如下图所示。

(1)上述六种元素,其中属于金属元素的有________种。
(2)元素f在周期表中的位置是____________。
(3)由a、b、c三种元素组成既含离子键又含共价键的化合物,该化合物的化学式为________,该化合物的水溶液显_________性,该化合物在水中的电离方程式为____________。
(4)b元素的气态氢化物与f元素的气态氢化物熔沸点高低顺序为_________(用氢化物的化学式表示)。
(5)a与b、c两元素分别可形成18电子的分子M和N,其中M的电子式为_______。化合物M是一种环保的液体燃料,常温下8g液态M与足量的液态N反应可放出204.5kJ的热量,则该反应的热化学反应方程式为___________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com