
【题目】已知2SO2(g)+ O2 (g)![]() 2SO3 (g);△H=﹣197kJmol﹣1。向同温、同体积的三个密闭容器中分别充入气体:(甲) 2mol SO2和1mol O2;(乙) 1mol SO2和0.5mol O2;(丙) 2mol SO3。恒温、恒容下反应达到平衡时,下列关系一定正确的是
2SO3 (g);△H=﹣197kJmol﹣1。向同温、同体积的三个密闭容器中分别充入气体:(甲) 2mol SO2和1mol O2;(乙) 1mol SO2和0.5mol O2;(丙) 2mol SO3。恒温、恒容下反应达到平衡时,下列关系一定正确的是
A.容器内压强P:P甲=P丙>2P乙
B.反应放出或吸收热量的数值Q:Q甲=Q丙>2Q乙
C.c(SO2)与c(O2)之比k:k甲=k丙>k乙
D.SO3的质量m:m甲=m丙>2m乙
【答案】D
【解析】
丙容器中2mol SO3折算成反应物为2mol SO2和1mol O2与甲容器相同,所以达到平衡时与甲为等效平衡,乙容器起始量为甲的一半,平衡时压强小于甲,由于该反应的正反应为体积减小的反应,所以乙容器中反应正向进行的程度小于甲,所以乙容器中压强大于甲容器压强的一半,SO3的质量小于甲的一半,平衡常数只受温度影响,与反应起始量无关,由于甲和丙是从相反方向到达的等效平衡,所以它们热量的数值之和应等于反应的反应热,据此答题。
丙容器中2mol SO3折算成反应物为2mol SO2和1mol O2与甲容器相同,所以达到平衡时与甲为等效平衡,乙容器起始量为甲的一半,平衡时压强小于甲,由于该反应的正反应为体积减小的反应,所以乙容器中反应正向进行的程度小于甲,所以乙容器中压强大于甲容器压强的一半,SO3的质量小于甲的一半,平衡常数只受温度影响,与反应起始量无关,由于甲和丙是从相反方向到达的等效平衡,所以它们热量的数值之和应等于反应的反应热,所以有:
A.容器内压强P:P甲=P丙<2P乙,故A错误;
B.甲与丙为等效平衡,平衡时对应各组分的物质的量相等,故Q甲+Q丙=197,甲等效为在乙的基础上增大一倍压强,平衡向正反应移动,SO2转化率增大,故Q甲>2Q乙,故B错误;
C.对于甲、乙,SO2、O2起始物质的量之比等于化学计量数之比,c(SO2)与c(O2)之比为定值2:1,丙为分解反应,丙中c(SO2)与c(O2)之比为2:1,故k甲=k丙=k乙=2,故C错误;
D.SO3的质量m:m甲=m丙>2m乙,故D正确;
故答案为D。


科目:高中化学 来源: 题型:
【题目】(1)某温度时,水的离子积为KW=1×10-13,则该温度___25℃(填“>”、“<”或“=”)。在此温度下,某溶液中由水电离出来的H+浓度为1×10-10mol/L,则该溶液的pH可能为_____。
(2)若温度为25℃时,体积为Va、pH=a的H2SO4与体积为Vb、pH=b的NaOH混合,恰好中和。已知Va>Vb,且a=0.5b,此溶液中各种离子的浓度由大到小的排列顺序是:____,a的取值范围____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】HCHO与O2在HAP表面催化氧化的历程示意图如图:(HAP仅为部分结构)
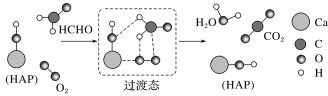
下列说法正确的是( )
A.HAP能提高HCHO的平衡转化率
B.HCHO在反应过程中有C-H键的断裂
C.产物CO2分子中的氧原子全部来自O2
D.该反应可表示为2HCHO+O2![]() CO2+2H2O
CO2+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表格中的各种情况,可以用右图的曲线表示的是 ( )
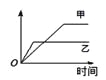
反 应 | 纵坐标 | 甲 | 乙 | |
A | 相同质量的氨,在同一容器中 | 氨气的转化率 | 500℃ | 400℃ |
B | 等质量钾、钠分别与足量水反应 | H2质量 | 钠 | 钾 |
C | 在体积可变的恒压容器中,体积比1︰3的N2、H2, | 氨气的浓度 | 活性高的催化剂 | 活性一般的催化剂 |
D | 2 molSO2和1 molO2,在相同温度下2SO2+ O2 | SO3物质的量 | 2个大气压 | 10个大气压 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有原子序数依次增大的a、b、c、d四种元素,最外层电子数分别为4、1、x、7,已知c原子的电子层数等于x,d-的电子层结构与Ar元素相同。下列说法错误的是( )
A.元素a与氢形成原子比为1:1的化合物有多种
B.元素b的单质能与水、无水乙醇反应
C.c的简单离子与d-的简单离子最外层电子数和电子层数都不相同
D.元素a与元素d可形成既含有极性共价键又含非极性共价键的化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为铝热反应的实验装置,请回答下列问题:
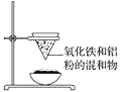
(1)该实验装置中还缺________,引发铝热反应的操作为_______。
(2)若将氧化铁换成氧化镁,该反应____(填“能”或“不能”)发生,理由是______。
(3)铝热反应的用途有哪些__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】奥司他韦是一种高效、高选择性神经氨酸酶抑制剂,是目前治疗流感的最常用药物之一,是公认的抗禽流感、甲型H1N1等病毒最有效的药物之一。其合成路线如图所示:
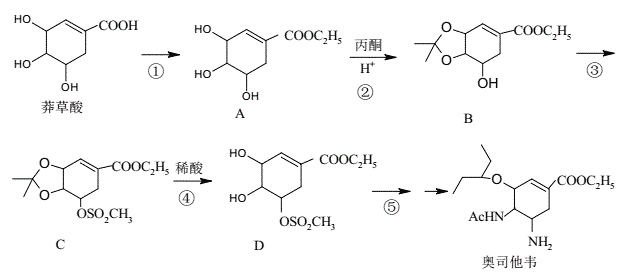
回答下列问题:
(1)莽草酸的含氧官能团名称有__;反应③的反应类型__。
(2)反应①的反应试剂和反应条件__。
(3)1molB最多可以消耗___molNaOH溶液。
(4)请写出反应②的化学方程式__。
(5)芳香化合物X是B的同分异构体,则符合官能团只含酚羟基的X有___种。
(6)设计由对甲基苯甲醛制备对醛基苯甲酸![]() 的合成路线__。
的合成路线__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】吗氯贝胺是新一代缓和的抗抑郁药物,某研究小组设计如图合成路线:
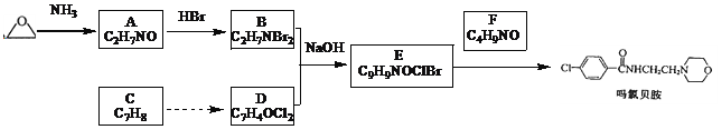
已知:①R-Br![]()
②R-COOH![]() R-COCl
R-COCl![]() R-CONHR′
R-CONHR′
③苯环上连羧基时,苯环上再取代主要生成间位取代产物。
按要求回答下列问题:
(1)化合物![]() 的结构简式________。
的结构简式________。
(2)下列有关说法正确的是________。
A.吗氯贝胺的分子式为![]()
B.在水中溶解能力![]() ,原因是
,原因是![]() 与水分子间可形成氢键
与水分子间可形成氢键
C.![]() 的反应中
的反应中![]() 的作用是反应产生氨基及中和反应产生的酸
的作用是反应产生氨基及中和反应产生的酸
D.![]() 吗氯贝胺的反应类型为取代反应
吗氯贝胺的反应类型为取代反应
(3)写出![]() 的反应方程式________。
的反应方程式________。
(4)![]() 与
与![]() 反应制备吗氯贝胺中加适量碳酸钾或过量
反应制备吗氯贝胺中加适量碳酸钾或过量![]() 均有利于提高产率,用反应方程式解释加过量
均有利于提高产率,用反应方程式解释加过量![]() 有利于提高产率的原因________。
有利于提高产率的原因________。
(5)设计![]() 的合成路线(用流程图表示,无机试剂任选)________。
的合成路线(用流程图表示,无机试剂任选)________。
(6)写出化合物![]() 同时符合下列条件的同分异构体的结构简式________。
同时符合下列条件的同分异构体的结构简式________。
①![]() 谱检测表明:分子中有3种氢原子;
谱检测表明:分子中有3种氢原子;
②![]() 谱检测表明:分子中存在
谱检测表明:分子中存在![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式中,正确的是( )
A.甲烷的燃烧热为890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3kJ·mol-1
B.500℃、30MPa下,将 0.5molN2(g)和1.5molH2(g)置于密闭容器中充分反应生成 NH3(g)放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g) △H = -38.6kJ·mol-1
2NH3(g) △H = -38.6kJ·mol-1
C.HCl 和 NaOH 反应的中和热△H=-57.3 kJ·mol-1 ,则H2SO4和Ba(OH)2反应的中和热 △H = 2×(-57.3)kJ·mol -1
D.在101kPa 时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)=2H2O(1) △H =-571.6 kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com