
����Ŀ���о�С������ͼװ����ȡCl2 �� ֤�������������к���HCl�� 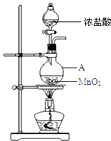
��1������A������Ϊ��A�з�Ӧ�����ӷ���ʽΪ��
��2����ͬѧ��A�в���������ͨ�������Һ��
ʵ����� | �Լ� | ���� |
a | ��ɫʯ����Һ | |
b | AgNO3��Һ | ���ְ�ɫ���� |
��ʵ��a�е�����Ϊ��
�ڲ���֤�������������к���HCl��ʵ����������ĸ��ţ���
��3����֪��HCl����ͨ�뱥��ʳ��ˮ���а�ɫ������������ͬѧ��A�в���������ͨ�뱥��ʳ��ˮ�У��а�ɫ��������������ʵ�鲻��֤�������к���HCl����ϻ�ѧ���������ԭ����
��4����֪��2S2O32��+I2�TS4O62��+2I�� �� ��ͬѧ��A�в���������ͨ������ˮ�У��õ���ҺX����������ʵ��֤�������к���HCl��
I���ⶨX���ܽ��Cl2 �� ȡ25.00mL��ҺX���������KI��Һ��Ȼ����0.04molL��1 Na2S2O3��Һ�ζ�����
��I2 �� ��ζ��յ�ʱ����Na2S2O3��ҺV mL��
�ⶨX��ClԪ����������ȡ25.00mL��ҺX��ѡ���ʵ��Ļ�ԭ�����ܽ��Cl2ȫ����ԭΪCl�� �� ����0.10molL��1 AgNO3��Һ�ζ�������Һ�е�Cl�� ��
��X�е�HClO����Ӱ��I�IJⶨ�����ԭ������
����I������ʵ�����ݿ�֤��A�в����������к���HCl�����������0.10molL��1 AgNO3��Һ�����Ӧ����mL���ú�V�Ĵ���ʽ��ʾ����
���𰸡�
��1��Բ����ƿ��MnO2+4H++2Cl�� ![]() ?Cl2��+2H2O+Mn2+
?Cl2��+2H2O+Mn2+
��2���ȱ�����ɫ��a��b
��3��Cl2+H2O?HCl+HClO��Cl2����ˮ��ʹ����Һ�е�c��Cl��������Ҳ����������
��4������1mol HClO������1mol Cl2 �� HClOҲ�������ԣ�1mol HClO��1mol Cl2���ܽ�2mol KI������I2��0.4V
���������⣺��1.������A������ΪԲ����ƿ����Һ©���е�Ũ�����Բ����ƿ�еĶ������̷�����Ӧ�����������Ȼ��̡���ˮ�����ӷ���ʽΪ��MnO2+4H++2Cl�� ![]() Cl2��+2H2O+Mn2+ �� ���Դ��ǣ�Բ����ƿ�� MnO2+4H++2Cl��
Cl2��+2H2O+Mn2+ �� ���Դ��ǣ�Բ����ƿ�� MnO2+4H++2Cl�� ![]() Cl2��+2H2O+Mn2+��
Cl2��+2H2O+Mn2+��
��2.����������ˮ��Ӧ��������ʹ����ᣬ���������������ӣ���Һ�����ԣ�������ɫ��ʯ���Լ��Ժ�ɫ�����������Ư���ԣ��DZ�����Һ��ɫ����������Ϊ���ȱ�����ɫ�����Դ��ǣ��ȱ�����ɫ����������ˮ��Ӧ��������ʹ����ᣬ��������ܹ����������Ӻ������ӣ���Һ�����ԣ����������������Ӳ�����ɫ����������a��b������֤�������������к���HCl�����Դ��ǣ�ab��
��3.��������ˮ��Ӧ��������ʹ����ᣬ����ʽΪ��Cl2+H2OHCl+HClO��Cl2����ˮ��ʹ����Һ�е�c��Cl���������������Ȼ��Ƶ��ܽ⣬��Ҳ�о������������Դ��ǣ�Cl2+H2OHCl+HClO��Cl2����ˮ��ʹ����Һ�е�c��Cl��������Ҳ���������壻
��4.����Cl2+H2OHCl+HClO������1 mol HClO������1 mol Cl2 �� HClOҲ�������ԣ�1 mol HClO��1 mol Cl2���ܽ�2 mol KI������I2��
���Դ��ǣ�����1 mol HClO������1 mol Cl2 �� HClOҲ�������ԣ�1 mol HClO��1 mol Cl2���ܽ�2 mol KI������I2��
�ڸ��ݢ���и����Ĺ�ϵ��֪��
2S2O32�� | �� | 2I�� | �� | Cl2 | �� | 2Cl�� | �� | 2Ag+ |
2 | 2 | |||||||
0.04molL��1��V | 0.10molL��1��V��AgNO3�� |
��ã�V��AgNO3��=0.4Vml��
A�в��������������Ǻ���HCl��HClҲ������������Ӧ���������ĵ���������Һ�����Ӧ����0.4Vml��
���Դ��ǣ�0.4V��
�����㾫�������ڱ��⿼��������Ļ�ѧ���ʺ�������ʵ�����Ʒ�����Ҫ�˽������Ļ�ѧ���ʣ��������Ӧ�����������ɸ�̬���ǽ�����Ӧ����ˮ��Ӧ����Ӧ���뻹ԭ�����ʷ�Ӧ��ʵ�����Ʒ���MnO2+4HCl��Ũ��=MnCl2+Cl2��+2H2O���ܵó���ȷ�𰸣�


 ����ѧ����ϵ�д�
����ѧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͭ����(CuSO4��xH2O)��һ����;�㷺���Լ���ijС����̽������ͭ��������ʡ�
ʵ��I:̽������ͭ�������ԡ�
ȡ��������ͭ��Һ���Թ��У�����(NH4)2SO3��Һ����������M�����ˡ�ϴ�ӣ��õ�����M��Ϊ��̽��M����ɣ���������ʵ��:
�ٽ�һ����ͬ��M�ֳ����ݡ�
����һ�ݹ����м���ϡ���ᣬ�����д̼�����ζ������(X)����Һ�����ɫ���к�ɫ����������������ͨ��Ʒ����Һ�У�Ʒ����Һ��ɫ��
������һ�ݹ����м���Ũ�ռ���Һ�����ȣ���������(Y)����������ʹʪ��ĺ�ɫʯ����ֽ�������ش���������:
��1��Y�ĵ���ʽΪ_____________________��
��2�����ⶨM�������ӡ������Ӹ���֮��Ϊ2:1��M�Ļ�ѧʽΪ__________��
ʵ��II:̽������ͭ��������ȶ��ԡ�
ȡ��������ͭ�������ʵ�飬װ����ͼ��ʾ��

��֪����ʵ������Ϊ:A����ɫ������ɰ�ɫ��ĩ������ɺ�ɫ��ĩ��B�в�����ɫ������D����Һ��ɺ�ɫ��
��3�������Ʋ�����ͭ����ķֽ������_________________________��
��4��B��Cװ�õ�λ�ò��ܻ�����ԭ����_______________________________________��
��5��D�еķ�Ӧ���������У�д����һ����Ӧ�����ӷ���ʽ_____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��pH=1��ij��ҺX�н�����NH4+��Al3+��Ba2+��Fe2+��Fe3+��CO32����SO32����SO42����Cl����NO3���е�һ�ֻ��֣�����ˮ�ĵ��뼰���ӵ�ˮ�⣩��ȡ����Һ��������ʵ�飬ʵ�������ͼ�������й��ƶϲ���ȷ���ǣ�������
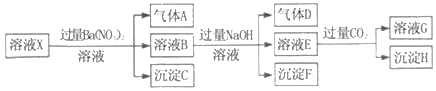
A. ��ҺX��һ������H+��Al3+��NH4+��Fe2+��SO42��
B. ������������ʵ�鲻��ȷ����ҺX���Ƿ���Fe3+��Cl��
C. ����HΪAl��OH��3��BaCO3�Ļ����
D. ����ҺXΪ100mL������������AΪ44.8mL����״��������X��c��Fe2+��=0.06molL��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������Ӽ������ۼ��ĸ��������У�˵����ȷ���ǣ� ��
A.�����ӻ������У�ֻ�������Ӽ���û�й��ۼ�
B.�Ǽ��Լ�ֻ������˫ԭ�ӵĵ��ʷ�����
C.�ڹ��ۻ���������ڣ�һ�����������Ӽ�
D.�ɲ�ͬԪ����ɵĶ�ԭ�ӷ����һ��ֻ���ڼ��Լ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ��������������������Ҫ�ɷ�ΪFe3O4��Fe2O3��FeO��SiO2��Ϊԭ���Ʊ��ߵ����ϩ������������죨Fe2O3����
��������������ͼ��![]()
�Իش��������⣺
��1�������ܡ�������Fe3O4������Ӧ�����ӷ�Ӧ����ʽΪ��
��2��ʵ����ʵ�֡�������з���������õIJ��������������������ձ��ȣ��������Ӧѡ���Լ�������Һ��pH������ĸ��ţ�
A��ϡ���� B������������Һ C�����������Һ D����ˮ
��3�����鲽����Ѿ�������ȫ���Լ�����
��4��������ķ�Ӧ�¶�һ���������35�����£���Ŀ������
��5��������з�����Ӧ�Ļ�ѧ��Ӧ����ʽΪ��
��6��������У�FeCO3�ﵽ�����ܽ�ƽ��ʱ���������²����Һ��pHΪ8.5��c��Fe2+��=1��10��6 molL��1 �� ���ж����õ�FeCO3���Ƿ���Fe��OH��2����ǡ�������ͨ������˵����������֪��Ksp[Fe��OH��2]=4.9��10��17����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��Ӧԭ����ʾ�˲�ͬ��������ˮ��Һ���в�ͬ����Ϊ���밴Ҫ��ش��������⣺����֪��H2SO3�� Ka1=1.7��10��2��Ka2=6.0��10��8 �� NH3��H2O��Kb=1.8��10��5��
��1���������ʵ�����SO2��NH3����ˮ��ַ�Ӧ��������Һ��_________�ԣ�����Һ�и�����Ũ���ɴ�С��˳��Ϊ��_____________________________________________,������Һ��c��H+���� c��OH����=___________________________����д����ʽ��

��2����NaOH��Һ���������е�SO2�������õ�Na2SO3��Һ���е�⣬��ѭ������NaOH��ͬʱ�õ�H2SO4����ԭ������ͼ��ʾ���缫����Ϊʯī����
�� ͼ��a��Ҫ���ӵ�Դ��(����������������)________����C��������������________��
��SO32���ŵ�ĵ缫��ӦʽΪ______________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�����ӷ���ʽ��д����ȷ����
A. �Ȼ��������ۣ�Fe 3+ ��Fe === 2Fe2+
B. ��������ˮ��2Na �� 2H2O === 2Na+ �� 2OH�� �� H2��
C. ϡ������̼��ƣ�CaCO3 �� 2H�� === Ca2+ �� CO2 �� �� H2O
D. ͭ��Ũ���Cu �� 4H���� 2NO3�� ![]() Cu2����2NO2�� ��2H2O
Cu2����2NO2�� ��2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ж��������йػ�ѧ����ķ�����ȷ���ǣ�������
A.�ƺ����������ں����ḻ�Ŀ���Ԫ�أ����Ƕ�������Ԫ��
B.�������պͷ��缼���Ľ�ϣ��Ƚ������Ⱦ���⣬����Ч��������������������
C.������ͨ��������Ҫ��Ӧԭ��֮һΪ��CaO+SiO2 ![]() =CaSiO3
=CaSiO3
D.��ù�������緢�ֵ���Ȼ�����أ��������������õ���ˮ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ѧ֪ʶ��ա�
��1�����������Fe��ȥ��ˮ���е������Σ�NO3�����ѳ�Ϊ�������о����ȵ�֮һ��Fe��ԭˮ����NO3���ķ�Ӧԭ����ͼ��ʾ�� 
���������������� ��
�������ĵ缫��Ӧʽ�� ��
��2���״�������Ҫ�Ļ���ԭ�ϣ��ֿ���Ϊȼ�ϣ����úϳ�������Ҫ�ɷ�ΪCO��CO2��H2���ڴ��������ºϳɼ״�����������Ҫ��Ӧ���£�
��CO��g��+2H2��g��CH3OH��g����H1
��CO2��g��+3H2��g��CH3OH��g��+H2O��g����H2
��CO2��g��+H2��g��CO��g��+H2O��g����H3
��֪��Ӧ������صĻ�ѧ���������������
��ѧ�� | H��H | C��O | C��O | H��O | C��H |
E/��KJmol��1�� | 436 | 343 | 1075 | 465 | 413 |
�ɴ˼����H1=kJmol��1 �� ��֪��H2=��58kJmol��1 �� ���H3=kJmol��1 ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com