
【题目】氨法溶浸氧化锌烟灰制取高纯锌的工艺流程如图所示。溶浸后氧化锌烟灰中锌、铜、镉、砷元素分别以![]() 、
、![]() 、
、![]() 、
、![]() 的形式存在。
的形式存在。
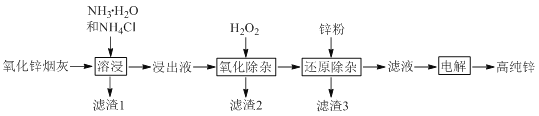
回答下列问题:
![]() 中Zn的化合价为_______,“溶浸”中ZnO发生反应的离子方程式为_______。
中Zn的化合价为_______,“溶浸”中ZnO发生反应的离子方程式为_______。
![]() 锌浸出率与温度的关系如图所示,分析
锌浸出率与温度的关系如图所示,分析![]() 时锌浸出率最高的原因为_______。
时锌浸出率最高的原因为_______。

![]() “氧化除杂”中,
“氧化除杂”中,![]() 转化为
转化为![]() 胶体吸附聚沉除去,溶液始终接近中性。该反应的离子方程式为_______。
胶体吸附聚沉除去,溶液始终接近中性。该反应的离子方程式为_______。
![]() “滤渣3”的主要成分为_______。
“滤渣3”的主要成分为_______。
![]() “电解”时
“电解”时![]() 在阴极放电的电极反应式为______。阳极区放出一种无色无味的气体,将其通入滴有KSCN的
在阴极放电的电极反应式为______。阳极区放出一种无色无味的气体,将其通入滴有KSCN的![]() 溶液中,无明显现象,该气体是_______
溶液中,无明显现象,该气体是_______![]() 写化学式
写化学式![]() 。电解后的电解液经补充_______
。电解后的电解液经补充_______![]() 写一种物质的化学式
写一种物质的化学式![]() 后可返回“溶浸”工序继续使用。
后可返回“溶浸”工序继续使用。
【答案】![]()
![]() 低于
低于![]() 时,浸出反应速率随温度的升高而增大;超过
时,浸出反应速率随温度的升高而增大;超过![]() 时,氨气逸出导致浸出反应速率下降
时,氨气逸出导致浸出反应速率下降 ![]() 胶体
胶体![]()
![]() 、Cd
、Cd ![]() 或
或![]()
![]()
![]() 或
或![]()
【解析】
由流程可知, 氧化锌烟灰加入氨水、氯化铵进行溶浸,溶浸后氧化锌烟灰中锌、铜、
、镉、砷元素分别以以![]() 、
、![]() 、
、![]() 、
、![]() 的形式存在,加入过氧化氢,
的形式存在,加入过氧化氢,![]() 转化为As2O5,胶体吸附聚沉除去,过滤后加入锌粉还原,可除去Cu、Cd等,滤液主要含有Zn(NH3)42+, 电解可生成高纯度锌,以此解答该题。
转化为As2O5,胶体吸附聚沉除去,过滤后加入锌粉还原,可除去Cu、Cd等,滤液主要含有Zn(NH3)42+, 电解可生成高纯度锌,以此解答该题。
![]() 中Zn的化合价为
中Zn的化合价为![]() ;依据流程图可知,“溶浸”中ZnO发生反应的离子方程式为:
;依据流程图可知,“溶浸”中ZnO发生反应的离子方程式为:![]() ;
;
故答案为:![]() ;
;![]() ;
;
![]() 锌浸出率与温度的关系如图所示,分析
锌浸出率与温度的关系如图所示,分析![]() 时锌浸出率最高的原因为:低于
时锌浸出率最高的原因为:低于![]() 时,浸出反应速率随温度的升高而增大;超过
时,浸出反应速率随温度的升高而增大;超过![]() 时,氨气逸出导致浸出反应速率下降;
时,氨气逸出导致浸出反应速率下降;
故答案为:低于![]() 时,浸出反应速率随温度的升高而增大;超过
时,浸出反应速率随温度的升高而增大;超过![]() 时,氨气逸出导致浸出反应速率下降;
时,氨气逸出导致浸出反应速率下降;
![]() “氧化除杂”中,
“氧化除杂”中,![]() 转化为
转化为![]() 胶体吸附聚沉除去,溶液始终接近中性。该反应的离子方程式为:
胶体吸附聚沉除去,溶液始终接近中性。该反应的离子方程式为:![]() 胶体
胶体![]() ;
;
故答案为:![]() 胶体
胶体![]() ;
;
![]() 依据流程图可知,“滤渣3”的主要成分为锌发生置换反应的产物,所以主要成分为:Cu、Cd;故答案为:Cu、Cd;
依据流程图可知,“滤渣3”的主要成分为锌发生置换反应的产物,所以主要成分为:Cu、Cd;故答案为:Cu、Cd;
![]() “电解”时
“电解”时![]() 在阴极发生还原反应,所以电极反应式为:
在阴极发生还原反应,所以电极反应式为:![]() 或
或![]() ;阳极发生氧化反应,放出一种无色无味的气体,将其通入滴有KSCN的
;阳极发生氧化反应,放出一种无色无味的气体,将其通入滴有KSCN的![]() 溶液中,无明显现象,所以该气体是
溶液中,无明显现象,所以该气体是![]() ;依据反应的总方程式可得,电解后的电解液经补充
;依据反应的总方程式可得,电解后的电解液经补充![]() 或
或![]() 后可返回“溶浸”工序继续使用。故答案为:
后可返回“溶浸”工序继续使用。故答案为:![]() 或
或![]() ;
;![]() ;
;![]() 或
或![]() 。
。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某元素构成的双原子单质分子有3种,其分子量分别为158、160、162。在天然单质中,此三种单质的物质的量之比为1︰1︰1,由此推断的以下结论中,正确的是( )
A.此元素有三种同位素
B.其中质量数为79的同位素原子占原子总数的1/2
C.其中一种同位素的质量数为80
D.此元素的单质的平均分子量为160
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一固定容积的密闭容器中,充入2 mol A和1 mol B发生如下反应:2A(g)+B(g) ![]() xC(g),达到平衡后,C的体积分数为w%;若维持容器体积和温度不变,以0.6 mol A、0.3 mol B和1.4 mol C为起始物质,达到平衡后,C的体积分数也为w%,则x的值为
xC(g),达到平衡后,C的体积分数为w%;若维持容器体积和温度不变,以0.6 mol A、0.3 mol B和1.4 mol C为起始物质,达到平衡后,C的体积分数也为w%,则x的值为
A.5 B.4 C.3 D.1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图乙是根据图甲的电解池进行电解时某个量(纵坐标x)随时间变化的函数曲线(各电解池都用石墨作电极,不考虑电解过程中溶液浓度变化对电极反应的影响),这个量x是表示( )
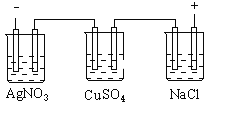
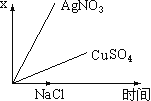
甲 乙
A. 各电池析出气体体积总数的变化B. 各电解池阳极质量的增加
C. 各电解池阴极质量的增加D. 各电极上放电的离子总数的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有五种短周期主族元素 X、 Y、 Z、 R、 Q, 它们的原子序数逐渐增大; 在周期表中的相对位置如图所示,Z是组成叶绿素的金属元素。下列说法错误的是
![]()
A.工业上都用电解法制Z、R单质
B.X和Y 的单质熔点: X<Y
C.Z、R、Y 的简单离子半径: Y>Z>R
D.Y和Q的最高价氧化物对应水化物酸性:Y>Q
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分:
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
1 | A | |||||||
2 | D | E | G | I | ||||
3 | B | C | F | H |
(1)从原子结构角度分析,D、E、G、I四种元素处于同一行,是由于它们的_______相同。E和F元素在周期表处于同一列是由于它们的______相同。
(2)E元素的最低化合价为___________,原子半径:r(E)_________ r(D)![]() ”、“
”、“![]() ”或“
”或“![]() ”
”![]() ,离子半径:r(G)_________ r(C)(填“
,离子半径:r(G)_________ r(C)(填“![]() ”、“
”、“![]() ”或“
”或“![]() ”)。
”)。
(3)在表中所列元素中最高价氧化物对应水化物中酸性最强的是________(写化学式)。
(4)科学家通过对某些元素的化合物进行研究,寻找高效农药。这些元素往往位于元素周期表的 _____________(选填序号)。
a.左下角区域 b.右上角区域 c.左上角区域 d.右下角区域
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(g)+2B(g)==C(g)的反应过程中能量变化如下图所示。下列相关说法正确的是 ( )

A. 正反应活化能大于逆反应活化能
B. 曲线b表示使用催化剂后的能量变化
C. 由图可知该反应的焓变△H=+91kJ/mol
D. 反应中将气体A换为固体反应,其他条件不变,反应放出热量大于91kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,将浓度均为0.1 mol·L-1,体积分别为Va和Vb的HA溶液与BOH溶液按不同体积比混合,保持Va+Vb=100 mL,Va、Vb与混合液pH的关系如图所示,下列说法正确的是

A. Ka(HA)=1×10-6
B. b点c(B+)=c(A-)=c(OH-)=c(H+)
C. a→c过程中水的电离程度始终增大
D. c点时,c(A-)/[c(OH-)c(HA)]随温度升高而减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】改变0.1mol·L-1二元弱酸H2A溶液的pH,溶液中H2A、HA-、A2-的物质的量分数δ(X)随pH的变化如图所示[已知δ(X)=![]() ]。下列叙述错误的是( )
]。下列叙述错误的是( )
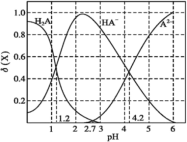
A.pH=1.2时,c(H2A)=c(HA-)
B.pH=2.7时,c(HA-)>c(H2A)=c(A2-)
C.pH=4.2时,c(HA-)=c(A2-)=c(H+)
D.lg[K2(H2A)]=-4.2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com