
| A、Fe3+、HCO3-、Cl-、Na+ |
| B、SO42-、NO3-、Ba2+、Cu2+ |
| C、MnO4-、Na+、K+、Mg2+ |
| D、Ca2+、Cl-、NO3-、Na+ |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、可用加热的方法除去混在碳酸氢钠固体中的碳酸钠固体 |
| B、除去CO中少量的O2,可将混合气体通过灼热的Cu网 |
| C、向某溶液中加入盐酸,产生使澄清石灰水变浑浊的气体,该溶液中可能含有HCO3- |
| D、向某溶液中加入盐酸酸化的BaCl2溶液有白色沉淀,该溶液中一定含有SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe2S3、I2、S |
| B、Al(OH)3、I2、S |
| C、Fe(OH)3、Al(OH)3、S |
| D、FeS、S、Al(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
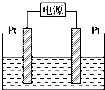 熔融盐燃料电池具有较高的发电效率,因而受到重视.某燃料电池以熔融的K2CO3(其中不含O2-和HCO)为电解质,以丁烷为燃料,以空气为氧化剂,以具有催化作用和导电性能的稀土金属材料为电极.该燃料电池负极电极反应式为:2C4H10+26CO-52e-═34CO2+10H2O.
熔融盐燃料电池具有较高的发电效率,因而受到重视.某燃料电池以熔融的K2CO3(其中不含O2-和HCO)为电解质,以丁烷为燃料,以空气为氧化剂,以具有催化作用和导电性能的稀土金属材料为电极.该燃料电池负极电极反应式为:2C4H10+26CO-52e-═34CO2+10H2O.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、A为非电解质 |
| B、A为强电解质 |
| C、A既不是电解质也不是非电解持 |
| D、A为弱电解质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com