
配制500 mL 0.0500 mol·L-1的Na2CO3溶液,不需要的仪器有
A.500 mL容量瓶 B.锥形瓶 C.烧杯 D.玻璃棒
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016届浙江省高一下学期期中考化学试卷(解析版) 题型:选择题
根据热化学方程式:S(g)+O2(g) SO2(g) △H=-QkJ·mol-1(Q>0),下列分析正确的是( )
SO2(g) △H=-QkJ·mol-1(Q>0),下列分析正确的是( )
A.1 mol S(g)与1 mol O2(g)反应生成1 mol SO2(g)放出QkJ的热量
B.1个S(g)与1个O2(g)完全反应要放出Q kJ的热量
C.S(s)+O2(g) SO2(g) △H<-Q kJ·mol-1
SO2(g) △H<-Q kJ·mol-1
D.1 mol S(g)与1 mol O2(g)的总能量比1 mol SO2(g)的总能量低QkJ
查看答案和解析>>
科目:高中化学 来源:2016届河南长葛第三实验高中高一下学期第一次考试化学试卷(解析版) 题型:选择题
下列关于元素周期表和元素周期律的说法错误的是
A.Li、Na、K元素的原子核外电子层数随着核电荷数的增加而增多
B.第二周期元素从Li到F,非金属性逐渐增强
C.因为Na比K容易失去电子,所以Na比K的还原性强
D.O与S为同主族元素,且O比S的非金属性强
查看答案和解析>>
科目:高中化学 来源:2016届江苏省淮安市协作体高一下学期期中考试化学试卷(解析版) 题型:选择题
下列反应过程中的能量变化与下图一致的是
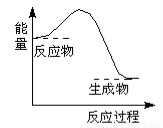
A.2Al+Fe2O3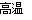 2Fe+Al2O3
2Fe+Al2O3
B.C+CO2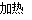 2CO
2CO
C.CaCO3 CaO+CO2↑
CaO+CO2↑
D.C+H2O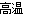 CO+H2
CO+H2
查看答案和解析>>
科目:高中化学 来源:2016届江苏省淮安市协作体高一下学期期中考试化学试卷(解析版) 题型:选择题
在下列物质中,化合物类型相同的一组是
A.NaCl HCl B.CO2 H2O
C.H2CO3 KCl D.MgCl2 SO2
查看答案和解析>>
科目:高中化学 来源:2016届江苏省沭阳县高一下学期期中调研测试化学试卷(解析版) 题型:填空题
如图所示的装置中电极a、b均为碳棒,两烧杯中所盛溶液均为500mL1.0mol/L。

(1)A为 池,(填原电池、或电解池),其中的Ag极为 极,发生 反应(填“氧化”或“还原”)。
(2)B装置中的电极b极为 极,电极反应式为 ,总反应的化学方程式为 。经过一段时间后,B装置中溶液的碱性 (填“增强”、“减弱”或“不变”)
(3)若工作一段时间后,当Zn片质量减少3.25g时,a极逸出的气体在标准状况下的体积为 L。
查看答案和解析>>
科目:高中化学 来源:2016届江苏省沭阳县高一下学期期中调研测试化学试卷(解析版) 题型:选择题
把锌片和铜片用导线相连后插入稀硫酸溶液中构成原电池。对该电池的描述合理的是①溶液中硫酸的物质的量浓度保持不变;②Cu极上有气泡产生,发生还原反应;③Cu为负极,Zn为正极;④原电池在工作时电子由负极通过溶液流向正极;⑤该装置将化学能转变为电能
A.②⑤ B.③⑤ C.①② D.④⑤
查看答案和解析>>
科目:高中化学 来源:2016届江苏省沭阳县高一下学期期中调研测试化学试卷(解析版) 题型:选择题
新能源的开发利用是人类社会可持续发展的重要课题。下列属于新能源的是
A.氢气 B.煤炭 C.天然气 D.石油
查看答案和解析>>
科目:高中化学 来源:2016届安徽师大附中高一下学期期中考查化学试卷(解析版) 题型:实验题
安徽省从2013年12月1日零时起,车用汽油升级为“国Ⅳ”标准,对二氧化硫的排放有了大大的改善。已知SO2可以用Fe( NO3)3溶液吸收, 0.1mol/L的Fe(NO3)3 溶液的pH=2。某学习小组据此展开如下相关探究:
【探究I】铜与浓硫酸的反应探究:
(l)取12.8g铜片于三颈烧瓶中,通N2一段时间后再加入20 mL 18 mol?L-1的浓硫酸,加热。装置A中有白雾(硫酸酸雾)生成,装置B中产生白色沉淀,充分反应后,烧瓶中仍有铜片剩余。
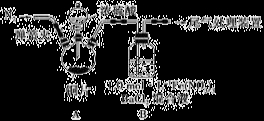
①该小组同学认为烧瓶中除有铜片剩余外还应有较多的硫酸剩余,其原因是: ___________________ 。
②该小组同学欲通过测定产生气体的量来求余酸的物质的量,设计了多种实验方案。下列方案不可行的是______ 。
A.将产生的气体缓缓通过预先称量的盛有碱石灰的干燥管,结束反应后再次称重
B.将产生的气体缓缓通入足量硫酸酸化的高锰酸钾溶液后,再加入足量的BaCl2溶液,测量所得沉淀的质量
C.用排饱和NaHSO3溶液的方法测定其产生气体的体积(折算成标准状况)
【探究II】装置B中产生沉淀的原因探究:
(2)加入浓硫酸之前先通N2一段时间,其目的是____ 。
(3)经过讨论,该小组对装置B中产生沉淀的原因,提出下列猜想(不考虑各因素的叠加):
猜想1: 装置A中的白雾进入B参与反应
猜想2:SO2被Fe3+氧化为SO42-
猜想3: 。
(4)甲同学认为只要在装置A、B间增加洗气瓶C,就可以排除装置A中白雾影响,则C中盛放的试剂是 。
(5)乙同学取出少量装置B中清液,加入几滴酸性高锰酸钾,发现紫红色褪去,据此认为猜想2成立。你是否同意其结论?并说明理由: 。
【思考与交流】
(6)实验结束后,若使烧瓶中铜片继续溶解,下列方案(必要时可加热)可行的是 。
A.打开弹簧夹,通入O2 B.由分液漏斗加入H2O2溶液
C.由分液漏斗加入NaNO3溶液 D.由分液漏斗加入Na2SO4溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com