
【题目】某化学兴趣小组设计实验,用浓硫酸与铜的反应制取SO2并进行相关实验探究,同时获得少量NaHSO3,实验装置如下图所示:
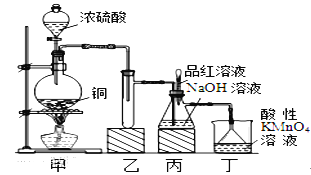
(1)装置甲中发生反应的化学方程式是________________,装置乙的作用是___________。
(2)装置丁的作用是吸收污染空气的SO2气体,其反应的离子方程为___________________。
(3)SO2气体有漂白性、还原性和氧化性。将SO2通入溴水中,SO2表现的是__________性,化学反应方程式为_________________________________。
(4)反应过程中,将丙中滴管里的品红溶液滴入锥形瓶,若现象为_____________,则溶液中的NaOH完全转化为了NaHSO3。
(5)若丙中没有加入品红溶液,则不能准确判断氢氧化钠是否完全转化。现有可供选择的仪器和试剂:烧杯、试管、玻璃棒、胶头滴管; 2mol/L盐酸、2mol/L硝酸、1mol/L氯化钡溶液、1 mol/L氢氧化钡溶液、品红溶液、蒸馏水。请设计实验探究吸收后产物中是否存在NaHSO3和Na2SO3,将实验操作、预期的实验现象和结论填在下表中。
实验操作 | 预期现象与结论 |
步骤1:取少量待测液放入试管中,滴加过量1 mol/L氯化钡溶液。静置一段时间后,得到滤液A和固体B。 | (空) |
步骤2:往固体B中加入蒸馏水洗涤沉淀,静置后弃去上层清液,向固体滴入2滴(或少量)品红,再滴加__________________。 | 若品红褪色(或有气泡),则说明含有Na2SO3。 |
步骤3:用试管取少量A,向其中加入过量___________。 | 若生成白色沉淀,则说明有NaHSO3生成 |
【答案】 Cu+2H2SO4(浓) ![]() CuSO4+SO2↑+2H2O 防倒吸 2MnO4-+5SO2+2H2O=5SO42-+2Mn2++4H+ 还原 SO2+Br2+2H2O=H2SO4+2HBr 红色褪去 盐酸 Ba(OH)2溶液
CuSO4+SO2↑+2H2O 防倒吸 2MnO4-+5SO2+2H2O=5SO42-+2Mn2++4H+ 还原 SO2+Br2+2H2O=H2SO4+2HBr 红色褪去 盐酸 Ba(OH)2溶液
【解析】(1)浓硫酸与铜在加热的条件下反应的化学方程式为:Cu+2H2SO4(浓) ![]() CuSO4+SO2↑+2H2O;SO2气体易溶于NaOH溶液中,导致丙中导气管口压强减小而引起倒流,所以乙的作用是防倒吸。
CuSO4+SO2↑+2H2O;SO2气体易溶于NaOH溶液中,导致丙中导气管口压强减小而引起倒流,所以乙的作用是防倒吸。
(2)KMnO4具有强氧化性,与SO2发生氧化还原反应而除去SO2,对应的离子方程式为2MnO4-+5SO2+2H2O=5SO42-+2Mn2++4H+。
(3)Br2具有氧化性,能将SO2氧化为H2SO4,SO2表现还原性,对应的化学方程式为:SO2+Br2+2H2O=H2SO4+2HBr。
(4)SO2可以漂白品红溶液,使红色褪去,若NaOH完全转化为NaHSO3,说明通入的SO2气体是过量的,则将丙中滴管里的品红溶液滴入锥形瓶,品红溶液将会褪色,如果不褪色,说明SO2不过量,NaOH未完全转化为NaHSO3,答案为:红色褪去。
(5)步骤2中将沉淀洗涤干净,除去沉淀表面的具有干扰性的物质(NaHSO3),于沉淀上加几滴品红,再加少量稀盐酸,如果产生使品红褪色的气体,则沉淀为BaSO3,从而吸收后产物中含有Na2SO3;步骤3中取滤液A(已不含有Na2SO3),加入过量Ba(OH)2,如果产生白色沉淀,说明滤液中的物质为NaHSO3,从而吸收后产物中含有NaHSO3。


科目:高中化学 来源: 题型:
【题目】室温下,0.1 mol·L-1的某二元酸H2A溶液中,可能存在的含A粒子(H2A、HA-、A2-)的物质的量分数随pH变化的关系如图所示,下列说法正确的是( )

A. H2A的电离方程式:H2A![]() H++HA-
H++HA-
B. pH=5时,在NaHA和Na2A的混合溶液中:c(HA-):c(A2-)=1:100
C. 等物质的量浓度的NaHA和Na2A溶液等体积混合, 离子浓度大小关系为:c(Na+)>c(HA-)>c(A2-)
D. Na2A溶液必存在c(OH-)=c(H+)+c(HA-)+ 2c(H2A),各粒子浓度均大于0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W 是短周期元素,其在周期表的位置如图,请找出错误选项( )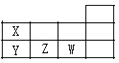
A.原子半径:Y>Z>W
B.酸性:HWO4>HXO3>H3YO4
C.热稳定性:HW>XH3>YH3
D.离子半径:Y3﹣<Z2﹣<W﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.写出下列反应的化学方程式,并指出反应类型:
(1)用乙烯制备聚乙烯:________________________________;反应类型_________。
(2)乙醇在加热有铜作催化剂的条件下反应:______________________________;反应类型__________。
(3)乙酸乙酯在稀硫酸加热条件下水解:_________________________________________;反应类型__________。
II.现有下列五种有机物:①CH4、②CH2=CH2、③CH3CH2OH、④ CH3 CH2CH2 CH3 、⑤CH3COOH。请回答:
(1)写出⑤的官能团的名称______。
(2)与①互为同系物的是______(填序号)。
(3)写出④ 的同分异构体的结构简式________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH3、H2S等是极性分子,CO2,BF3,CCl4等是含极性键的非极性分子。根据上述实例可推出ABn型分子是非极性分子的经验规律是( )
A. 分子中不能含有氢原子
B. 在ABn分子中A的相对原子质量应小于B的相对原子质量
C. 在ABn分子中A原子没有孤电子对
D. 分子中每个共价键的键长应相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列氯化物中,既能由金属和氯气直接化合制得,又能由金属和盐酸反应制得的是( )
①CuCl2 ②FeCl2 ③MgCl2 ④ZnCl2
A.③④B.②③C.②③④D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:
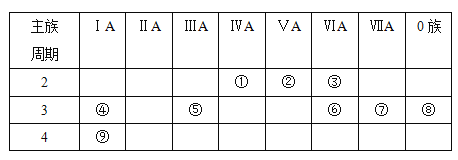
(1)在这些元素中,化学性质最不活泼的是________(填元素符号,下同)。
(2)从①到③的元素中,非金属性最强的是________
(3)在最高价氧化物的水化物中,酸性最强的化合物的化学式是_______,碱性最强的化合物的电子式是_________。
(4)最高价氧化物是两性氧化物的元素是_______;写出它的最高价氧化物与氢氧化钠反应的离子方程式_______________________________。
(5)用结构式表示元素①与③形成的一种可溶于水的化合物_________ 。
(6)写出元素④的单质与水反应的化学方程式________________________________。
(7)写出元素①的单质和元素⑥最高价氧化物对应水化物的浓溶液反应的化学方程式___________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是一个化学反应过程的示意图.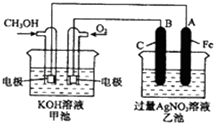
已知甲池的总反应式为:2CH3OH+3O2+4KOH=2K2CO3+6H2O
(1)请回答图中甲、乙两池的名称.甲电池是装置,乙池是装置.
(2)请回答下列电极的名称:通入CH3OH的电极名称是 , B(石墨)电极的名称是 .
(3)写出电极反应式:通入O2的电极的电极反应式是 . A(Fe)电极的电极反应式为 ,
(4)乙池中反应的化学方程式为 .
(5)当乙池中A(Fe)极的质量增加5.40g时,甲池中理论上消耗O2mL(标准状况下)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】国家规定,酿造食醋的总酸含量标准为3.5~5.0 g/100 mL(总酸含量即100 mL食醋中CH3COOH的质量).某化学兴趣小组为测定某市售食醋的总酸含量,进行了实验.实验后,得知10.0mL该食醋样品与7.5 g溶质的质量分数为4%的氢氧化钠溶液恰好完全反应.计算该市售食醋样品中的总酸含量,并说明是否符合国家标准.(假设该市售食醋样品中其他物质不与氢氧化钠发生反应)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com