
【题目】海水是重要的资源,可以制备一系列物质。下列说法不正确的是( )

A.要除去粗盐中![]() 、
、![]() 、
、![]() 等杂质,步骤
等杂质,步骤![]() 中所加试剂及相关操作顺序可以是过量NaOH溶液
中所加试剂及相关操作顺序可以是过量NaOH溶液![]() 过量
过量![]() 溶液
溶液![]() 过量
过量![]() 溶液
溶液![]() 过滤
过滤![]() 盐酸
盐酸
B.步骤![]() 的反应原理为
的反应原理为![]()
![]()
![]()
C.步骤![]() 中需将
中需将![]() 置于干燥的HCl气流中加热脱水制备无水
置于干燥的HCl气流中加热脱水制备无水![]()
D.步骤![]() 、
、![]() 、
、![]() 所涉及的反应中,溴元素均发生氧化反应
所涉及的反应中,溴元素均发生氧化反应
【答案】D
【解析】
A.选NaOH除去镁离子,选氯化钡除去硫酸根离子,选碳酸钠除去钙离子及过量的钡离子,过滤后加盐酸至中性;
B.电解饱和食盐水可生成NaOH、氢气、氯气;
C.加热促进镁离子水解,且生成盐酸易挥发,HCl可抑制水解;
D.步骤④中Br元素的化合价升高、⑤中Br元素的化合价降低、⑥中Br元素的化合价升高。
![]() 选NaOH除去镁离子,选氯化钡除去硫酸根离子,选碳酸钠除去钙离子及过量的钡离子,过滤后加盐酸至中性,则步骤①中所加试剂及相关操作顺序可以是过量NaOH溶液
选NaOH除去镁离子,选氯化钡除去硫酸根离子,选碳酸钠除去钙离子及过量的钡离子,过滤后加盐酸至中性,则步骤①中所加试剂及相关操作顺序可以是过量NaOH溶液![]() 过量
过量![]() 溶液
溶液![]() 过量
过量![]() 溶液
溶液![]() 过滤
过滤![]() 盐酸,故A正确;
盐酸,故A正确;
B. 电解饱和食盐水可生成NaOH、氢气、氯气,步骤②的反应原理为![]()
![]()
![]() ,故B正确;
,故B正确;
C. 加热促进镁离子水解,且生成盐酸易挥发,HCl可抑制水解,则步骤③中需将![]() 置于干燥的HCl气流中加热脱水制备无水
置于干燥的HCl气流中加热脱水制备无水![]() ,故C正确;
,故C正确;
D. 步骤④中Br元素的化合价升高、⑤中Br元素的化合价降低、⑥中Br元素的化合价升高,则步骤④、⑥中溴元素均发生氧化反应,⑤中溴元素被还原,故D错误;


科目:高中化学 来源: 题型:
【题目】在某一容积为2 L的密闭容器中,加入0.8 mol的H2和0.6 mol 的I2,在一定的条件下发生如下反应:H2(g)+I2(g) ![]() 2HI(g) ΔH<0反应中各物质的浓度随时间变化情况如图:
2HI(g) ΔH<0反应中各物质的浓度随时间变化情况如图:
(1)根据如图数据,反应开始至达到平衡时,平均速率v(HI)为________。
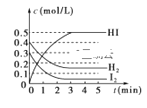
(2)反应达到平衡后,第8 min时:①若升高温度,化学平衡常数K________(填“增大”、“减小”或“不变”),HI浓度的变化正确的是________(用如图中a~c的编号回答)。
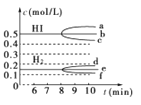
②若加入I2,H2浓度的变化正确的是________(用如图中d~f的编号回答)。
(3)反应达到平衡后,第8 min时,若反应容器的容积扩大一倍,请在图中画出8 min后HI浓度的变化情况。
 ______
______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是元素周期表中前四周期的五种常见元素,其原子序数依次增大。详细信息见表,请回答下列问题:
① | A的一种核素在考古时常用来鉴定一些文物的年代 |
② | B的氧化物是导致光化学烟雾的主要物质之一 |
③ | C的某一种单质是空气的主要成分之一 |
④ | D的基态原子核外有6个原子轨道处于半充满状态 |
⑤ | E能形成红色的E2O和黑色的EO两种氧化物 |
(1)D的价电子排布式可表示为_______。
(2)BC3-的空间构型为____ (用文字描述)。
(3)根据等电子原理,AC分子的结构式为_____。
(4)1 mol AC2中σ键、π键数目之比为____。
(5)将白色的ESO4溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配位数是4的配合离子。请写出生成此配合离子的离子方程式:____。
(6)E2+能与NH3、H2O、Cl-等形成配位数为4的配合物。
①[E(NH3)4]2+中存在的化学键类型有____(填序号)。
A.配位键 B.离子键 C.极性共价键 D.非极性共价键
②[E(NH3)4]2+具有对称的空间构型,[E(NH3)4]2+中的两个NH3被两个Cl-取代,能得到两种不同结构的产物,则[E(NH3)4]2+的空间构型为_____。其中,配体的杂化类型是_____。
(7)E的晶胞如下图所示,E为______堆积,空间利用率为_____,E晶体中每个E原子周围距离最近的E原子数目为____;已知E原子的半径为a nm,阿伏加德罗常数的值为NA,则E晶体的密度是_____g·cm-3。(列出算式即可)。
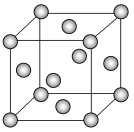
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用0.100 mol·L-1的KOH标准溶液滴定未知浓度的盐酸,其操作可分解为如下几步:
A.移取20 mL待测盐酸溶液注入洁净的锥形瓶中,并加入2~3滴酚酞;
B.用标准溶液润洗滴定管2~3次;
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管使尖嘴处充满溶液;
D.取标准KOH溶液注入碱式滴定管至刻度“0”以上2~3 cm 处;
E.调节液面至“0”或“0”以下刻度,记下读数;
F.把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点并记下滴定管液面的刻度。
就此实验完成填空:
(1)正确操作步骤的顺序是(用序号字母填写)__________________________。
(2)上述B步骤操作的目的是__________________________________________。
(3)上述A步骤操作之前,若先用待测溶液润洗锥形瓶,则滴定结果______(填“偏高“、“偏低”或“不变”)
(4)判断到达滴定终点的实验现象是________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组热化学方程式中,化学反应的ΔH前者大于后者的是( )
①C(s)+O2(g)= CO2(g)ΔH1;C(s)+ ![]() O2(g)= CO(g)ΔH2
O2(g)= CO(g)ΔH2
②S(s)+O2(g)= SO2(g)ΔH3;S(g)+O2(g)=SO2(g)ΔH4
③H2(g)+ ![]() O2(g)=H2O(l)ΔH5;2H2(g)+O2(g)= 2H2O(l)ΔH6
O2(g)=H2O(l)ΔH5;2H2(g)+O2(g)= 2H2O(l)ΔH6
④CaCO3(s)= CaO(s)+CO2(g)ΔH7;CaO(s)+H2O(l)= Ca(OH)2(s)ΔH8
A.①B.④C.②③④D.①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究化学反应与能量的变化具有重要意义。
![]() 已知
已知![]() 的反应过程的能量变化如图1:
的反应过程的能量变化如图1:

![]() 该反应通常用
该反应通常用![]() 作为催化剂,加入
作为催化剂,加入![]() 会使图中的B点________
会使图中的B点________![]() 填“升高”、“不变”或“降低”
填“升高”、“不变”或“降低”![]() 。
。
![]() E
E![]() 表示的意义为___________。
表示的意义为___________。
![]() 如图2中的a和b为氢镍可充电碱性电池的电极,该电池总反应式为:
如图2中的a和b为氢镍可充电碱性电池的电极,该电池总反应式为:![]()
![]() 为了实现铜与稀硫酸反应,用Z通入氧气的同时,将开关K与Y相连即可。石墨电极的反应式为___________,总反应的化学方程式为__________。
为了实现铜与稀硫酸反应,用Z通入氧气的同时,将开关K与Y相连即可。石墨电极的反应式为___________,总反应的化学方程式为__________。
![]() 不通入氧气,直接将K与X相连也能实现铜与稀硫酸反应。则氢镍碱性电池的负极为____
不通入氧气,直接将K与X相连也能实现铜与稀硫酸反应。则氢镍碱性电池的负极为____![]() 填“a”或“b”
填“a”或“b”![]() ,电解槽内总反应的离子方程式为______________________。
,电解槽内总反应的离子方程式为______________________。
![]() 当给氢镍碱性电池充电时,该电池的正极反应式为______;氢镍电池放电时,负极附近的pH会________
当给氢镍碱性电池充电时,该电池的正极反应式为______;氢镍电池放电时,负极附近的pH会________![]() 填“变大”、“不变”或“变小”
填“变大”、“不变”或“变小”![]() 。
。
![]() 若将
若将![]() 题图2中的稀硫酸换成
题图2中的稀硫酸换成![]() 溶液,并且将氢镍碱性电池的电极反接,将K连接X,通电一段时间后,向所得溶液中加入
溶液,并且将氢镍碱性电池的电极反接,将K连接X,通电一段时间后,向所得溶液中加入![]() 碱式碳酸铜
碱式碳酸铜![]() 后,恰好恢复到原来的浓度和
后,恰好恢复到原来的浓度和![]() 不考虑
不考虑![]() 的溶解
的溶解![]() ,则电解过程中转移电子的物质的量为__________。
,则电解过程中转移电子的物质的量为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氯化二硫(S2Cl2)是一种重要的化工原料,常用作橡胶硫化剂,改变生橡胶受热发粘、遇冷变硬的性质。查阅资料可知S2Cl2具有下列性质:
物理性质 | 毒性 | 色态 | 挥发性 | 熔点 | 沸点 |
剧毒 | 金黄色液体 | 易挥发 | -76℃ | 138℃ | |
化学性质 | ①300℃以上完全分解;②S2Cl2+Cl2 ③遇高热或与明火接触,有引起燃烧的危险 ④受热或遇水分解放热,放出腐蚀性烟气 | ||||
(1)制取少量S2Cl2
实验室可利用硫与少量氯气在110~140℃反应制得S2Cl2粗品,氯气过量则会生成SCl2。

①仪器m的名称为__,装置F中的试剂作用是__。
②装置连接顺序:__→__→__→__→__→D。__
③实验前打开K1,通入一段时间的氮气排尽装置内空气。实验结束停止加热后,再通入一段时间的氮气,其目的是__。
④为了提高S2Cl2的纯度,实验的关键是__。(写两点)
(2)S2Cl2有剧毒,少量S2Cl2泄漏时应喷水雾减慢其挥发(或扩散)。S2Cl2遇水会生成SO2、HCl两种气体,写出该反应的化学方程式__。
(3)某同学设计了如下实验方案来测定S2Cl2与水反应后的混合气体中SO2的体积分数。
![]()
①W溶液可以是__(填标号)。
a.H2O2溶液 b.KMnO4溶液(硫酸酸化) c.氯水
②该混合气体中二氧化硫的体积分数为__(用含V、m的式子表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组分别用下图所示装置对原电池和电解原理进行实验探究.
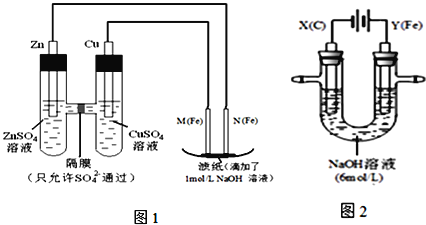
请回答:
I.用图1所示装置进行第一组实验.
(1)在保证电极反应不变的情况下,不能替代Cu做电极的是______(填字母序号).
A.铝 B.石墨 C.银 D.铂
(2)N极发生反应的电极反应式为_____________.
(3)实验过程中,SO42-______(填“从左向右”、“从右向左”或“不”)移动;滤纸上能观察到的现象有______________.
II.用图2所示装置进行第二组实验.实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清.查阅资料发现,高铁酸根(FeO42-)在溶液中呈紫红色.
(4)电解过程中,X极区溶液的pH______(填“增大”、“减小”或“不变”).
(5)电解过程中,Y极发生的电极反应为_____________和4OH-- 4e-= 2H2O + O2↑
(6)若在X极收集到672mL气体,在Y极收集到168mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少______g.
(7)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为:2K2FeO4+3Zn═Fe2O3+ZnO+2K2ZnO2 该电池正极发生的反应的电极反应式为__________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.室温时某溶液的pH<7,则该物质一定是酸或强酸弱碱盐
B.已知室温时,0.1mol·L-1某一元酸HA的电离平衡常数为1×10-7,则该酸的电离度约为0.01%
C.0.02mol·L-1CH3COOH溶液和0.01mol·L-1NaOH溶液等体积混合,则溶液中: 2c(H+)+c(CH3COOH)=2c(OH-)+c(CH3COO-)
D.在温度不变的条件下向CaSO4饱和溶液中加入Na2SO4溶液,CaSO4将会析出,但Ksp不会发生改变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com