
【题目】二氯化二硫(S2Cl2)是一种重要的化工原料,常用作橡胶硫化剂,改变生橡胶受热发粘、遇冷变硬的性质。查阅资料可知S2Cl2具有下列性质:
物理性质 | 毒性 | 色态 | 挥发性 | 熔点 | 沸点 |
剧毒 | 金黄色液体 | 易挥发 | -76℃ | 138℃ | |
化学性质 | ①300℃以上完全分解;②S2Cl2+Cl2 ③遇高热或与明火接触,有引起燃烧的危险 ④受热或遇水分解放热,放出腐蚀性烟气 | ||||
(1)制取少量S2Cl2
实验室可利用硫与少量氯气在110~140℃反应制得S2Cl2粗品,氯气过量则会生成SCl2。

①仪器m的名称为__,装置F中的试剂作用是__。
②装置连接顺序:__→__→__→__→__→D。__
③实验前打开K1,通入一段时间的氮气排尽装置内空气。实验结束停止加热后,再通入一段时间的氮气,其目的是__。
④为了提高S2Cl2的纯度,实验的关键是__。(写两点)
(2)S2Cl2有剧毒,少量S2Cl2泄漏时应喷水雾减慢其挥发(或扩散)。S2Cl2遇水会生成SO2、HCl两种气体,写出该反应的化学方程式__。
(3)某同学设计了如下实验方案来测定S2Cl2与水反应后的混合气体中SO2的体积分数。
![]()
①W溶液可以是__(填标号)。
a.H2O2溶液 b.KMnO4溶液(硫酸酸化) c.氯水
②该混合气体中二氧化硫的体积分数为__(用含V、m的式子表示)。
【答案】直形冷凝管(或冷凝管) 除去Cl2中混有的HCl杂质 AFCBE 将装置内的氯气排入D内吸收以免污染空气,并将B中残留的S2Cl2排入E中收集 控制反应的温度、控制滴入浓盐酸的速率 S2Cl2+2H2O=4HCl+SO2+3S ac ![]() ×100%或
×100%或![]() %或
%或![]() %或
%或![]() %
%
【解析】
实验室利用硫与少量氯气在110~140℃反应制得S2Cl2粗品时,依据S2Cl2的性质,则需先去除HCl,再进行干燥,以防其水解;同时需要控制温度,以防受热分解放热,放出腐蚀性烟气;产物应冷却,以防遇高热或与明火接触,有引起燃烧的危险。
(1)①仪器m的名称为直形冷凝管(或冷凝管),Cl2中混有的HCl需要除去,所以装置F中的试剂作用是除去Cl2中混有的HCl杂质。
②制取气体时,需先除去HCl、水蒸气,然后发生Cl2与S的反应,产品需要冷凝,尾气需要处理,所以装置连接顺序:AFCBE。
③S2Cl2会污染环境,实验结束停止加热后,再通入一段时间的氮气,其目的是将装置内的氯气排入D内吸收以免污染空气,并将B中残留的S2Cl2排入E中收集。
④因为温度高,S2Cl2遇高热或与明火接触,有引起燃烧的危险;受热或遇水分解放热,放出腐蚀性烟气,所以为了提高S2Cl2的纯度,实验的关键是控制反应的温度、控制滴入浓盐酸的速率。答案为:直形冷凝管(或冷凝管);除去Cl2中混有的HCl杂质;AFCBE;将装置内的氯气排入D内吸收以免污染空气,并将B中残留的S2Cl2排入E中收集;控制反应的温度、控制滴入浓盐酸的速率;
(2)S2Cl2遇水会生成SO2、HCl两种气体,依据价态变化规律,同时会生成硫,该反应的化学方程式为S2Cl2+2H2O=4HCl+SO2+3S。答案为:S2Cl2+2H2O=4HCl+SO2+3S;
(3)①因为实验的目的是将SO2氧化为硫酸,但KMnO4溶液(硫酸酸化)会将HCl氧化为Cl2,所以W溶液可以是ac。
②m(BaSO4)=mg,则该混合气体中二氧化硫的体积分数为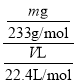 =
=![]() ×100%或
×100%或![]() %或
%或![]() %或
%或![]() %。答案为:
%。答案为:![]() ×100%或
×100%或![]() %或
%或![]() %或
%或![]() %。
%。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】电化学原理在防止金属腐蚀、能量转换、物质合成等方面应用广泛。

(1)图1中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择__________(填字母)。
a.碳棒b.锌板c.铜板

(2)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。图2为“镁—次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。
①E为该燃料电池的________(填“正”或“负”)极。F电极上的电极反应式为____________________________________________________________。
②镁燃料电池负极容易发生自腐蚀产生氢气,使负极利用率降低,用化学用语解释其原因_________________________________________________________________________。

(3)乙醛酸(HOOC-CHO)是有机合成的重要中间体。工业上用“双极室成对电解法”生产乙醛酸,原理如图3所示,该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸。
①N电极上的电极反应式为_______________________________________________________。
②若有2mol H+通过质子交换膜,并完全参与了反应,则该装置中生成的乙醛酸为________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W、X、Y、Z原子的最外层电子数之和为21,下列说法中不正确的是

A. 原子半径:X>Y>W
B. 简单阴离子的还原性:Z>W
C. 气态氢化物的稳定性:W>Y
D. 氧化物对应水化物的酸性:Z>Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水是重要的资源,可以制备一系列物质。下列说法不正确的是( )

A.要除去粗盐中![]() 、
、![]() 、
、![]() 等杂质,步骤
等杂质,步骤![]() 中所加试剂及相关操作顺序可以是过量NaOH溶液
中所加试剂及相关操作顺序可以是过量NaOH溶液![]() 过量
过量![]() 溶液
溶液![]() 过量
过量![]() 溶液
溶液![]() 过滤
过滤![]() 盐酸
盐酸
B.步骤![]() 的反应原理为
的反应原理为![]()
![]()
![]()
C.步骤![]() 中需将
中需将![]() 置于干燥的HCl气流中加热脱水制备无水
置于干燥的HCl气流中加热脱水制备无水![]()
D.步骤![]() 、
、![]() 、
、![]() 所涉及的反应中,溴元素均发生氧化反应
所涉及的反应中,溴元素均发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。 请回答:

(1)B极是电源的__________极,C极的电极反应式为____________________________________,一段时间后丁中X极附近的颜色逐渐______________。(填“变深”或者“变浅”)
(2)若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为 ______________。
(3)现用丙装置给铜件镀银,则H应该是______________ (填“铜”或“银”),电镀液是___________ 溶液。当乙中溶液的pH是13时(此时乙溶液体积为500mL),丙中镀件上析出银的质量为________ g,甲中溶液的pH _____________(填“变大”、“变小”或“不变”)。
(4)若甲烧杯是在铁件表面镀铜,已知电镀前两电极质量相同,电镀完成后将它们取出,洗净、烘干、称量,发现二者质量相差5.12g,则电镀时电路中通过的电子为_______mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中发生反应I2(g) + H2(g)![]() 2HI(g) ΔH =-14.9 kJ·mol-1,能说明反应已经达到化学平衡状态的是
2HI(g) ΔH =-14.9 kJ·mol-1,能说明反应已经达到化学平衡状态的是
A.各物质的浓度相等
B.反应容器内压强不变
C.容器内颜色不再变化
D.单位时间内断裂a mol H-H键,同时形成2a mol H-I键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用化学平衡移动原理解释的是( )
A.向AgCl浊液中加入少量KI溶液,可看到白色沉淀变为黄色沉淀
B.高压比常压更有利于N2和H2转化为NH3
C.蒸干AlCl3溶液无法得到无水AlCl3
D.滴加少量CuSO4溶液可以加快Zn与稀H2SO4反应的速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中,对应的现象以及解释或结论都正确且两者具有因果关系的是
选项 | 实验 | 现象 | 解释或结论 |
A | 向足量的浓硝酸中加入铁片,一段时间后加入铜粉 | 有气体生成,溶液呈蓝绿色 | 浓硝酸将Fe氧化为 |
B | 分别向 | 均有白色沉淀产生 | 金属性: |
C | 表面变黑的银器浸泡到盛有食盐水的铝制容器中,银器与铝接触 | 银器变得光亮如新 | 构成原电池,铝做负极,硫化银得电子被还原成单质银 |
D | 向 | 白色沉淀逐渐变为浅蓝色 |
|
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 常温下,10 mL 0.02 mol·L-1 HCl溶液与10 mL 0.02 mol·L-1 Ba(OH)2溶液充分混合,若混合后溶液的体积为20 mL,则溶液的pH=12
B. 在0.1 molL﹣1 CH3COONa溶液中:n(OH﹣)+0.1mol>n(CH3COOH)+n(H+)+n(Na+)
C. 在10mL 0.1 mol/L的AgNO3溶液中加入6mL等浓度的NaCl溶液,有白色沉淀产生,再加入6 mL等浓度的Na2S溶液,溶液中又有黑色沉淀生成,说明Ksp(Ag2S)< Ksp(AgCl)
D. 常温下pH=4的NaHC2O4溶液中:c(H2C2O4)>c(C2O42-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com