
【题目】某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生反应的化学方程式有________________________________________________。
(2)硫酸铜溶液可以加快氢气生成速率的原因是__________________________________________。
(3)实验室中现有Na2SO4、MgSO4、Ag2SO4、K2SO4等4种溶液,可与上述实验中CuSO4溶液起相似作用的是________;
(4)要加快上述实验中气体产生的速率,还可采取的措施有______________(答两种);
(5)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列的实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需的时间。
A | B | C | D | E | F | |
4 mol·L-1H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
①请完成此实验设计,其中:V1=________,V6=________,V9=________。
②反应一段时间后,实验E中的金属呈________色;
③该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高,但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因________________________________________________________。
【答案】(1)CuSO4+Zn![]() ZnSO4+Cu,Zn+H2SO4===ZnSO4+H2↑(2分)
ZnSO4+Cu,Zn+H2SO4===ZnSO4+H2↑(2分)
(2)CuSO4与Zn反应产生的Cu与Zn形成Cu-Zn微电池,加快了氢气产生的速率(2分)
(3)Ag2SO4(1分)
(4)升高反应温度、适当增加硫酸的浓度、增加锌粒的比表面积等(答两种即可)(2分)
(5)①30(1分) 10(1分) 17.5(1分) ②暗红(1分)
③当加入一定量的CuSO4后,生成的单质Cu会沉积在Zn的表面,降低了Zn与溶液的接触面积(2分)
【解析】(1)在稀硫酸中加入硫酸铜后发生了两个反应:CuSO4+Zn===ZnSO4+Cu、Zn+H2SO4===ZnSO4+H2↑。(2)由于Zn与反应生成的Cu及硫酸铜溶液组成了Cu-Zn微电池,大大加快了生成氢气的反应速率。(3)只要是比锌的金属性差的金属都可以与锌组成原电池,都可以加快生成氢气的反应速率,故在所给的物质中只有Ag2SO4符合题意。(4)要加快生成氢气的反应速率,还可以采取如下措施:升高温度、适当增大硫酸的浓度、增加锌粒的比表面积等。(5)因为要研究硫酸铜的量对反应速率的影响,故应保持硫酸的浓度在各组实验中相同,则硫酸溶液的体积均取30 mL,根据F中增加的水与硫酸铜溶液的体积之和为20 mL,可以求得各组实验中加入水的体积分别为V7=20 mL,V8=19.5 mL,V9=17.5 mL,V10=15 mL。E中析出较多的铜,则显示出了铜晶体的颜色:暗红色。由于析出的铜的量较多,会覆盖在锌的表面,使得锌与稀硫酸的接触面积大大减小,故反应速率反而会减慢了。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】在一定温度下的恒容容器中,当下列物理量不变时,不能表明反应:A(s)+2B(g)C(g)+D(g)已达到平衡的是( )
A.混合气体压强
B.混合气体的密度
C.混合气体的平均相对分子质量
D.B的物质的量浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质分类正确的是
A. SO2、SiO2、CO均为酸性氧化物 B. 稀豆浆、硅酸、氯化铁溶液均为胶体
C. 烧碱、冰醋酸、蔗糖均为电解质 D. 盐水、水玻璃、氨水均为混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中新社北京2017年2月25日电,总装机达到672万千瓦的世界在役最大火力发电厂在内蒙古投入商业运营。火力发电排放的CO、CO2、SO2等物质对环境影响极大,需分离并进行利用,变废为宝。
(1)火电产生的CO在高温下可将SO2还原为S,已知:
C(s)+O2(g)CO2(g) ΔH1=a kJ·mol1
CO2(g)+C(s)2CO(g) ΔH2=+b kJ·mol1
S(s)+O2(g)SO2(g) ΔH3=c kJ·mol1
①a、b、c均大于0,请写出CO除SO2的热化学方程式:__________________________。
②根据传感器记录某温度下CO、SO2的反应进程,测量SO2浓度与时间数据绘制出如图,前1 min内用生成物表示的化学反应速率为_____________,第2 min时的X值范围为_____________。

(2)火力发电厂CO主要来源于反应:C(s)+CO2(g)![]() 2CO(g)。若一定量的CO2与足量的碳在体积可变的恒压密闭容器中发生该反应,其压强为p,平衡时,体系中气体体积分数与温度的关系如图所示:
2CO(g)。若一定量的CO2与足量的碳在体积可变的恒压密闭容器中发生该反应,其压强为p,平衡时,体系中气体体积分数与温度的关系如图所示:

①T℃时,若充入氮气,平衡向_____________(填“正反应方向移动”“逆反应方向移动”或“不移动”)。
②用平衡分压代替平衡浓度计算,其中,分压=总压×物质的量分数。则800℃时的平衡常数Kp=____________(列式即可,气体总压可记作p总)。
(3)CO在高温下与H2O反应可获得合成氨所需H2,若在等容条件下合成氨:N2(g)+3H2(g)![]() 2NH3(g)(ΔH<0),改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如图所示:
2NH3(g)(ΔH<0),改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如图所示:

①H2的平衡转化率αⅠ(H2)、αⅡ(H2)、αⅢ(H2)中最大的是___________,其值是___________。
②由第一次平衡到第二次平衡,采取的措施是______________________。
③比较第Ⅱ阶段反应温度(T2)和第Ⅲ阶段反应温度(T3)的高低:T2__________T3(填“<”“>”或“=”),判断的理由是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将1.000 mol·L-1盐酸滴入20.00 mL 1.000 mol·L-1氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示。下列有关说法正确的是( )

A. a点由水电离出的c(H+)=1.0×10-14 mol·L-1
B. b点:c(NH![]() )+c(NH3·H2O)=c(Cl-)
)+c(NH3·H2O)=c(Cl-)
C. c点:c(Cl-)=c(NH![]() )
)
D. d点后,溶液温度略下降的主要原因是NH3·H2O电离吸热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】全钒液流电池足一种新型的绿色环保储能电池。其电池总反应为:V3++VO2++H2O ![]() VO2++2H++V2+,下列说法正确的是
VO2++2H++V2+,下列说法正确的是
A.放电时正极反应为:VO2++2H++e-=VO2++H2O
B.充电时阴极反应为:V2+-e-=V3+
C.放电过程中电子由负极经外电路移向正极,再由正极经电解质溶液移向负极
D.充电过程中,H+由阴极区向阳极区迁移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个体积恒定的密闭容器中,加入2 mol A和1 mol B发生反应:2A(g)+B(g)![]() 3C(g)+D(g),一定条件下达到平衡时,C的浓度为W mol·L1,若容器体积和温度保持不变,按下列四种配比作为起始物质,达到平衡后,C的浓度仍为W mol·L1的是
3C(g)+D(g),一定条件下达到平衡时,C的浓度为W mol·L1,若容器体积和温度保持不变,按下列四种配比作为起始物质,达到平衡后,C的浓度仍为W mol·L1的是
A.4 mol A+2 mol B
B.3 mol C+1 mol D
C.2 mol A+1 mol B+3 mol C+1 mol D
D.1 mol A+0.5 mol B+3 mol C+1 mol D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】G是一种新型香料的主要成分之一,其结构中含有三个六元环。G的合成路线如下(部分产物和部分反应条件略去):

已知:
①B中核磁共振氢谱图显示分子中有6种不同环境的氢原子;
②D和F互为同系物。
请回答下列问题:
(1)(CH3)2C=CH2的系统命名法名称为 ,生成B这一步的反应类型为 。
(2)E的结构简式为 ,F分子中含有的含氧官能团名称是 。
(3)C经氧化后可得到一种能与新制银氨溶液发生银镜反应的物质,请写出该银镜反应的化学方程式 。
(4)F可在一定条件下合成高分子化合物,请写出该高分子化合物的结构简式 。
(5)同时满足下列条件:①与FeCl3溶液发生显色反应;②苯环上有两个取代基;③能与碳酸氢钠溶液反应放出气体;这样的D的同分异构体共有 种(不包括立体异构);
(6)请参照合成路线中苯乙烯合成F的方法,写出由1-丁烯制取2-羟基丁酸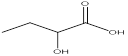 的合成线路: 。
的合成线路: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据路透社北京报道,中国石油计划2017年加大在四川省的页岩气开发,制订了在2020年前新增100亿立方米页岩气产能的计划。页岩气主要成分为CH4,请回答下列问题:
(1)页岩气不仅能用作燃料,还可用于生产合成气(CO与H2的混合气),已知:CH4与H2O(g)通入聚焦太阳能反应器,会发生下列反应:CH4(g)+H2O(g)![]() CO(g)+3H2(g) ΔH=+206 kJ·mol1 ①;又知CH4(g)+2O2(g)
CO(g)+3H2(g) ΔH=+206 kJ·mol1 ①;又知CH4(g)+2O2(g)![]() CO2(g)+2H2O(g) ΔH=802 kJ·mol1②,则CO2与H2O(g)反应生成CO的热化学方程式为_____________。
CO2(g)+2H2O(g) ΔH=802 kJ·mol1②,则CO2与H2O(g)反应生成CO的热化学方程式为_____________。
(2)用合成气生产CH3OH的反应为:CO(g)+2H2(g)![]() CH3OH(g) ΔH。在10 L的恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的转化率随温度的变化及不同压强下CO的转化率变化如图所示,p2和200 ℃时n(H2)随时间变化结果如表所示。
CH3OH(g) ΔH。在10 L的恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的转化率随温度的变化及不同压强下CO的转化率变化如图所示,p2和200 ℃时n(H2)随时间变化结果如表所示。

p2和200 ℃时n(H2)随时间变化
t/min | 0 | 1 | 3 | 5 |
n(H2)/mol | 8 | 5 | 4 | 4 |
①ΔH________0(填“<”“=”或“>”)。
②你认为可同时提高反应速率和H2转化率的措施是___________________(列举两条即可)。
③下列说法正确的是_________(填字母)。
A.温度越高,该反应的平衡常数越大
B.达平衡后再充入稀有气体,H2转化率将提高
C.体系内气体压强不变时,反应达到最大限度
D.图中压强p1<p2
④在p2和200 ℃时,反应0~3 min内,用CH3OH表示的平均反应速率v(CH3OH)=
___________________。
⑤在p2和200 ℃时,达平衡后再加入2 mol CO、2 mol H2、2 mol CH3OH,化学平衡______________(填“向正反应方向移动”“向逆反应方向移动”或“不移动”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com