
����Ŀ����ijһ�¶��£�ijһ�ܱ������У�M��N��R��������Ũ�ȵı仯��ͼa��ʾ���������������䣬���¶ȷֱ�ΪT1��T2ʱ��N�����������ʱ���ϵ��ͼb��ʾ�������н�����ȷ���ǣ������� 
A.�÷�Ӧ���Ȼ�ѧ����ʽM��g��+3N��g��2R��g����H��0
B.�ﵽƽ����������������䣬��С���������ƽ�����淴Ӧ�����ƶ�
C.�ﵽƽ����������������䣬�����¶ȣ������淴Ӧ�ٶȾ�����M��ת���ʼ�С
D.�ﵽƽ����������������䣬ͨ��ϡ�����壬ƽ��һ��������Ӧ�����ƶ�
���𰸡�C
���������⣺A����ͼa�ɵó�M��NΪ��Ӧ�RΪ������ɡ�c֮�ȿ�֪��ѧ������֮�ȣ��÷�ӦΪM��g��+3N��g��2R��g������ͼb��Ҳ����T1��T2�������¶ȣ�N������������ƽ�������ƶ����ʸ÷�ӦΪ���ȷ�Ӧ����H��0����A����
B����С�����������������ѹǿ��ƽ�������ƶ�����B����
C�������¶ȣ�v����v��������ƽ�������ƶ���M��ת���ʼ�С����C��ȷ��
D�������ں��º��ݵ�������ͨ��ϡ�����壬��ƽ�ⲻ�ƶ�����D����
��ѡC��
A����ͼb��Ҳ����T1��T2�������¶ȣ�N������������
B����С�����������������ѹǿ��
C�������¶ȣ�v����v��������ƽ�������ƶ���
D������ʱ��ͨ��ϡ�����壬M��N��R��Ũ�Ȳ��䣮


 ��ѧȫ��������ѵ��ϵ�д�
��ѧȫ��������ѵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Է���һ����Ҫ���л�����ԭ�ϡ����ñ��Ӻϳ��Ѷ�ȩ[OHC(CH2)4CHO]������6(![]() )�ĺϳ�·������:
)�ĺϳ�·������:

��֪:I.  ��
��
II.  ��
��
�ش���������:
��1����A��ȡB�ķ�Ӧ����Ϊ_______��C�Ļ�ѧ����Ϊ___________��
��2��E�Ľṹ��ʽΪ____________��
��3�����������кϳ�����6�Ļ�ѧ����ʽΪ_____________________��
��4���Ѷ�ȩ��������Һ��Ӧ�Ļ�ѧ����ʽΪ___________________��
��5���Ѷ�ȩ��ͬ���칹���мȺ���Ԫ���ṹ���ֺ��� �� �ṹ����_____��(�����������칹)�����к˴Ź��������������Ľṹ��ʽ��_________________��
�� �ṹ����_____��(�����������칹)�����к˴Ź��������������Ľṹ��ʽ��_________________��
��6��д����������Ϊԭ��(�����Լ���ѡ)�Ʊ���ȩ�ĺϳ�����:_______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Һ�п��Դ������棬��OH��������������H+���������һ�������ǣ� ��
A.Na+��Cu2+��CO32����Cl��
B.Na+�� Cl���� HCO3����Mg2+
C.Cl����NO3����K+�� Ca2+
D.NH4+�� K+�� H+�� SO42��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ӦA��B�D��C���������У���A��B�D��X����X�D��C����Ӧ�����������仯��ͼ��ʾ��E1��ʾ��ӦA��B�D��X�Ļ�ܡ������й�������ȷ����(����)
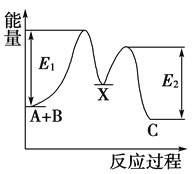
A. E2��ʾ��ӦX�D��C�Ļ��
B. X�Ƿ�ӦA��B�D��C�Ĵ���
C. ��ӦA��B�D��C�Ħ�H<0
D. ��������ɸı䷴ӦA��B�D��C���ʱ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ����٤��������ֵ����������������ǣ�������
A.1.8g18O2������1.8g18O3�����к��е���������ͬ
B.7.8gNa2S��7.8g Na2O2�к��е���������Ŀ��Ϊ0.1NA
C.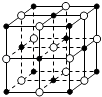 23.4 g NaCl�����к���0.1NA����ͼ��ʾ�Ľṹ��Ԫ
23.4 g NaCl�����к���0.1NA����ͼ��ʾ�Ľṹ��Ԫ
D.��16 g��ԭ�ӵĶ������辧���к��еĦļ���ĿΪ2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������գ�
��1��������ˮ��Һ�д��ڵ�������֣����ӣ�CN��2�м����֮��ļн�Ϊ180�㣬���жԳ��ԣ�������ÿ��ԭ������������8�����ȶ��ṹ����ṹʽΪ �� 1�������к������м���
��2�����������仯�����ںϽ�����Լ������ȷ���Ӧ�ù㷺��NiO�ľ���ṹ�������Ȼ��Ƶ���ͬ��NiO������Ni��O����λ����Ϊ���ܶ�����л�����Ni���¿���H2�����ӳɷ�Ӧ�����CH2=CH2����HC��CH���� ![]() ����HCHO�ȣ�����̼ԭ�Ӳ��Dz�ȡsp2�ӻ��ķ������������ʱ�ţ���HCHO���ӵ����幹��Ϊ ��
����HCHO�ȣ�����̼ԭ�Ӳ��Dz�ȡsp2�ӻ��ķ������������ʱ�ţ���HCHO���ӵ����幹��Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪A��g��+B��g��C��g��+D��g����Ӧ��ƽ�ⳣ�����¶ȵĹ�ϵ���£�
�¶�/�� | 700 | 900 | 830 | 1000 | 1200 |
ƽ�ⳣ�� | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
�ش��������⣺
��1���÷�Ӧ��ƽ�ⳣ������ʽK= �� ��H0���������������=������
��2��830��ʱ����һ��5L���ܱ������г���0.20mol��A��0.80mol��B���練Ӧ��ʼ6s��A��ƽ����Ӧ����v��A��=0.003molL��1s��1 �� ����6sʱc��A��= molL��1 �� C�����ʵ���Ϊmol������Ӧ��һ��ʱ��ﵽƽ��ʱA��ת����Ϊ �� �����ʱ����ܱ��������ٳ���1mol�����ƽ��ʱA��ת����Ϊ��
��3���жϸ÷�Ӧ�Ƿ�ﵽƽ�������Ϊ������ȷѡ��ǰ����ĸ���� a��ѹǿ����ʱ��ı� b��������ܶȲ���ʱ��ı�
c��c��A������ʱ�ʸı� d����λʱ��������c��D�����ʵ������
��4��1200��ʱ��ӦC��g��+D��g��A��g��+B��g����ƽ�ⳣ����ֵΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС��Ҫ����к��ȵIJⶨ���ش��������⣺
��1��ʵ�����ϱ��д�С�����ձ�����ĭ���ϡ���ĭ���ϰ塢��ͷ�ιܡ����β����������0.5molL��1���ᡢ0.55molL��1NaOH��Һ��ʵ����ȱ�ٵIJ�����Ʒ�� ��
��2����֪����Ӧ����Һ�ı�����cΪ4.18J����1g��1 �� 0.5molL��1�����0.55molL��1NaOH��Һ���ܶȾ�Ϊ1gcm��3 �� ʵ��ʱ��¼��ʵ�����������
ʵ�� | ��Ӧ�P���� | �� Һ �� �� | ||
t1 | t2 | |||
1 | 50mL0.55molL��1NaOH��Һ | 50mL.0.5molL��1HCl��Һ | 20�� | 23.3�� |
2 | 50mL0.55molL��1NaOH��Һ | 50mL.0.5molL��1HCl��Һ | 20�� | 23.5�� |
��������������Ʒ�Ӧ���к��ȡ�H1=��������λС����
����֪��CH3COOH��aq��CH3COO����aq��+H+��aq����H2��0��
CH3COOH��aq��+OH����aq��=CH3COO����aq��+H20��l����H3 ���H3��H1�������������������=����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com