
【题目】设NA表示阿伏加德罗常数的值,下列判断正确的是( )
A.在常温常压下,48 g氧气和臭氧的混合气体含氧原子数是3NA
B.标准状况下,22.4 L H2O中含有的原子数目为3NA
C.同温同压下,NA个CO2与NA个N2和O2的混合气体的体积不相等
D.物质的量浓度为0.5 mol·L-1的MgCl2溶液中,含有Cl-数为NA
科目:高中化学 来源: 题型:
【题目】Na5PW11O39Cu/T1O2膜可催化污染物的光降解,一种生产工艺流程如下,回答下列问题:

(1)“溶解I”发生的离子反应方程式为______________,Na2WO4 (钨酸钠)在酸性条件下有较强的氧化性,该步骤不能用浓盐酸代替浓硝酸的原因是____________。
(2)“除杂”时用过量有机溶剂萃取溶液中的NO3-,再通过_________方法分离杂质。
(3)“溶解II”需要加入水、乙醇和稀硫酸。
①加入乙醇的目的是_____________。
②钛酸四丁酯水解产生TiO2和C4H9OH的化学方程式为_____。
③溶液中Cu2+浓度为0.02 mol·L-1,需调节pH小于________。(已知Ksp[Cu(OH)2]=2×10-20)
(4)培烧温度、Na5PW11O39Cu 用量对Na5PW11O39Cu/TiO2膜催化活性的影响随(时间)变化如图1、图2所示:
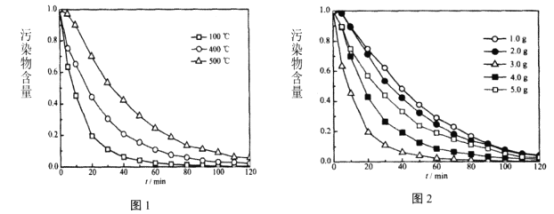
制备Na5PWl1O39Cu/TiO2膜的最佳条件为:培烧温度_____,Na5PW11O39Cu用量_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物的转化过程如图所示。下列分析合理的是

A. 催化剂a表面发生了极性共价键的断裂和形成
B. N2与H2反应生成NH3的原子利用率为100%
C. 在催化剂b表面形成氮氧键时,不涉及电子转移
D. 催化剂a、b能提高反应的平衡转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在没有氧气存在时,铁与水几乎不反应,但高温下,铁能与水蒸气反应。请设计实验,证明还原铁粉与水蒸气能够发生反应。
(1)铁粉与水蒸气反应的化学方程式是: __________________________________________
(2)证明还原铁粉与水蒸气发生了反应的方法是_________________________________________
(3)某同学用如图所示装置进行实验,请帮助该同学完成设计,用下列简图画出未完成的实验装置示意图(铁架台可省略,导气管的形状可根据需要选择)
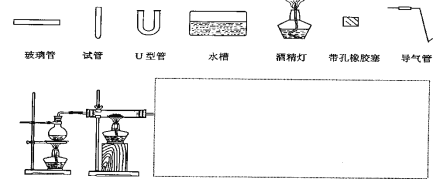 __________
__________
(4)停止反应,待装置冷却后,取出反应过的还原铁粉混合物,加入过量的稀硫酸充分反应,过滤。若混和物中既有Fe3+又有Fe2+,则证明该结论的实验方法:_________________________________________
(5)经检验上述滤液中不含Fe3+,这不能说明还原铁粉与水蒸气反应所得产物中不含+3价的Fe元素。原因是(结合离子方程式说明)___________________________________________
(6)某同学利用上述滤液制取白色的Fe(OH)2沉淀,向滤液中加入NaOH溶液后,观察至生成的白色沉淀迅速变成灰绿色,最后变成红褐色。沉淀由白色→红褐色的化学方程式是:_________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1,4-环己二醇可通过下列路线合成(某些反应的反应物和反应条件未列出):
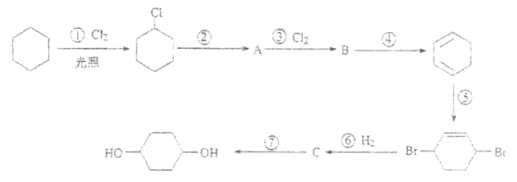
(1)写出反应④、⑦的化学方程式:
④__________________________________;
⑦__________________________________。
(2)上述七个反应中属于加成反应的有____________(填反应序号),A中所含有的官能团名称为____________。
(3)反应⑤中可能产生一定量的副产物,其可能的结构简式为_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2O2分解速率受多种因素影响。实验测得 70 ℃时不同条件下H2O2浓度随时间的变化如图所示。下列说法正确的是
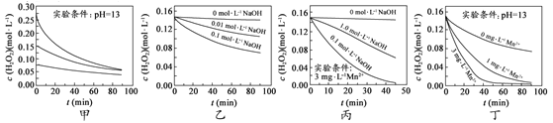
A.图甲表明,其他条件相同时,H2O2浓度越小,其分解速率越快
B.图乙表明,其他条件相同时,溶液pH越小,H2O2分解速率越快
C.图丙表明,少量Mn 2+存在时,溶液碱性越强,H2O2分解速率越快
D.图丙和图丁表明,碱性溶液中,Mn2+对H2O2分解速率的影响大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图示光合作用的部分过程,磷酸丙糖是光合作用暗反应的产物,它可在叶绿体中转化为淀粉,也可运输到细胞质基质合成蔗糖,回答下列问题:
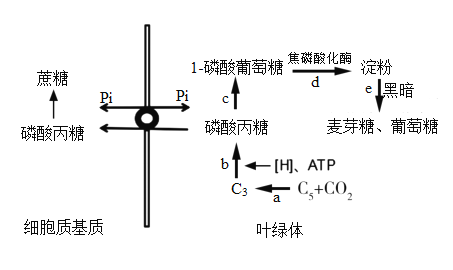
(1)图示中a过程表示三碳化合物的合成,该过程发生在叶绿体________中,光照强度下降会导致光合速率下降,原因是光反应产物减少,直接导致图示中________(填图中字母)过程反应速率下降。我国劳动人民在古代就总结出“正其行,通其风”增产措施,该措施主要目的是促进图示中_______(填图中字母)过程。
(2)在萨克斯验证叶片在光下产生淀粉的实验中,对实验材料进行24h的饥饿处理,请据图解释遮光部分为何检测不到淀粉:________________
(3)已知焦磷酸化酶催化淀粉的合成,该酶活性受叶绿体内C3和Pi调节,叶绿体在白天会形成淀粉粒,夜间淀粉粒消失,据此推断对焦磷酸化酶有活化作用的是_____________,有抑制作用的是_________。图示中,细胞质基质Pi浓度较高时磷酸丙糖与Pi交换后转移到细胞质基质,因此淀粉的合成和蔗糖的合成量成___________关系。
(4)合理施用磷肥,可增加作物产量,改善作物品质,P通常以HPO42-或H2PO4-形式被植物吸收,参与重要大分子有机物如_________的合成;也参与光合作用的过程,如___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究发现NOx和SO2是雾霾的主要成分。
I.NOx主要来源于汽车尾气,可以利用化学方法将二者转化为无毒无害的物质。
已知:N2(g)+O2(g)![]() 2NO(g) △H=+180 kJ· mol-1
2NO(g) △H=+180 kJ· mol-1
2CO(g)+O2(g)![]() 2CO2(g) △H=-564 kJ· mol-1
2CO2(g) △H=-564 kJ· mol-1
(1)2NO(g)+2CO(g) ![]() 2CO2(g)+N2(g) △H=___________,该反应在___________下能自发进行(填“高温”低温”或“任意温度”)
2CO2(g)+N2(g) △H=___________,该反应在___________下能自发进行(填“高温”低温”或“任意温度”)
(2)T℃时,将等物质的量的NO和CO充入容积为2L的密闭容器中,保持温度和体积不变,反应过程0-5min中NO的物质的量随时间变化如右图所示。

①已知:平衡时气体的分压=气体的体积分数×体系的总压强,T℃时达到平衡,此时体系的总压强为P=14MPa,则T℃时该反应的压力平衡常数Kp=___________MPa-1;平衡后,再向容器中充入NO和CO2各0.1mol,平衡将___________(填“向左”“向右”或“不")移动
②15min时,若改变外界反应条件,导致n(NO)发生如图所示的变化,则改变的条件可能是___________(填字母)
A.升温 B.增大CO浓度 C.加入催化剂 D减小容器体积
Ⅱ.SO2主要来源于煤的燃烧。燃烧烟气的脱硫减排是减少大气中含硫化合物污染的关键。
(1)已知:亚硫酸的电离常数为Ka1=2.0×10-2,Ka2=6.0×10-7。则NaSO3溶液呈___________(填“酸性”、“中性”或“碱性”)
(2)如图所示的电解装置,可将雾霾中的NO、SO2转化为硫酸铵,从而实现废气的回收再利用。通入NO的电极反应式为___________;若通入的N体积为4.48L(标况下),则另外一个电极通入SO2的质量理论上应为__________g。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com