
【题目】向二元弱酸H2Y溶液中滴加KOH溶液,所得混合溶液的pH与离子浓度变化的关系如图所示。下列有关说法正确的是
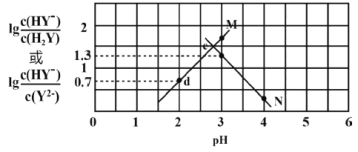
A.曲线N表示pH与![]() 的变化关系
的变化关系
B.交点e的溶液中:c(H2Y)=c(Y2-)>c(HY-)>c(H+)>c(OH-)
C.d点溶液中:c(H+)-c(OH-)=c(Y2-)+c(HY-)-c(K+)
D.Ka2(H2Y)=10-4.3
【答案】D
【解析】
H2Y溶液中滴加KOH溶液,随着pH的不断增大,先发生H2Y+OH-=HY-+H2O,后发生HY-+OH-=Y2-+H2O。
A. 按反应的先后次序,可确定曲线N表示pH与![]() 的变化关系,A不正确;
的变化关系,A不正确;
B. 交点e的溶液中,![]() =
=![]() ,由此得出c(H2Y)=c(Y2-),由反应H2Y+OH-=HY-+H2O、HY-+OH-=Y2-+H2O的顺序,可确定c(HY-)>c(H2Y)=c(Y2-)>c(H+)>c(OH-),B不正确;
,由此得出c(H2Y)=c(Y2-),由反应H2Y+OH-=HY-+H2O、HY-+OH-=Y2-+H2O的顺序,可确定c(HY-)>c(H2Y)=c(Y2-)>c(H+)>c(OH-),B不正确;
C. 依电荷守恒,d点溶液中:c(H+)-c(OH-)=2c(Y2-)+c(HY-)-c(K+),C不正确;
D. 根据图像当pH=3时![]() =1.3,H2Y的第二步电离方程式为HY-
=1.3,H2Y的第二步电离方程式为HY-![]() H++Y2-,Ka2(H2Y)=
H++Y2-,Ka2(H2Y)=![]() =
= ![]() =10-4.3,D正确;
=10-4.3,D正确;
故选D。


科目:高中化学 来源: 题型:
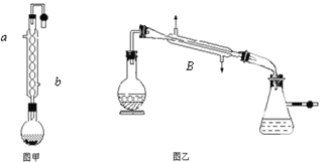
【题目】实验室合成乙酸乙酯的步骤如下:在图甲的圆底烧瓶内加入乙醇、浓硫酸和乙酸,加热回流一段时间,然后换成图乙装置进行蒸馏,得到含有乙醇、乙酸和水的乙酸乙酯粗产品。
请回答下列问题
(1)图甲中冷凝水从______(a或b)进,图乙中B装置的名称为_______;
(2)图甲在烧瓶中除了加入乙醇、浓硫酸和乙酸外,还应放入沸石,目的是_______;
(3)反应中加入过量的乙醇,目的是_______;
(4)现拟分离粗产品乙酸乙酯、乙酸和乙醇的混合物下列框图是分离操作步骤流程图:
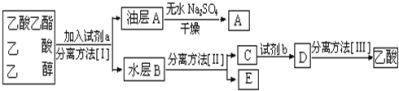
则试剂a是______,分离方法I是_______,分离方法II是_______,产物E是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设![]() 为阿伏加德罗常数的值。下列说法不正确的是
为阿伏加德罗常数的值。下列说法不正确的是![]()
![]()
A.![]() 和
和![]() 于密闭容器中充分反应后,其分子总数为
于密闭容器中充分反应后,其分子总数为![]()
B.标准状况下,![]() 某气体含有的分子数为Y,则
某气体含有的分子数为Y,则![]() 该气体的体积为
该气体的体积为![]()
C.常温下,![]() 质量分数为
质量分数为![]() 的乙炔的苯溶液中,含有碳原子的数目为
的乙炔的苯溶液中,含有碳原子的数目为![]()
D.氢氧燃料电池正极消耗![]() 气体时,负极消耗的气体分子数为
气体时,负极消耗的气体分子数为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设![]() 为阿伏加德罗常数的值,下列说法不正确的是
为阿伏加德罗常数的值,下列说法不正确的是 ![]()
![]()
A.![]() 的
的![]() 中含有的质子数与中子数均为
中含有的质子数与中子数均为![]()
B.![]() 的
的![]() 的核内中子数为N,质量数为
的核内中子数为N,质量数为![]() 的核外电子数为
的核外电子数为![]()
C.![]() 与
与![]() 混合气体中含
混合气体中含![]() 键的数目为
键的数目为![]()
D.![]() 和
和![]() 的固体混合物中含有的阳离子数为
的固体混合物中含有的阳离子数为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 表示阿伏加德罗常数,下列说法正确的是
表示阿伏加德罗常数,下列说法正确的是
A.1mol硝基![]() 与46g二氧化氮
与46g二氧化氮![]() 所含的电子数均为
所含的电子数均为![]()
B.![]() 液与
液与![]() 溶液中的
溶液中的![]() 数目相同
数目相同
C.标准状况下,![]() 三氯甲烷中含碳氯共价键的数目为
三氯甲烷中含碳氯共价键的数目为![]()
D.向FeI2溶液中通入适量![]() ,当有
,当有![]() 被氧化时,转移的电子数为
被氧化时,转移的电子数为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是
A.氨气通入醋酸溶液中 CH3COOH+NH3=CH3COONH4
B.澄清的石灰水跟盐酸反应 H++OH-=H2O
C.碳酸钡溶于醋酸 BaCO3+2H+=Ba2++H2O+CO2↑
D.金属钠跟水反应 2Na+H2O=2Na++2OH-+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若NA表示阿伏加德罗常数,下列叙述中正确的是 ( )
A.标准状况下,22.4L SO3含NA个分子
B.含0.4mol HCl的浓盐酸与足量二氧化锰反应转移电子数为0.2NA
C.32gCu与足量硫完全反应,转移的电子数为0.5NA
D.在200mL 5mol·L-1 AlCl3溶液中,Al3+数目为NA,等于Cl-数目的1/3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应2A(g)+2B(g)![]() C(g)+2D(g),在容器均为2L的甲,乙,丙三个恒温(反应温度分别为300℃,T℃,300℃)容器中分别加入物质的量之比为1:1的A和B,测得各容器中n(B)随反应时间t的变化情况如下表所示:
C(g)+2D(g),在容器均为2L的甲,乙,丙三个恒温(反应温度分别为300℃,T℃,300℃)容器中分别加入物质的量之比为1:1的A和B,测得各容器中n(B)随反应时间t的变化情况如下表所示:
0 | 40 | 80 | 120 | 160 | |
甲 | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
乙 | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
丙 | 1.00 | 0.80 | 0.65 | 0.53 | 0.45 |
根据表中数据,下列说法正确的是
A.乙容器中的反应温度T<300
B.丙容器中,0-40min内用A的浓度变化表示的平均反应速率为为0.05mol/(L·min)
C.若起始时向甲容器中加入0.2、0.2、0.4和1.2,则反应将向正反应方向进行
D.在0-40min内,提高乙容器中的A的转化率的有效途径是使用高效催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向10mL0.1mol/L的某一元酸HR溶液中逐滴加入0.1mol/L氨水,所得溶液pH及导电能力变化如图。下列分析不正确的是( )

A. a~b点导电能力增强说明HR为弱酸
B. a、b点所示溶液中水的电离程度不相同
C. b恰好完全中和,pH=7说明NH4R没有水解
D. c 点溶液存在c(NH4+)>c(R-)、c(OH-)>c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com