
A、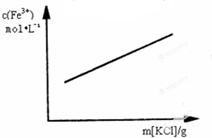 FeCl3+3KSCN?Fe(SCN)3+KCl(忽略液体体积变化) | ||
B、 2NO+O2?2NO2△H<0 | ||
C、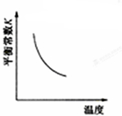 NO(g)+CO(g)?
| ||
D、 A2(g)+3B2(g)?2AB3(g)△H=-373.4KJ?mol-1 |


 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②④ | B、②③ | C、①④ | D、①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钠在水层中反应并四处游动 |
| B、钠停留在苯层中不发生反应 |
| C、钠在苯的液面上反应并四处游动 |
| D、钠在苯与水的界面处反应并可能做上、下跳动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、C(Cl-)>C(NH4+)>C(H+)>C(OH-) |
| B、C(NH4+)>C(Cl-)>C(H+)>C(OH-) |
| C、C(NH4+)>C(Cl-)>C(OH-)>C(H+) |
| D、C(Cl-)>C(NH4+)>C(OH-)>C(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、原子化热:Y>Z |
| B、WX3和水反应形成的化合物是离子化合物 |
| C、气态氢化物的热稳定性:R<W |
| D、Y和Z两者最高价氧化物的晶格能Z>Y |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、③④ | B、③④⑤ |
| C、①②③④ | D、①③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、化学键都具有饱和性和方向性 |
| B、晶体中只要有阴离子,就一定有阳离子 |
| C、氢键具有方向性和饱和性,也属于一种化学键 |
| D、金属键由于无法描述其键长、键角,故不属于化学键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com