
【题目】苹果汁是人们喜爱的饮料,由于此饮料中含有Fe2+,现榨的苹果汁在空气中会由浅绿色变为棕黄色。若榨汁时加入维生素C,可有效防止这种现象发生。这说明谁生素C具有
A.氧化性 B.还原性 C.碱性 D.酸性
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:
【题目】某实验小组用0.50 mol·L-1 NaOH溶液和0.50 mol·L-1硫酸溶液进行中和热的测定。
Ⅰ.配制0.50 mol·L-1 NaOH溶液
(1)若实验中大约要使用245 mL NaOH溶液,至少需要称量NaOH固体 g。
(2)从下图中选择称量NaOH固体所需要的仪器是 (填字母): 。
名称 | 托盘天平 (带砝码) | 小烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
仪器 |
|
|
|
|
|
|
序号 | a | b | c | d | e | f |
Ⅱ.测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示。

(4)取50 mL NaOH溶液和30 mL硫酸溶液进行实验,实验数据如表。
温度 实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | 温度差 平均值 (t2-t1)/℃ | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 29.6 | |
2 | 27.0 | 27.4 | 27.2 | 31.2 | |
3 | 25.9 | 25.9 | 25.9 | 29.8 | |
4 | 26.4 | 26.2 | 26.3 | 30.4 | |
上表中的温度差平均值为 ℃
近似认为0.50 mol·L-1 NaOH溶液和0.50 mol·L-1硫酸溶液的密度都是1 g·cm-3,中和后生成溶液的比热容c=4.18 J·(g·℃)-1。则中和热ΔH= (取小数点后一位)。
③ 上述实验数值结果与57.3 kJ·mol-1有偏差,产生偏差的原因可能是(填字母) 。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向某恒容密闭容器中充入一定量CO2和H2,发生反应:CO2(g)+H2(g)![]() HCOOH(g) 测得平衡体系中CO2的百分含量(CO2%)与反应温度变化的关系如图所示。下列物理量中,a点大于b点的是①正反应速率②逆反应速率③HCOOH(g)的浓度④对应温度时的平衡常数( )
HCOOH(g) 测得平衡体系中CO2的百分含量(CO2%)与反应温度变化的关系如图所示。下列物理量中,a点大于b点的是①正反应速率②逆反应速率③HCOOH(g)的浓度④对应温度时的平衡常数( )

A、①② B、①③
C、②④ D、③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题:
(1)将28.5 g氯化镁溶于水配成的500 mL溶液中Cl-浓度是____________,写出氯化镁的电离方程式_________________。
(2)已知m mol某气体的质量为ag,则bg该气体在标准状况下的体积为____________L。
(3)某A12(SO4)3溶液VmL中含有Al3+ ag,取出![]() mL溶液稀释成V mL后,SO42-的物质的量浓度为 ______(用含a、V的代数式表示,化简到最简整数比)。
mL溶液稀释成V mL后,SO42-的物质的量浓度为 ______(用含a、V的代数式表示,化简到最简整数比)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯(ClO2)是一种高效环保的自来水消毒剂,其中氯和氧的化合价分别为( )
A. +2、-2 B. +4、-2 C. -2、-1 D. -4、+2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增加,m、p、r是由这些元素组成的二元化合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,0.01 mol/Lr溶液的pH为2,s通常是难溶于水的混合物。上述物质的转化关系如图所示。下列说法正确的是( )
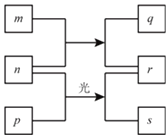
A. 原子半径的大小W<X<Y
B. 元素的非金属性Z>X>Y
C. Y的氢化物常温常压下为液态
D. X的最高价氧化物的水化物为强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定能在下列溶液中大量共存的离子组是( )
A. 含有大量Mg2+的溶液:Na+、NH4+、SO![]() -、Cl-
-、Cl-
B. 碱性溶液:Na+、Ca2+、SO![]() -、CO
-、CO![]() -
-
C. 含有大量Fe3+的溶液:Na+、Mg2+、NO![]() 、SCN-
、SCN-
D. 含有大量NO![]() 的溶液:H+、Fe2+、SO
的溶液:H+、Fe2+、SO![]() -、Cl-
-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】浓度均为0.10mol·L-1、体积均为V0的MOH与ROH溶液,分别加水稀释至体积V,pH随lg(V/ V0)的变化如图所示,下列叙述错误的是( )
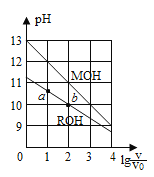
A.MOH的碱性强于ROH的碱性
B.ROH的电离程度:b点大于a点
C.若两溶液无限稀释,则它们的c(OH-)相等
D.当lg(V/ V0))=2时,若两溶液同时升高温度,则c(M+)/c(R+)增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.实验室可以用二氧化锰和浓盐酸反应制取氯气,方程式如下:MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O,下图是某学生设计的试验室制备干燥Cl2的实验装置图,根据图中的装置和有关试剂回答下列问题:
MnCl2+Cl2↑+2H2O,下图是某学生设计的试验室制备干燥Cl2的实验装置图,根据图中的装置和有关试剂回答下列问题:
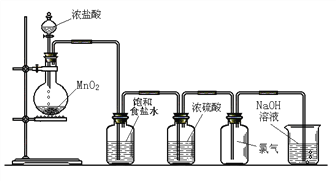
(1)该实验中还缺少一种仪器,这种仪器是_____________;
(2)饱和食盐水的作用是____________________;
(3)氯气与冷的氢氧化钠溶液反应生成NaCl、NaClO和H2O,与热的氢氧化钠溶液按照下面的反应进行:____________________
Cl2+ NaOH(热) - NaCl+ NaClO3+ H2O,请配平上述反应方程式;
(4)8.7 g MnO2和足量的浓盐酸反应,其中被氧化的HCl的物质的量为_________mol。
Ⅱ.某同学为探究铜跟浓硫酸的反应情况,用如图所示装置进行了有关实验。
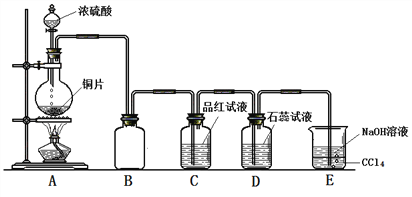
(1)B是用来收集实验中生成的气体的装置,但未将导管画全,请把导管补充完整_____________;
(2)D中的现象是_____________________;
(3)E中NaOH溶液的作用是_________________;
(4)下列药品中能够用来验证反应停止后的烧瓶中有H2SO4剩余的是__________(填字母编号)。
a.BaCl2溶液 b.NaHCO3粉末 c.Ba(NO3)2溶液 d.银粉
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com