
【题目】水煤气变换反应的能量变化如图。下列叙述错误的是
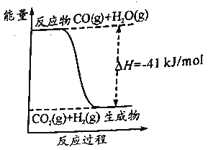
A.反应为:CO(g)+H2O(g)=CO2(g)+H2(g)B.反应物总能量高于生成物总能量
C.H2的燃烧热为41 kJ·mol-1D.使用催化剂可以降低反应所需活化能
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:
【题目】按要求回答下列问题。
(1)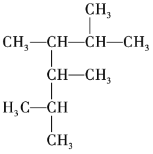 的名称为______。
的名称为______。
(2) 的名称为______。
的名称为______。
(3)3-甲基-2-戊烯的结构简式为______。
(4)1,3,5-三甲基苯的结构简式为______。
(5)某烷烃的相对分子质量为72,其一氯代物只有一种,该烷烃的结构简式为______。
(6)2,3-二甲基-2-丁烯的键线式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用Pt-g-C3N4光催化氧化法脱除NO的过程如图所示。该脱除过程中,下列说法不正确的是

A.该脱除过程中太阳能转化为化学能。
B.在Pt端发生的是氧化反应
C.过程①发生的反应为H2O2 - 2e-=O2↑+ 2H+
D.过程③的化学方程式2NO2 + H2O2= 2HNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究小组进行右图所示实验,试剂A为0.2mol/LCuSO4溶液,发现铝条表面无明显变化,于是改变实验条件,探究铝和CuSO4溶液、CuCl2溶液反应的影响因素。用不同的试剂A进行实验1~实验4,并记录实验现象:
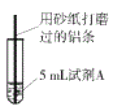
实验序号 | 试剂A | 实验现象 |
1 | 0.2mol/LCuCl2溶液 | 铝条表面有气泡产生,并有红色固体析出 |
2 | 0.2mol/LCuSO4溶液,再加入一定质量的NaCl固体 | 开始铝条表面无明显变化,加NaCl后,铝条表面有气泡产生,并有红色固体析出 |
3 | 2mol/LCuSO4溶液 | 铝条表面有少量气泡产生,并有少量红色固体 |
4 | 2mol/LCuCl2溶液 | 反应非常剧烈,有大量气泡产生,溶液变成棕褐色,有红色固体和白色固体生成 |
(1)实验1中,铝条表面析出红色固体的反应的离子方程式为_________。
(2)实验2的目的是证明铜盐中的阴离子Cl-是导致实验1中反应迅速发生的原因,实验2中加入NaCl固体的质量为______g。
(3)实验3的目的是_________ 。
(4)经检验可知,实验4中白色固体为CuCl。甲同学认为产生白色固体的原因可能是发生了Cu+CuCl2=2CuCl的反应,他设计了右图所示实验证明该反应能够发生。
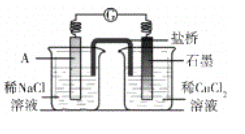
①A极的电极材料是_________。
②能证明该反应发生的实验现象是_________ 。
(5)为探究实验4中溶液呈现棕褐色的原因,分别取白色CuCl固体进行以下实验:
实验序号 | 实验操作 | 实验现象 |
i | 加入浓NaCl溶液 | 沉淀溶解,形成无色溶液 |
ii | 加入饱和AlCl3溶液 | 沉淀溶解,形成褐色溶液 |
iii | 向i所得溶液中加入2mol/LCuCl2溶液 | 溶液由无色变为褐色 |
查阅资料知:CuCl难溶于水,能溶解在Cl-浓度较大的溶液中,生成[CuCl2]
①由述球实验及资料可推断,实验4中溶液呈棕褐色的原因可能是[CuCl2]-与_____作用的结果。
②为确证实验4所得的棕褐色溶液中含有[CuCl2]-,应补充的实验是_______。
(6)上述实验说明,铝和CuSO4溶液、CuCl2溶液的反应现象与______有关。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列各组物质:
①O2和O3 ②CH2=CH-CH3和CH2=CH-CH=CH2 ③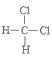 和
和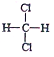
④11H2O和21H2O ⑤CH3CH2CH3和CH3C(CH3)3 ⑥23592A和质量数为238中子数为146的原子⑦C2H5C≡CCH3和CH3CH=CHCH=CH2
按要求用序号填空
(1)属于同系物的是_______。
(2)属于同分异构体的是________。
(3)属于同位素的是_______。
(4)属于同素异形体的是________。
(5)属于同种物质的是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】花椒毒素(H)有抗实验性心律失常、镇痛、抗炎等作用。由芳香族化合物A为原料合成H的一种合成路线如下:
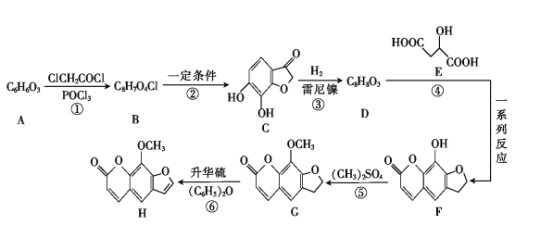
已知:![]() +ClCH2CH2Cl
+ClCH2CH2Cl![]()
![]() +HCl
+HCl
回答下列问题:
(1)A的化学名称是 _____(用系统命名法)。
(2)G中所含官能团的名称是 ____。
(3)碳原子上连有4个不同的原子或基团时,该碳称为手性碳。E中___ (填“有”或“没有”)手性碳。
(4)反应⑥的反应类型是 ____ 。
(5)D的结构简式为 _____。
(6)F与足量NaOH溶液反应的化学方程式为 ____。
(7)芳香族化合物W是D的同分异构体,能发生银镜反应和水解反应,遇FeCl3溶液发生显色反应;W的核磁共振氢谱有5组峰,且面积比为1∶2∶2∶2∶1。符合上述要求的W有____种。
(8)有机物M(![]() )是一种重要的化工原料。设计由邻苯二酚和氯乙酰氯(ClCH2COCl)为起始原料制备有机物M的合成路线____。(无机试剂及有机溶剂任用)
)是一种重要的化工原料。设计由邻苯二酚和氯乙酰氯(ClCH2COCl)为起始原料制备有机物M的合成路线____。(无机试剂及有机溶剂任用)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,其中A、C、D、E为短周期元素,最外层电子数之和为23,下列说法正确的是

A.元素A的氢化物,在同族元素中沸点最低
B.元素B的金属性比E弱
C.A、C、D均可形成18e-分子
D.与金属钠的反应中,1mol C原子和1 mol E原子得电子数目一定相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应2SO2(g)+O2(g)![]() 2SO3(g)是硫酸工业的最重要反应,因该反应中使用催化剂而被命名为接触法制硫酸。
2SO3(g)是硫酸工业的最重要反应,因该反应中使用催化剂而被命名为接触法制硫酸。
(1)使用V2O5催化该反应时,涉及到催化剂V2O5的热化学反应有:
①V2O5(s)+SO2(g)![]() V2O4(s)+SO3(g) △H1=+59.6kJ·mol-1
V2O4(s)+SO3(g) △H1=+59.6kJ·mol-1
②2V2O4(s)+O2(g)![]() 2V2O5(s) △H2=-315.4kJ·mol-1
2V2O5(s) △H2=-315.4kJ·mol-1
则2SO2(g)+O2(g)![]() 2SO3(g) △H3=__________kJ·mol-1
2SO3(g) △H3=__________kJ·mol-1
(2)向10 L密闭容器中加入V2O4(s)、SO2(g)各1 mol及一定量的O2,改变加入O2的量,在常温下反应一段时间后,测得容器中V2O4、V2O5、SO2和SO3的量随反应前加入O2的变化如图甲所示,图中没有生成SO3的可能原因是_________________________
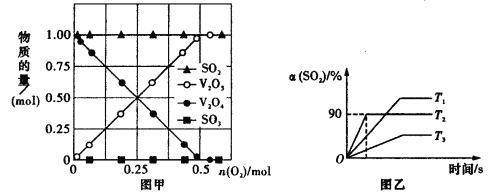
(3)在原10 L的恒容装置中,加入V2O5(s)、SO2(g)各0.6 mol,O2(g)0.3 mol,分别在T1、T2、T3时进行反应,测得容器中SO2的转化率如图乙所示。
①T2时,2SO2(g)+O2(g)![]() 2SO3(g)的平衡常数K=__________。
2SO3(g)的平衡常数K=__________。
②结合化学方程式及相关文字,解释反应为什么在T3条件下比T2条件下的速率慢:_____
(4)在温度T2使用V2O5进行反应:2SO2(g)+O2(g)![]() 2SO3(g),在保证O2(g)的浓度不变的条件下,增大容器的体积,平衡__________(填字母代号)。
2SO3(g),在保证O2(g)的浓度不变的条件下,增大容器的体积,平衡__________(填字母代号)。
A.向正反应方向移动 B.向逆反应方向移动
C.不移动 D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镇痛药物J的合成方法如下:
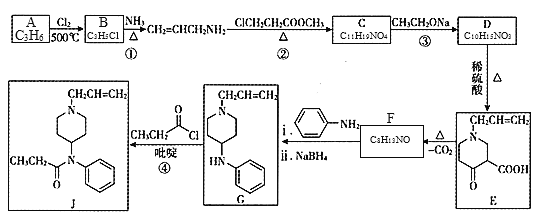
已知:
![]() +Cl-R3
+Cl-R3![]()
![]() +HCl
+HCl
R1COOR2+R3CH2COOR4![]()
![]() +R2OH
+R2OH
![]()
![]()
![]()
(R1、R2、R3、R4为氢或烃基)
(1)B的名称为______;F的结构简式为______。
(2)C中含氧官能团名称为______;②的反应类型为______反应。
(3)③的化学方程式为______。
(4)有机物K分子组成比F少两个氢原子,符合下列要求的K的同分异构体有______种。
A.遇FeCl3显紫色 B.苯环上有三个取代基
(5)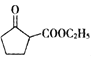 是一种重要的化工中间体。以环已醇(
是一种重要的化工中间体。以环已醇(![]() )和乙醇为起始原料,结合己知信息选择必要的无机试剂,写出
)和乙醇为起始原料,结合己知信息选择必要的无机试剂,写出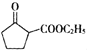 的合成路线______。(已知:RHC=CHR
的合成路线______。(已知:RHC=CHR![]() RCOOH+R′COOH,R、R′为烃基。用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)
RCOOH+R′COOH,R、R′为烃基。用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com