
【题目】按要求回答下列问题。
(1)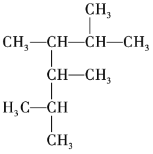 的名称为______。
的名称为______。
(2) 的名称为______。
的名称为______。
(3)3-甲基-2-戊烯的结构简式为______。
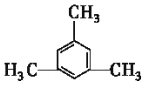
(4)1,3,5-三甲基苯的结构简式为______。
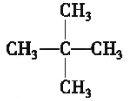
(5)某烷烃的相对分子质量为72,其一氯代物只有一种,该烷烃的结构简式为______。
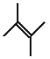
(6)2,3-二甲基-2-丁烯的键线式为______。
【答案】2,3,4,5-四甲基己烷 2-甲基-1-丁烯 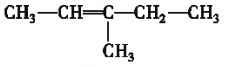
【解析】
(1)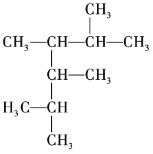 属于烷烃,最长碳链上含有6个碳原子,2、3、4、5的碳原子上含有甲基;
属于烷烃,最长碳链上含有6个碳原子,2、3、4、5的碳原子上含有甲基;
(2)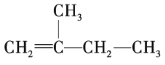 属于烯烃,分子中含有碳碳双键的最长碳链含有4个碳原子,编号从距离碳碳双键最近的一端开始,在1、2号碳原子上有碳碳双键,2号碳原子上连有1个甲基;
属于烯烃,分子中含有碳碳双键的最长碳链含有4个碳原子,编号从距离碳碳双键最近的一端开始,在1、2号碳原子上有碳碳双键,2号碳原子上连有1个甲基;
(3)3-甲基-2-戊烯属于烯烃,结构简式为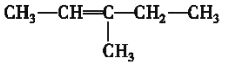 ;
;
(4)1,3,5-三甲基苯属于苯的同系物,结构简式为 ;
;
(5)烷烃的通式为CnH(2n+2),若烷烃的相对分子质量为72,则有14n+2=72,解得n=5,该烷烃分子式为C5H12,C5H12有三种同分异构体;
(6)2,3-二甲基-2-丁烯属于烯烃,结构简式为CH3(CH3)CH=CH(CH3)CH3。
(1) 属于烷烃,最长碳链上含有6个碳原子,2、3、4、5的碳原子上含有甲基,则名称为2,3,4,5-四甲基己烷,故答案为:2,3,4,5-四甲基己烷;
属于烷烃,最长碳链上含有6个碳原子,2、3、4、5的碳原子上含有甲基,则名称为2,3,4,5-四甲基己烷,故答案为:2,3,4,5-四甲基己烷;
(2)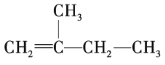 属于烯烃,分子中含有碳碳双键的最长碳链含有4个碳原子,编号从距离碳碳双键最近的一端开始,在1、2号碳原子上有碳碳双键,2号碳原子上连有1个甲基,名称为2-甲基-1-丁烯,故答案为:2-甲基-1-丁烯;
属于烯烃,分子中含有碳碳双键的最长碳链含有4个碳原子,编号从距离碳碳双键最近的一端开始,在1、2号碳原子上有碳碳双键,2号碳原子上连有1个甲基,名称为2-甲基-1-丁烯,故答案为:2-甲基-1-丁烯;
(3)3-甲基-2-戊烯属于烯烃,结构简式为 ,故答案为:
,故答案为: ;
;
(4)1,3,5-三甲基苯属于苯的同系物,结构简式为 ,故答案为:
,故答案为: ;
;
(5)烷烃的通式为CnH(2n+2),若烷烃的相对分子质量为72,则有14n+2=72,解得n=5,该烷烃分子式为C5H12,C5H12有三种同分异构体,一氯代物只有一种的结构简式为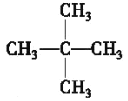 ,故答案为:
,故答案为: ;
;
(6)2,3-二甲基-2-丁烯属于烯烃,结构简式为CH3(CH3)CH=CH(CH3)CH3,则键线式为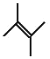 ,故答案为:
,故答案为: 。
。


 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案科目:高中化学 来源: 题型:
【题目】焦亚硫酸钠(Na2S2O5)可作为贮存水果的保鲜剂。现欲制备焦亚硫酸钠并探究其部分化学性质。
Ⅰ.制备Na2S2O5
可用试剂:饱和Na2SO3溶液、浓NaOH溶液、浓H2SO4、苯、Na2SO3固体(试剂不重复使用)。
焦亚硫酸钠的析出原理:2NaHSO3(饱和溶液)=Na2S2O5(晶体)+H2O(l)
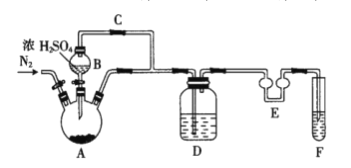
(1)如图装置中仪器A的名称是___。A中发生反应的化学方程式为___。仪器E的作用是___。
(2)F中盛装的试剂是___。
Ⅱ.探究Na2S2O5的还原性
(3)取少量Na2S2O5晶体于试管中,滴加1mL2mol/L酸性KMnO4溶液,剧烈反应,溶液紫红色很快褪去。反应的离子方程式为___。食品级焦亚硫酸钠可作为贮存水果保鲜剂的化学原理是防止食品___。
Ⅲ.测定Na2S2O5样品的纯度。
(4)将10.0gNa2S2O5样品溶解在蒸馏水中配制100mL溶液,取其中10.00mL加入过量的20.00mL0.3000mol/L的酸性高锰酸钾溶液,充分反应后,用0.2500mol/L的Na2SO3标准液滴定至终点,消耗Na2SO3溶液20.00mL,Na2S2O5样品的纯度为___%(保留一位小数),若在滴定终点时,俯视读数Na2SO3标准液的体积,会导致Na2S2O5样品的纯度___。(填“偏高”、“偏低”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学学习小组利用如图装置来制取乙酸乙酯。
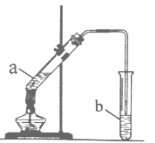
I.实验过程:向试管a中加入碎瓷片,3mL乙醇,然后边振荡试管边慢慢加入2mL浓硫酸,最后加入2mL乙酸,按图连接好装置,用酒精灯缓慢加热,将产生的蒸汽经导管通到b试管中的液面上。
II. 已知化学方程式:CH3COOH+CH3CH2OH ![]() CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
III.查阅资料得知:乙酸乙酯不溶于水,密度比水小,且有香味
请回答下列问题:
(1)试管a中加入碎瓷片,其作用是_____(填字母代号)。
A.加快化学反应速率 B.防止溶液暴沸
(2)试管b中的溶液是_____(填字母代号)。
A饱和碳酸钠溶液 B.饱和氢氧化钠溶液
(3)实验完毕后,将b试管中的液体充分振荡,静置后,溶液分为两层。
①乙酸乙酯在________(填“上层”或“下层”)。
②常用________操作将两层液体分离(填“过滤”或“分液”)。
(4)实验中加入乙酸的质量为2.1g,其中60%的乙酸发生酯化反应,则得到乙酸乙酯的质量为______g(计算结果保留两位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法中,错误的是( )
A.NH4H是一种离子晶体,其中氢离子的核外电子排布与氦原子相同
B.在石墨晶体中,碳原子与共价键的个数比为2:3
C.三种氢化物的沸点高低:HBr>HCl>HF
D.甲基的电子式为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,有关物质的电离平衡常数如下:
化学式 | CH3COOH | H2CO3 | H2SO3 |
电离平衡常数K | K=1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=1.5×10-2 K2=1.02×10-7 |
(1)电解质由强至弱顺序为_________________(用化学式表示,下同)。
(2)常温下,0.02 mol·L-1的CH3COOH溶液的电离度约为 ,体积为10mLpH=2的醋酸溶液与亚硫酸溶液分别加蒸馏水稀释至1000mL,稀释后溶液的pH,前者 后者(填“>”、“<”或“=”)。
(3)下列离子CH3COO-、CO32-、HSO3-、SO32-在溶液中结合H+的能力由大到小的顺序为_____________。
(4)NaHSO3溶液显酸性的原因___________________________(离子方程式配适当文字叙述),其溶液中离子浓度由大到小的关系是_______________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,甲池的总反应式为:N2H4+O2=N2+H2O,下列关于该电池工作时的说法正确的是( )

A. 该装置工作时,Ag电极上有气体生成
B. 甲池中负极反应为N2H4-4e-=N2+4H+
C. 甲池和乙池中的溶液的pH均减小
D. 当甲池中消耗0.1molN2H4时,乙池中理论上最多产生6.4g固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解质溶液是中学化学中的非常重要的知识点,请根据要求填空。
(1)向NaHSO3溶液滴加石蕊溶液后变红,则HSO3-的电离程度___其水解程度(填“>”或“=”或“<”)。该物质能___(填“促进”或“抑制”)水的电离。
(2)酸碱中和滴定时,不宜用___(填“酚酞”“石蕊”或“甲基橙” )用作指示剂。用标准的NaOH滴定未知浓度的盐酸,选用酚酞为指示剂,造成测定结果偏高的原因可能是___(填字母)。
A.未用标准液润洗碱式滴定管
B.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
C.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
D.滴定终点读数时,俯视滴定管的刻度,其它操作均正确
(3)醋酸(CH3COOH)是一种弱电解质,25℃时,醋酸的电离平衡常数表达式Ka=___。
①将等体积等物质的量浓度的醋酸和氢氧化钠溶液混合后,溶液呈___(填“酸性”,“中性”或“碱性”,下同),溶液中c(Na+)___c(CH3COO-)(填“>”或“=”或“<”)。
②pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈___。若物质的量浓度相同的醋酸和氢氧化钠溶液混合后,溶液中c(Na+)=c(CH3COO-),则混合后溶液呈___。
(4)现有a.醋酸、b.盐酸、c.硫酸三种溶液,根据要求答题。
①若它们物质的量浓度相等,它们的pH由大到小的关系为___(用abc表示,下同)。
②若它们的pH相等,它们物质的量浓度由大到小的关系为___。
③若它们的pH相等,均加水稀释100倍后,其pH由大到小的关系为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过对实验现象的观察、分析推理得出正确的结论是化学学习的方法之一。对下列实验事实的解释正确的是
现象 | 解释 | |
A | 用洁净的铂丝蘸取某溶液进行焰色反应,火焰呈黄色 | 该溶液中一定含有 |
B |
|
|
C | 某溶液中先加入稀盐酸无现象,再加入氯化钡溶液,有白色沉淀生成 | 该溶液中一定含有 |
D | 铁加入稀硝酸中有气泡产生 | 铁与稀硝酸发生了置换反应 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物J是一种防止血管中血栓形成与发展的药物,其合成路线如图所示 (部分反应条件略去)。
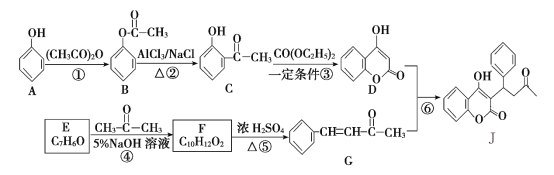
回答下列问题:
(1)反应①的反应类型是________,反应⑥的反应类型是________。
(2)J的分子式是________。F的结构简式是________。
(3)反应③的化学方程式为___________________________________。
(4)写出同时满足下列条件的F的所有同分异构体的结构简式________。
①苯环上只有两个处于对位的取代基;
②1 mol该有机物能与含2 mol NaOH的溶液恰好完全反应。
(5)参照J的合成路线,设计一种以![]() 为原料制备
为原料制备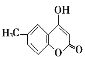 的合成路线________。
的合成路线________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com