
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | 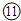 | 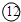 |
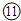 为Ca,
为Ca,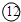 为Br,
为Br,
| ||
| 冰晶石 |
| ||
| ||
| 冰晶石 |
| ||


科目:高中化学 来源:不详 题型:问答题
| 族 周期 | IA | 0 | ||||||
| l | ① | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.第ⅤA族元素都是非金属元素 |
| B.磷比氮难以与氢化合生成气态氢化物 |
| C.气态氢化物的稳定性:PH3>NH3>H2O |
| D.酸性:HNO3>H3PO4>H2SO4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①② | B.③④ | C.①④ | D.②③ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.根据元素周期律,由HClO4可类推出氟元素也存在最高价氧化物的水化物HFO4 |
| B.在元素周期表的金属和非金属分界线附近寻找半导体材料 |
| C.元素周期表有7个周期,8个主族 |
| D.ⅠA族的元素全部是金属元素 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.从上到下原子半径逐渐减小 |
| B.易形成-1价离子 |
| C.最高价氧化物的水化物显酸性 |
| D.从上到下氢化物的稳定性依次减弱 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题



查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com