
����Ŀ����������ȡ���������ͼ����֪���з�����Ӧ�Ļ�ѧ����ʽΪ��Cl2+2KI===2KCl+I2����ش��������⣺
(1)ָ����ȡ��Ĺ������й�ʵ����������������ƣ�__________��________��
(2)��3 mL��ˮ�У�����1 mL���Ȼ�̼�������ú۲쵽�Թ���ķֲ���������ͼ�е�________(ע���Թ�����ɫ��Ϊ�Ϻ�ɫ��Һ)��

(3)�Ӻ�����л���Һ����ȡ��ͻ����л��ܼ������辭������ָ������ͼʵ��װ���еĴ���֮����(����װ�����ձ��ײ��ѵ���ʯ����)

��________________________________��
��________________________________��
���𰸡�(1)���� ��ȡ����Һ
(2)D
(3)���¶ȼ��¶˵�ˮ�����ܲ�����Һ�У�Ӧλ��֧�ܿ�
��������(��������)��ˮ��������
��������(1)������ҵ�����Һ����ɲ�������Һ��ͨ�����˵�ʵ�������ʵ�ֵģ������ˮ��Һת���ɺ�����л���Һ����Ҫ����ȡ�ٷ�Һ����ɡ�
(2)���Ȼ�̼���ܶȴ���ˮ���ֲ��λ���²㣬��ϵ�ˮ��CCl4������ֱ�Ϊ3 mL��1 mL�����ж�D��ȷ��
(3)������Ļ���ʵ��װ��ͼ��ԭ����֪���¶ȼ��¶˵�ˮ����Ӧλ��������ƿ��֧�ܿڴ�����������ˮ������ӦΪ�½��ϳ���


 �����Ƹ���ʦ����ϵ�д�
�����Ƹ���ʦ����ϵ�д� ��ͨ����ͬ����ϰ��ϵ�д�
��ͨ����ͬ����ϰ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��25��ʱ�����볣��Kb(NH3��H2O)=1.8��l0-5��CH3COOH�ĵ��볣��������ȡ�����1 L 0.1 molL-1��ˮ�м���������0.1 molL-1CH3COOH��Һ��������˵����ȷ����
A. �ڵμӹ����У�Kwʼ�ձ��ֲ���
B. 25��ʱ����Ӧ����Һ�� c(NH4+)>c(CH3COO-)
C. ���ð�ˮ����Һ�ζ����ᣬ��Ӧѡ���̪��Ϊָʾ��
D. 25��ʱ����ӦNH4++H2O![]() NH3H2O+H+��ƽ�ⳣ��ԼΪ 5.6 ��10-10
NH3H2O+H+��ƽ�ⳣ��ԼΪ 5.6 ��10-10
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ӳ�ʳƷ�����ڵķ����У���ԭ��������������ͬ����
A. ��ʳ������ B. ����� C. �䵪�� D. ʹ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
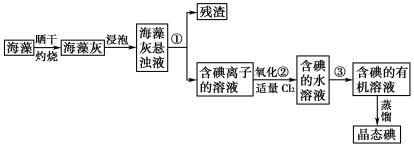
����Ŀ��ʵ��������Ҫ������NaCl��Һ�����ֱ�ֻ�л���Na2SO4��NH4HCO3��NaCl��ijѧ���������ͼ��ʾ������ȡ������NaCl��Һ��(��֪��NH4HCO3![]() NH3��+CO2��+H2O)
NH3��+CO2��+H2O)

����˷�����ȷ����ô��
(1)���в�������ѡ������������______________��
(2)������Ϊʲô�������ᱵ��Һ����������_____________________________��
(3)���в�����������ж�![]() �ѳ�����������_________________________��
�ѳ�����������_________________________��
(4)��������Ŀ����________________��Ϊʲô���ȹ��˺��̼������Һ��������____________��
(5)��������Ŀ����________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵���������
A. �����д����ƹ�ʹ��һ�������ϴ���ֽ��
B. �ÿ����Ե����κ����δ���ˮ�е�������
C. ά����C���л�ԭ�ԣ�������ʳƷ��������
D. ��SO2�����ں���п�����ɱ���Ϳ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڢ�A���⻯����۷е�Ƚ��У�ˮ��ߵ�ԭ����
A. ˮ���Ӽ������ B. ˮ�����ڵĹ��۽����ȶ�
C. ˮ���Ӽ�ķ��»������ D. ��Ԫ�صķǽ�������ǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ԡ����ʵ�����Ϊ���ĵļ����ǻ�ѧ����Ļ����������롰���ʵ�������صļ�����ȷ����
A������CO��CO2��O3�������壬���Ƿֱ���1 mol O����������������ʵ���֮��Ϊ3��2��1
B��n g Cl2����m��Clԭ�ӣ����ӵ�����NA����ֵ�ɱ�ʾΪ![]()
C����״���£�11.2 L X������ӵ�����Ϊ16 g����X�����Ħ��������32
D��5.6 g CO��22.4 L CO2�к��е�̼ԭ����һ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����÷Ͼ�п��Ƥ�Ʊ�����Fe3O4�������Ӽ�������ZnO��һ���Ʊ�����ͼ���£�

��֪��Ksp[Zn(OH)2]= 1.2��10��17��Zn(OH)2��������ǿ�ᣬ��������ǿ��������ڰ�ˮ������[Zn��NH3)4]2����
��1����ҺA�м�ϡH2SO4����Zn(OH)2�����ӷ���ʽΪ_________��
��2�������£�Zn(OH)2������Һ��c(Zn2��)=3��10��6mol/L������ҺA�м���ϡH2SO4���������ܽ������Zn(OH)2��Zn(OH)2��ʼ�ܽ��pHΪ_________��Ϊ��ֹZn(OH)2�ܽ⣬�ɽ�ϡH2SO4��Ϊ_________����lg2=0.3��
��3���������������Σ�NaClO3����ԭΪCl������ԭ������������Ӧ�����ʵ���֮����_________��
��4��������ҺB�Ƶ�Fe3O4�������ӵĹ�����ͨ��N2��ԭ����_________��
��Fe3O4�������ӵ�ֱ���ķ�Χ��_________��
��ȷ����ҺB�к���Fe2�����Լ���_________��
��5���Խ�����ʵ���Ҳ������ÿ�����п���백ˮ��Ӧ�Ʊ�������п��ԭ��_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����칬һ�š��Ĺ���ϵͳ������������ȼ�ϵ�أ�RFC����RFC��һ�ֽ�̫���ܵ�ص��ˮ����������ȼ�ϵ�ؼ������ϵĿɳ���ء���ͼΪRFC����ԭ��ʾ��ͼ����ĤΪ����ѡ������Ĥ��������˵������ȷ����
![]()

װ��I װ��II
A. c���Ϸ����ĵ缫��Ӧ�ǣ�O2 + 4H+ + 4e- = 2H2O
B. ����0.1mol����ת��ʱ��b������1.12L ����Y����״���£�
C. װ��I��װ��II�ĵ������Һ�У��������˶������෴
D. RFCϵͳ����������ֻ����3����ʽ������ת��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com