
【题目】根据下面的反应路线及所给信息回答问题
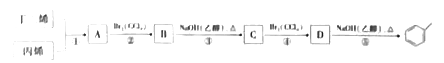
已知:![]()
(1)A中含有的官能团名称是______,A的名称是_____。
(2)不考虑顺反异构,丙烯的二氯代物有____种。
(3)反应类型:①是_________;⑤是_______________。
(4)反应③的化学方程式是_______________。
【答案】 碳碳双键 4-甲基-1-环已烯(或4-甲基环已烯) 5 加成反成 消去反应 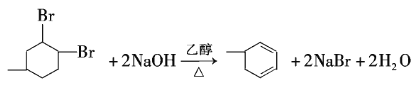
【解析】丁二烯与丙烯反应生成A为![]() ,
,![]() 与溴发生加成反应生成B为
与溴发生加成反应生成B为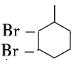 ,
, 在氢氧化钠的醇溶液中发生消去反应生成C为
在氢氧化钠的醇溶液中发生消去反应生成C为![]() ,
,![]() 与溴发生加成反应生成D为
与溴发生加成反应生成D为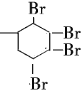 ,
, 在氢氧化钠的醇溶液中发生消去反应生成E为
在氢氧化钠的醇溶液中发生消去反应生成E为![]() 。(1)A为
。(1)A为![]() ,含有的官能团名称是碳碳双键,A的名称是4-甲基-1-环已烯(或4-甲基环已烯) ;(2)不考虑顺反异构,丙烯的二氯代物有1,1-二氯-2-丙烯、1,1-二氯-1-丙烯、1,2-二氯-2-丙烯、1,3-二氯-2-丙烯、2,3-二氯-1-丙烯共5种;(3)由上述分析可知,反应类型:①是加成反应;⑤是消去反应;(4)反应③是
,含有的官能团名称是碳碳双键,A的名称是4-甲基-1-环已烯(或4-甲基环已烯) ;(2)不考虑顺反异构,丙烯的二氯代物有1,1-二氯-2-丙烯、1,1-二氯-1-丙烯、1,2-二氯-2-丙烯、1,3-二氯-2-丙烯、2,3-二氯-1-丙烯共5种;(3)由上述分析可知,反应类型:①是加成反应;⑤是消去反应;(4)反应③是 在氢氧化钠的醇溶液中发生消去反应生成
在氢氧化钠的醇溶液中发生消去反应生成![]() ,反应的化学方程式是
,反应的化学方程式是 。
。


科目:高中化学 来源: 题型:
【题目】新泽茉莉醛是一种名贵的香料.其合成路线如下:
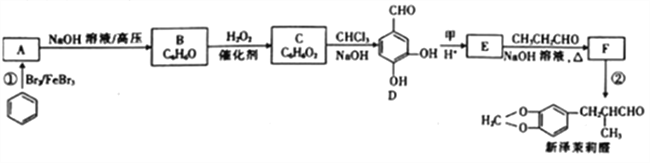
已知:①RCHO+R'CH2CHO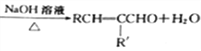
②
(1)已知甲的相对分子质量为30,甲的结构简式为____。E中含氧官能团的名称是____。
(2)反应②的反应类型是____ 。
(3)写出反应①的化学方程式:_________________。
(4)芳香族化合物G与E互为同分异构体,1molG能与足量NaHCO3溶液反应产生1mol气体,且G能发生银镜反应。则G的结构有______种。其中一种结构苯环上的一氯代物有两种,且被氧化后能与C反应生成高分子化合物,写出该高分子化合物的结构简式:_______。
(5)结合已知①,设计以乙醇和苯甲醛![]() 为原料(无机试剂任选)制备
为原料(无机试剂任选)制备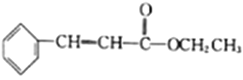 的合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件):__________________。
的合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件):__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Li4Ti5O12和LiFePO4都是锂离子电池的电极材料,可利用钛铁矿(主要成分为FeTiO3,还含有少量MgO、SiO2等杂质)来制备,工艺流程如下:

回答下列问题:
(1)“酸浸”实验中,铁的浸出率结果如下图所示。由图可知,当铁的净出率为70%时,所采用的实验条件为___________________。

(2)“酸浸”后,钛主要以TiOCl42-形式存在,写出相应反应的离子方程式__________________。
(3)TiO2·xH2O沉淀与双氧水、氨水反应40 min所得实验结果如下表所示:
温度/℃ | 30 | 35 | 40 | 45 | 50 |
TiO2·xH2O转化率% | 92 | 95 | 97 | 93 | 88 |
分析40℃时TiO2·xH2O转化率最高的原因__________________。
(4)Li2Ti5O15中Ti的化合价为+4,其中过氧键的数目为__________________。
(5)若“滤液②”中c(Mg2+)=0.02 mol/L,加入双氧水和磷酸(设溶液体积增加1倍),使Fe3+恰好沉淀完全即溶液中c(Fe3+)=1×10-5 mol/L,此时是否有Mg3(PO4)2沉淀生成?___________(列式计算)。
FePO4、Mg3(PO4)2的Ksp分别为1.3×10-22、1.0×10-24。
(6)写出“高温煅烧②”中由FePO4制备LiFePO4的化学方程式______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把下列四种X溶液分别迅速加入四个盛有10 mL 2 mol·L-1盐酸的烧杯中,此时,X和盐酸立刻进行反应,其中初始反应速率最快的是
A. 10℃ 10 mL 3 mol·L-1的X溶液 B. 20℃ 10 mL 2 mol·L-1的X溶液
C. 20℃ 10 mL 4 mol·L-1的X溶液 D. 10℃ 10 mL 2 mol·L-1的X溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组微粒,没有按照半径由小到大顺序排列的是
A. Cl、Na、F、K B. F、Cl、Na、K
C. Ca2+、K+、Cl-、S2- D. Na+、K+、Cl-、Br-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化硼是一种新合成的结构材料,它是一种超硬、耐磨、耐高温的物质。下列各组物质熔化时所克服粒子间作用力与氮化硼熔化时克服粒子间作用力的类型都相同的是
A. 硝酸钠和金刚石 B. 晶体硅和水晶
C. 冰和干冰 D. 苯和萘
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某100 mL混合液中,HNO3和H2SO4的物质的量浓度分别为0.4mol/L和0.1mol/L,向该混合液中加入1.92g铜粉。待充分反应后,所得溶液中的Cu2+的物质的量是( )
A. 0.45mol B. 0.225mol C. 0.3mol D. 0.0225mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com