
【题目】一定条件下,通过下列反应可实现燃煤烟气中硫的回收:SO2(g)+2CO(g) ![]() 2CO2(g)+S(l)△H<0若反应在恒容的密闭容器中进行,下列有关说法正确的是( )
2CO2(g)+S(l)△H<0若反应在恒容的密闭容器中进行,下列有关说法正确的是( )
A.平衡前,随着反应的进行,容器内压强始终不变
B.平衡时,其他条件不变,分离出硫,正反应速率加快
C.平衡时,其他条件不变,升高温度可提高SO2的转化率
D.其他条件不变,使用不同催化剂,该反应平衡常数不变
【答案】D
【解析】解:A.该反应是一个反应前后气体体积减小、放热的可逆反应,在反应达到平衡之前,随着反应的进行,气体的物质的量逐渐减小,则容器的压强在逐渐减小,故A错误;
B.硫是液体,分离出硫,气体反应物和生成物浓度都不变,所以不影响反应速率,故B错误;
C.该反应的正反应是放热反应,升高温度平衡向逆反应方向移动,抑制了二氧化硫的转化,所以二氧化硫的转化率降低,故C错误;
D.平衡常数只与温度有关,与使用哪种催化剂无关,故D正确;
故选D.
【考点精析】本题主要考查了化学平衡状态本质及特征的相关知识点,需要掌握化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效)才能正确解答此题.


 优学名师名题系列答案
优学名师名题系列答案科目:高中化学 来源: 题型:
【题目】常温下,向100mL 0.01molL﹣1的HA溶液中逐滴加入0.02molL﹣1的MOH溶液,图中所示曲线表示混合溶液的pH的变化情况,下列说法正确的是( ) 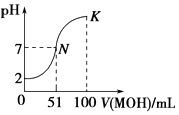
A.HA为弱酸
B.常温下,MA溶液的pH>7
C.K点对应的溶液中:c(M+)+c(MOH)=c(A﹣)
D.在N到K间任意一点对应的溶液中:c(M+)+c(H+)=c(OH﹣)+c(A﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究NO2、SO2、CO等大气污染气体的处理及利用的方法具有重要意义。
(1)新型氨法烟气脱硫技术的化学原理是采用氨水吸收烟气中的SO2,再用一定量的磷酸与上述吸收产物反应。该技术的优点除了能回收利用SO2外,还能得到一种复合肥料,该复合肥料可能的化学式为______________________(写出一种即可)。
(2)25℃ 101KPa,将1molCH4与一定量的O2混合后,充入一密闭绝热容器内,在连续电火花的作用下反应,恢复至原状况放出QkJ热量,容器内无无CH4和O2剩余且无固体物质生成,装置内气体全部通入足量的碱石灰后,剩余bmol气体。则:
①反应开始时CH4与O2的物质的量之比为___________________________。
②若已知 C(s) + O2(g) = CO2(g) △H1= -m kJ/mol
CO2(g) + C(s) = 2CO(g) △H2= +n kJ/mol
则表示CH4燃烧热的热化学方程式为_____________________________________________。
(3)工业上常用Na2CO3溶液吸收法处理氮的氧化物(以NO和NO2的混合物为例)。
已知:NO不能与Na2CO3溶液反应,
NO+NO2+Na2CO3===2NaNO2+CO2,2NO2+Na2CO3===NaNO2+NaNO3+CO2
① 用足量的Na2CO3溶液完全吸收NO和NO2的混合物,每产生22.4 L(标准状况)CO2(全部逸出)时,吸收液质量就增加44 g,则混合气体中NO和NO2的体积比为____________。
② 用Na2CO3溶液吸收法处理氮的氧化物存在的缺点是___________________。
(4)氮的固定是几百年来科学家一直研究的课题
①20世纪末,科学家采用高质子导电性的SCY陶瓷(能传递H+)为介质,用吸附在它内外表面上的金属钯多晶薄膜做电极,实现高温常压下的电化学合成氨,提高了反应物的转化率,其实验简图如图所示,正极的电极反应式是___________________________________。
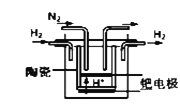
②近年,又有科学家提出在常温、常压、催化剂等条件下合成氨气的新思路,反应原理为:2N2(g)+6H2O(l)≒4NH3(g)+3O2(g),则其反应热△H=________________。
(已知:N2(g)+3H2(g)≒2NH3(g)△H=﹣92.4kJ.mol﹣1,2H2(g)+O2(g)≒2H2O(l) △H=﹣571.6kJ.mol﹣1 )
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是核电荷数依次增大的五种短周期主族元素,A元素的原子核内只有1个质子,B元素的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层多4个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C;C、E同主族。
(1)D在周期表中的位置___________;
(2)元素C、D、E形成的原子半径大小关系是______________(用元素符号表示)。
(3)C、D可形成化合物D2C2,D2C2含有的化学键类型有______________________;
(4)A、C两种元素形成的原子个数之比为1:1的化合物电子式________________;
(5)B的氢化物与B的最高价氧化物的水化物反应的离子方程式_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁铵[(NH4)2Fe(SO4)26H2O]又名摩尔盐,是浅绿色晶体,易溶于水,是分析化学中的重要试剂。某化学兴趣小组对摩尔盐的一些性质进行探究。回答下列问题:
(1)在试管中加入少量摩尔盐晶体,加水溶解,测得水溶液呈酸性。由此可知________。
(2)摩尔盐在500℃时隔绝空气加热完全分解,气体产物可能有NH3、SO2、SO3、H2O等。兴趣小组利用下图装置证明摩尔盐分解的气体产物中有SO2和SO3。

①a的名称是________。装置B的作用________。
②装置连接顺序为A→____→____→____→____(填字母序号)。
③能证明分解产物中有SO2的实验现象是________,反应的离子方程式是________。
④若装置连接顺序不变,能否将装置E中溶液换为BaCl2溶液?理由是________。
(3)为判断摩尔盐是否变质,可以测定样品中Fe2+的含量。取w g样品溶于水,配制成250 mL溶液。每次取25.00 mL溶液,用c mol/L的酸性KMnO4溶液滴定,滴定三次,平均消耗KMnO4溶液体积 v mL。
①滴定时,用________(填“酸式”或“碱式”)滴定管盛装KMnO4溶液。
②样品中Fe2+的质量分数为________(用含w、c、v的式子表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相对分子质量为112的有机物X完全燃烧只生成CO2和H2O,若X含一个六元碳环且可以发生银镜反应,则环上一溴代物的种类为( )
A.2
B.3
C.4
D.5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石油是一种重要的化工原料,可生产汽油、煤油、乙烯、苯等,实现石油的 综合利用,减少环境污染,是人类面临的重大课题.
(1)将石油分馏获得汽油、煤油等轻质油,是利用了各组分的_________不同;将 重油裂解可以获得很多化工原料,如 C8C18![]() C4H10+_____;
C4H10+_____;
(2)乙烯可制取聚乙烯塑料,聚乙烯的结构简式是______ ,它属于高分子 材料,大量使用塑料容易造成的环境问题是_______;
(3汽车尾气中的 NO 是雾霾成因之一,治理它的一种方法是在 400℃、催化剂存在的条件下使 NO 与 NH3 反应生成对大气无污染的物质,反应的化学方程式是__________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.往硝酸银溶液中滴加少量氨水:Ag++2NH3═[Ag(NH3)2]+
B.尼泊金酸( ![]() )与碳酸氢钠溶液反应:
)与碳酸氢钠溶液反应: ![]()
C.乙醛的银镜反应:CH3CHO+2[Ag(NH3)2]++2OH﹣ ![]() CH3COO﹣+NH4++2Ag↓+3NH3+H2O
CH3COO﹣+NH4++2Ag↓+3NH3+H2O
D.苯酚钠溶液中通入CO2:2C6H5O﹣+CO2+H2O→2C6H5OH+CO32﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学因腹泻引起身体严重缺水,医生除对其进行药物治疗外还考虑补液,下列补液方法最合理的是( )
A.喝葡萄糖水B.喝鲜橙汁
C.输生理盐水D.输蒸馏水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com