
在醋酸的电离过程中,加入水会使下列比值增大的是( )
|
| A. |
| B. |
|
|
| C. |
| D. |
|
| 弱电解质在水溶液中的电离平衡.. | |
| 专题: | 电离平衡与溶液的pH专题. |
| 分析: | 醋酸是弱电解质,加水稀释醋酸,促进醋酸电离,则n(CH3COO﹣)、n(H+)增大,n(CH3COOH)减小,但醋酸根离子、氢离子浓度增大的程度小于溶液体积增大的程度,所以c(CH3COO﹣)、c(H+)、c(CH3COOH)都减小,据此分析解答. |
| 解答: | 解:A.加水稀释醋酸,促进醋酸电离,则n(CH3COO﹣)增大、n(CH3COOH)减小,则 B.加水稀释,c(CH3COO﹣)减小,c(OH﹣)增大,则 C.加水稀释醋酸,促进醋酸电离,n(H+)增大,n(CH3COOH)减小,则 D.加水稀释醋酸,c(H+)减小,c(OH﹣)增大,则 故选C. |
| 点评: | 本题考查了弱电解质的电离,为高频考点,侧重于学生的分析能力和计算能力的考查,明确弱电解质电离特点是解本题关键,注意溶液中各粒子浓度或物质的量的变化,难度不大. |


 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案科目:高中化学 来源: 题型:
在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g) 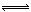 2NO2(g),随温度的升高,混合气体的颜色变深。
2NO2(g),随温度的升高,混合气体的颜色变深。
回答下列问题:
(1)反应的△H 0(填“>”或“<”);
100℃时,体系中各物质浓度随时间变化如图所示。在0~60s时段,反应速率v(N2O4)为
mol•L-1•s-1;反应的平衡常数K1= mol/L。
(2)100℃时达平衡后,改变反应温度为T,c(N2O4)以0.0020mol•L-1•s-1的平均速率降低,经10s又达到平衡。则:
① T 100℃(填“>”或“<”)。
② 计算温度T时反应的平衡常数K2= mol/L。
(3) 温度T时反应达平衡后,将反应容器的容积减少一半,则平衡向 (填“正”或“逆”)反应方向移动。
查看答案和解析>>
科目:高中化学 来源: 题型:
测定稀硫酸和稀氢氧化钠中和热的实验装
置如右图所示.
(1)写出该反应的热化学方程式(中和热为57.3 kJ/mol):
__________________________________________;
(2) 装置图中碎泡沫塑料所起作用为: ;
(3) ①取50 mL NaOH溶液和30 mL硫酸溶液进行实验,
实验数据如下表.请填写下表中的空白:
| 温度 实验次数 | 起始温度T1/℃ | 终止温度T2/℃ | 温度差平均值(T2-T1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | ________ |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 |
②若上述实验所测中和热数值偏小,产生偏差的原因可能是( )
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
查看答案和解析>>
科目:高中化学 来源: 题型:
将a%的某物质的水溶液加热蒸发掉m g水(溶质不挥发、且蒸发过程无溶质析出),所得溶液体积为V L,溶质的质量分数为蒸发前的2倍,设溶质的相对分子质量为M,则蒸发后所得溶液的物质的量浓度为( )mol/L
A ma/2VM B ma/100VM C 20ma/2VM D ma/50VM
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质全部是弱电解质的是( )
A.H2SiO3 H2S CO2 B.MgSO4 CH3COOH CH3CH2OH
C.H2SO3 BaSO4 CH4 D.H2O NH3•H2O H3PO4
查看答案和解析>>
科目:高中化学 来源: 题型:
反应P(g)+Q(g)⇌M(g)+N(s)△H<0,达到平衡时,下列说法正确的是( )
|
| A. | 减小容器体积,平衡不移动 | B. | 加入催化剂,M的产率增大 |
|
| C. | 增大c(P),P的转化率增大 | D. | 降低温度,Q的转化率增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在一体积可变的密闭容器中,加入一定量的X、Y,发生反应mX(g)⇌nY(g);△H=Q kJ/mol.反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如下表所示:
| /L积体气温体c(Y)/mol•L﹣1度/℃ | 1 | 2 | 3 |
| 100 | 1.00 | 0.75 | 0.53 |
| 200 | 1.20 | 0.90 | 0.63 |
| 300 | 1.30 | 1.00 | 0.70 |
下列说法正确的是( )
|
| A. | m>n |
|
| B. | Q<0 |
|
| C. | 温度不变,压强增大,Y的质量分数减少 |
|
| D. | 体积不变,温度升高,平衡向逆反应方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在“石蜡→液体石蜡→石蜡蒸气→裂化气”的变化过程中,被破坏的作用力依次是
A.范德华力、范德华力、共价键 B.范德华力、范德华力、范德华力
C.范德华力、共价键、共价键 D.共价键、共价键、共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室中要配制2mol/L的NaCl溶液480 ml,配制时应选用的容量瓶的规格和应称取的NaCl分别是
A.480 mL、117g B.500mL、58.5g C.480 mL、58.5 g D.500mL、117g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com