
在“石蜡→液体石蜡→石蜡蒸气→裂化气”的变化过程中,被破坏的作用力依次是
A.范德华力、范德华力、共价键 B.范德华力、范德华力、范德华力
C.范德华力、共价键、共价键 D.共价键、共价键、共价键
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案科目:高中化学 来源: 题型:
在恒容密闭容器中A(g)+3B(g)
 2C(g) ΔH<0,达平衡后,将气体混
2C(g) ΔH<0,达平衡后,将气体混
合物的温度降低,下列叙述中不正确的是 ( )
A.容器中混合气体的平均相对分子质量增大
B.正反应速率增大,逆反应速率减小,平衡向正反应方向移动
C.正反应速率和逆反应速率都变小,C的百分含量增加
D.混合气体密度的变化情况不可以作为判断反应是否再次达平衡的依据
查看答案和解析>>
科目:高中化学 来源: 题型:
PCl3和PCl5都是重要的化工原料.将PCl3(g) 和Cl2(g)充入体积不变的2L密闭容器中,在一定条件下发生下述反应,并于10min时达到平衡:PCl3(g)+Cl2(g)⇌PCl5(g),有关数据如下:
| PCl3(g) | Cl2(g) | PCl5(g) | |
| 初始浓度(mol/L) | 2.0 | 1.0 | 0 |
| 平衡浓度(mol/L) | c1 | c2 | 0.4 |
下列判断不正确的是( )
|
| A. | 10 min内,v(Cl2)=0.04 mol/(L•min) |
|
| B. | 当容器中Cl2为1.2 mol时,反应达到平衡 |
|
| C. | 升高温度(T1<T2),反应的平衡常数减小,平衡时PCl3的 |
|
| D. | 平衡后移走2.0 mol PCl3和1.0 molCl2,在相同条件下再达平衡时,c(PCl5)<0.2 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
在密闭容器中,将1.0molCO与1.0molH2O混合加热到800℃,发生下列反应:CO(g)+H2O(g)⇌CO2(g)+H2(g),一段时间后该反应达到平衡,测得CO的物质的量为0.5mol.求:
(1)达到平衡时CO2的物质的量分数和该反应的化学平衡常数;
(2)达到平衡后向该平衡体系中通入1.0mol水蒸气,达到新的平衡状态时,求水蒸气的物质的量和CO2的物质的量分数.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子在给定的条件下一定能大量共存的是
A.加入Al粉放出H2的溶液中:Na+、K+、Fe3+、NO3—
B.c(Fe3+)=0.1mol/L的溶液中:NH4+、AlO2—、SO42—、HCO3—
C.水电离出的c(H+)=1×10-13mol/L的溶液中:Mg2+、K+、NO3—、Cl—
D.c(H+)=1×10-13mol/L的溶液中:K+、Cl-、AlO2-、CO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
标准状况下V L氨气溶解在1 L水中(水的密度近似为1 g·mL-1),所得溶液的密度为
ρ g·mL-1,质量分数为w,物质的量浓度为c mol·L-1,则下列关系中不正确的是
A.ρ=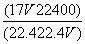 B.w=
B.w=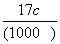 C.w=
C.w=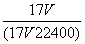 D.c=
D.c=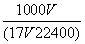
查看答案和解析>>
科目:高中化学 来源: 题型:
红磷P(s)和Cl2(g)发生反应,生成PCl3(g)和PCl5(g)。反应过程和能量的关系如图所示(图中△H表示生成1 mol 产物的数据)。
根据图回答下列问题:
 (1)P(s)和Cl2(g)反应生成PCl3(g)的热化学方程式:
(1)P(s)和Cl2(g)反应生成PCl3(g)的热化学方程式:
(2)PCl5(g)分解生成PCl3(g)和Cl2(g)的热化学方程式:
____________________;
(3)上述分解反应是一个可逆反应。温度T1时,在体积为1L的密闭容器中加入0.80mol PCl5,反应达平衡时PCl5还剩0.60mol,其分解率α1等于 ,平衡常数K1等于 ;若反应温度由T1升高到T2,平衡时PCl5的分解率为α2,平衡常数为K2,则α2 α1,
K2 K1。(填“大于”、“小于”或“等于”)
(4)P和Cl2分两步反应生成1mol PCl5的△H3 =
查看答案和解析>>
科目:高中化学 来源: 题型:
在0.1mol·L一CH3COOH溶液中存在如下电离平衡:CH3COOH  CH3COO一+ H+,对于该平衡,下列叙述不正确的是 ( )
CH3COO一+ H+,对于该平衡,下列叙述不正确的是 ( )
A.加入水时,平衡向正反应方向移动,溶液中n(H+)增大
B.加入少量冰醋酸,平衡向正反应方向移动,溶液中c(H+)增大
C.加入少量0.1 mol·L-HCl溶液,平衡向逆反应方向移动,溶液中c(H+)减小
D.加入少量CH3COONa固体,平衡向逆反应方向移动,溶液中c(H+)减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com