
【题目】X,Y,Z三种物质中含同种元素,在一定条件下可以实现如图所示转化,下列推断不正确的是( ) 
A.若Y为氧化铝,则Y 生成X的条件是“通电”
B.若X为硫单质,则Y 可能为硫化氢
C.若Z为硝酸,则X可能为一氧化氮
D.若Z为硝酸铁,则Y一定为铁单质
 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:
【题目】25℃时加水稀释10mL pH=11的氨水,下列判断正确的是( )
A.原氨水的浓度为10﹣3mol?L﹣1
B.溶液中 ![]() 减小
减小
C.氨水的电离程度增大,溶液中所有离子的浓度均减小
D.再加入10 mL pH=3的盐酸充分反应后混合液的pH值肯定大于7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,用浓度为0.1000molL﹣1 NaOH溶液分别滴定20.00mL浓度均为0.1000molL﹣1的三种酸HX、HY、HZ,滴定曲线如图所示.下列说法正确的是( ) 
A.相同浓度时,三种酸的酸性强弱顺序是:HX>HY>HZ
B.根据滴定曲线可得,Ka(HX)=10﹣3 molL﹣1
C.滴定HY,V(NaOH)=20 mL时,c(Na+)=c(Y﹣)>c(OH﹣)=c(H+)
D.滴定HZ,V(NaOH)=15 mL时,c(Z﹣)>c(Na+)>c(H+)>c(OH﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯。其变化可以表述为:
KClO3+ HCl(浓) → KCl+ ClO2↑+ Cl2↑+ H2O
(1)请完成该化学方程式并配平__________________
(2)浓盐酸在反应中显示出来的性质是_______(填写编号,多选倒扣)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)产生0.1molCl2,则转移的电子的物质的量是为_________mol。
(4)ClO2具有很强的氧化性。因此,常被用作消毒剂,其消毒的效率(以单位质量得到的电子数表示)是Cl2的_______倍。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组同学利用氧化还原反应:2KMnO4+10FeSO4+8H2SO4=2MnSO4+5Fe2(SO4)3+K2SO4+8H2O设计如下原电池,盐桥中装有饱和溶液.下列说法正确的是( ) 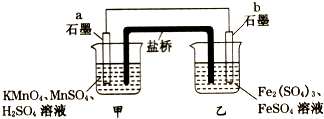
A.a电极上发生的反应为:MnO4﹣+8H++5e﹣═Mn2++4H2O
B.外电路电子的流向是从a到b
C.电池工作时,盐桥中的SO42﹣移向甲烧杯
D.b电极上发生还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种制取纯碱的方法如下:

(1)写出“反应I ”的化学方程式:__。
(2)“反应Ⅱ”为复分解反应,反应中所涉及物质的溶解度如图所示。写出“反应Ⅱ”的化学方程式:__。

(3)写出“煅烧”反应的化学方程式:__。
(4) “蒸氨”时需要加热,写出“蒸氨”时反应的化学方程式:___。
(5)写出将“蒸氨”产生的氨气通入Al2(SO4)3溶液中时反应的离子方程式: __。
【答案】 NH3·H2O+CO2=NH4HCO3 NaCl+NH4HCO3=NaHCO3↓+NH4Cl 2NaHCO3![]() Na2CO3+CO2↑+H2O 2NH4Cl+Ca(OH)2
Na2CO3+CO2↑+H2O 2NH4Cl+Ca(OH)2 ![]() CaCl2+2NH3↑+2H2O Al3++3NH3·H2O=Al(OH)3↓+3NH4+
CaCl2+2NH3↑+2H2O Al3++3NH3·H2O=Al(OH)3↓+3NH4+
【解析】(1)氨水显碱性,CO2为酸性氧化物,二者反应生成盐,CO2过量时生成酸式盐即碳酸氢铵,故化学方程式为:NH3·H2O+CO2=NH4HCO3。
(2)氨气极易溶于水,氨水的浓度非常大,可以溶解大量的氨气,则反应I得到浓度较大的碳酸氢铵溶液。向碳酸氢铵溶液中加入食盐后,溶液中主要存在四种离子:Na+、NH4+、HCO3-、Cl-,根据溶解度曲线可知,同温度下NaHCO3的溶解度最小,溶液中会析出晶体NaHCO3。反应II为复分解反应,则反应方程式为NaCl+NH4HCO3=NaHCO3↓+NH4Cl。
(3)过滤得到NaHCO3晶体,加热,NaHCO3分解为Na2CO3、H2O、CO2,反应方程式为:2NaHCO3![]() Na2CO3+CO2↑+H2O;
Na2CO3+CO2↑+H2O;
(4)向NH4Cl溶液中加入石灰乳,NH4+与OH-结合为NH3·H2O,加热条件下,促进NH3逸出,即为“蒸氨”,反应方程式为2NH4Cl+Ca(OH)2 ![]() CaCl2+2NH3↑+2H2O;
CaCl2+2NH3↑+2H2O;
(5)氨气溶于水得NH3·H2O,NH3·H2O碱性强于Al(OH)3,故将NH3通入Al2(SO4)3溶液中有Al(OH)3沉淀生成,离子方程式为:Al3++3NH3·H2O=Al(OH)3↓+3NH4+。
【题型】综合题
【结束】
22
【题目】实验室制备氯化亚铜(一种难溶于水的白色固体)的流程如下:

(1)“反应I”在加热条件下进行,同时有MnCl2生成,该反应的化学方程式为 __。
(2) “反应Ⅱ”中杂质与Cl2反应的化学方程式为__。 ⑶实验所用SO2气体可由铜和浓硫酸反应制得,该反应的化学方程式为__
(4)“反应Ⅲ”的离子方程式为___。
(5)若将等物质的量的S02、Cl2通入水中,所得溶液几乎没有漂白性,该反应的离子方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,部分物质的电离平衡常数如表所示:
化学式 | CH3COOH | H2C2O4 | H2S |
电离平衡常数 | 1.8×10﹣5 | Ka1=5.4×10﹣2 | Ka1=1.3×10﹣7 |
请回答下列问题:
(1)H2S的一级电离常数表达式为Ka1=
(2)CH3COOH、H2C2O4、H2S的酸性由强到弱的顺序
(3)H2C2O4与少量的KOH溶液反应的化学方程式:
(4)NaHS溶液与NaHC2O4溶液反应的离子方程式:
(5)H+浓度相同等体积的两份溶液A(盐酸)和B(CH3COOH)分别与锌粉反应,若最后仅有一份溶液中存在锌,放出氢气的质量相同,则下列说法正确的是(填写序号). ①反应所需要的时间B>A
②开始反应时的速率A>B
③参加反应的锌的物质的量A=B
④反应过程的平均速率B>A
⑤B中有锌剩余.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com