
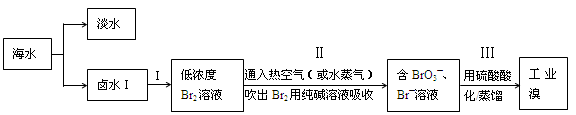
 =0.4125mol����Һ���V=0.4125L��
=0.4125mol����Һ���V=0.4125L��

 ��ѧ�����ϵ�д�
��ѧ�����ϵ�д� �·Ƿ��̸����100��ϵ�д�
�·Ƿ��̸����100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����


| | ���� | 1������ | ���ᶡ�� |
| �۵�(��) | 16��6 | ��89��5 | ��73��5 |
| �е�(��) | 117��9 | 117 | 126��3 |
| �ܶ�(g/cm3) | 1��05 | 0��81 | 0��88 |
| ˮ���� | ���� | ���� (9g/100gˮ) | �� |




�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������

 Al(OH)3+OH����
Al(OH)3+OH�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������ˮ���𱽺��屽 |
| B����BaCl2��Һ����SO42����CO32�� |
| C����ŨHNO3��Cu��Ӧ��ȡNO |
| D��������HCl��Cl2ͨ�뱥��NaHCO3��Һ�г�ȥHCl |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������

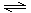 2RAn���л��㣩 + nH2SO4 (ˮ��)
2RAn���л��㣩 + nH2SO4 (ˮ��) �鿴�𰸺ͽ���>>
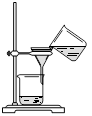
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
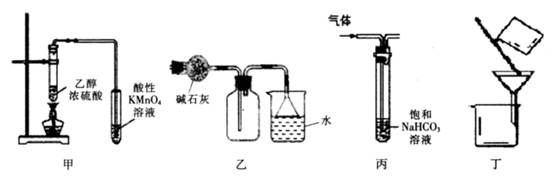
| A��װ�ü����ڼ�������ϩ���� |
| B��װ���ҿ������ռ������հ��� |
| C��װ�ñ������ڳ�ȥCO2�л��е�HCl���� |
| D��װ�ö������ڳ�ȥ�屽�е��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| | �Լ��� | ����X | ����Y |
| A | HCl��Ba(OH)2 | CO32�� | HCO3- |
| B | NH3 ��H2O | Al3+ | Mg2+ |
| C | AgNO3 | I�� | Cl�� |
| D | NH4SCN����ˮ | Fe2+ | Fe3+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
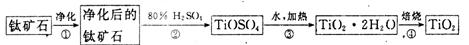
 TiCl4��1��+O2��g�� ��H��+151 kJ/mol�����Բ���ֱ����TiO2��Cl2��Ӧ�����Ȼ���Ӧ������ȡTiCl4����˵���жϸ÷�Ӧ���Է�����������_______�������Ȼ���Ӧ��ϵ�м���̼��Ӧ�ڸ�����������˳����������TiCl4��
TiCl4��1��+O2��g�� ��H��+151 kJ/mol�����Բ���ֱ����TiO2��Cl2��Ӧ�����Ȼ���Ӧ������ȡTiCl4����˵���жϸ÷�Ӧ���Է�����������_______�������Ȼ���Ӧ��ϵ�м���̼��Ӧ�ڸ�����������˳����������TiCl4�� 394 kJ/mol��
394 kJ/mol��
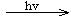 TiO2/S*������̬��
TiO2/S*������̬�� TiO2/S+ + e-
TiO2/S+ + e- 3I-
3I- 2TiO2/S + I3-
2TiO2/S + I3-| A����ع���ʱ��I-�����ڶƲ����粣���缫�Ϸŵ� |
| B����ع���ʱ���ǽ�̫����ת��Ϊ���� |
| C����صĵ������Һ��I-��I3- Ũ�Ȳ������ |
| D������жƲ����粣��Ϊ���� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com