
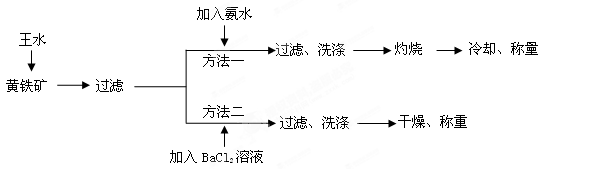
 S2+5HNO3+3HCl=FeCl3+2H2SO4+5NO↑+2H2O
S2+5HNO3+3HCl=FeCl3+2H2SO4+5NO↑+2H2O| A.NaOH | B.BaCl2 | C.HCl | D.Na2SO4 |
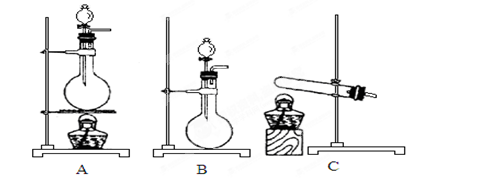
 ,则该矿石中FeS2的质量分数是________________。
,则该矿石中FeS2的质量分数是________________。科目:高中化学 来源:不详 题型:单选题
| A.用食盐水除水垢 |
| B.用加热的方法给聚乙烯塑料袋封口 |
| C.用铅笔芯代替石墨试验导电性 |
| D.用灼烧的方法区别羊毛线和棉线 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
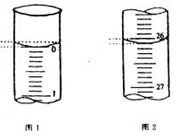
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
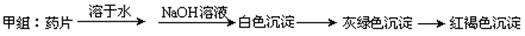 甲组同学按照设计的方案完成实验,但遗憾的是他们没有得到预期的实验结果,
甲组同学按照设计的方案完成实验,但遗憾的是他们没有得到预期的实验结果, 
 进行实验验证:________________________________
进行实验验证:________________________________| 序号 | V(KMnO4)初 | V(KMnO4)终 | V(KMnO4) |
| 1 | 2.24mL | 14.25mL | 12.01mL |
| 2 | 0.30mL | 12.72mL | 12.42mL |
| 3 | 0.50mL | 12.53 | 12.03mL |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.②⑥③⑦⑤ | B.④③⑤⑦⑥ | C.①③⑦⑤⑥ | D.②⑤⑦⑥ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 要的用途,分别是 和 ;
要的用途,分别是 和 ; 色。该同学还想通过实验分别证实溶质中含有Cu2+、SO42-,请你帮他想想办法,选择适当的试剂(写化学式),并写出其相应的离子方程式。
色。该同学还想通过实验分别证实溶质中含有Cu2+、SO42-,请你帮他想想办法,选择适当的试剂(写化学式),并写出其相应的离子方程式。| 溶质 | 加入试剂 | 离子方程式 |
| Cu2+ | | |
| SO42- | | |
 液浓度将
液浓度将  ;
;查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
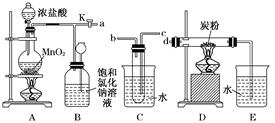
 斗中,然后再注入10 mL CCl4,盖好玻璃塞,振荡,静置于铁架台上,等分层后取上层液
斗中,然后再注入10 mL CCl4,盖好玻璃塞,振荡,静置于铁架台上,等分层后取上层液 和下层液,呈黄绿色的是________(填“上层液”或“下层液”),能使有色布条褪色的是________(填“上层液”或“下层液”).
和下层液,呈黄绿色的是________(填“上层液”或“下层液”),能使有色布条褪色的是________(填“上层液”或“下层液”).
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 应后的混合物过滤,再向得到的滤液中加入_____________溶液。
应后的混合物过滤,再向得到的滤液中加入_____________溶液。查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
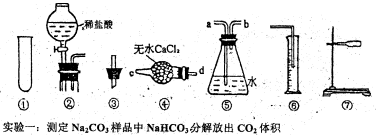
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com