
| A、氧化还原反应的本质是元素化合价发生变化 |
| B、物质所含元素化合价降低的反应是氧化反应 |
| C、置换反应一定属于氧化还原反应 |
| D、化合反应和分解反应不可能是氧化还原反应 |


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:
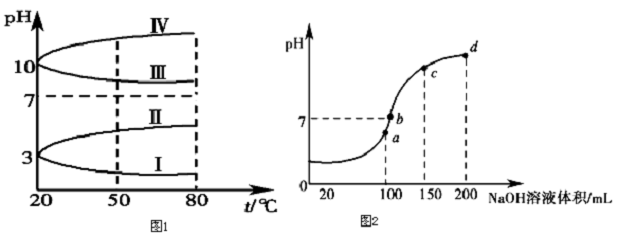
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1molCl2参加的任何反应,反应过程中转移电子数都是2NA |
| B、标准状况下,11.2L乙醇所含的羟基数为0.5NA |
| C、常温常压下,17g甲基(-14CH3)所含的中子数为9NA |
| D、室温下,42.0 g乙烯和丙烯的混合气体中含有的碳原子数约为3×6.02×1023个 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH3COOH+H2O?CH3COO-+H3O+ |
| B、CO2+H2O?HCO3-+H+ |
| C、CO32-+H2O?HCO3-+OH- |
| D、HS-+H2O?S2-+H3O+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、厕所清洁剂 醋 肥皂 厨房清洁剂 |
| B、醋 厕所清洁剂 肥皂 厨房清洁剂 |
| C、厕所清洁剂 厨房清洁剂 醋 肥皂 |
| D、厨房清洁剂 醋 肥皂 厕所清洁剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com