
【题目】已知X+、Y-、Z,H2O均为10电子结构的微粒,Z可使湿润的红色石蕊试纸变蓝,它们在一定条件下可发生如图转化。下列说法正确的是
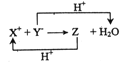
A. X+含有离子键
B. H2O的电子式为H:O:H
C. 含有Y的溶液一定显碱性
D. Z的沸点低于H2O的沸点
 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:
【题目】苏轼的《格物粗谈》中记载:“红柿摘下未熟,每篮用木瓜三枚放入,得气即发,并无涩味。”按照现代科技观点,该文中的“气”是指
A. 乙烯B. 脱落酸C. 生长素D. 甲烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素及其化合物的应用研究是目前科学研究的前沿之一。试回答下列问题:
(1)原子序数小于36的过渡元素A和B,在周期表中位于同一族,且原子序数B比A多1,基态B原子中含有三个未成对电子。请写出B元素在周期表中的位置为______,属于___区元素,A2+在基态时价电子排布图为__________________。
(2)二氧化钛作光催化剂能将居室污染物甲醛、苯等有害气体可转化为二氧化碳和水,达到无害化。水分子中心原子价层电子对数为____,二氧化碳的VSEPR模型为______,苯分子中碳原子的杂化类型为________。
(3)Co3+有多种配合物,如Co(CN)63-、Co(NH3)4Cl2+ 等。铑(Rh)与钴属于同族元素,某些性质相似。现有铑的某盐组成为CsRh(SO4)2·4H2O,易溶解于水,向其水溶液中加入一定浓度的BaCl2溶液,无沉淀生成。该盐中铑离子的配位数为____。请写出该盐溶解于水后的电离方程式:_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的SO2和含1molO2的空气(不考虑其他酸性气体)充入2L的恒容密闭容器中,某温度时,在催化剂作用下发生反应:2SO2(g)+O2 (g) ![]() 2SO3 (g) △H<0。反应达到平衡后,将容器中的混合气体通过过量NaOH溶液,气体减少了1.8 mol。再将剩余气体通过某溶液吸收O2,气体又减少了0.2 mol。请回答下列问题:
2SO3 (g) △H<0。反应达到平衡后,将容器中的混合气体通过过量NaOH溶液,气体减少了1.8 mol。再将剩余气体通过某溶液吸收O2,气体又减少了0.2 mol。请回答下列问题:
(1)判断该反应达到平衡状态的标志是________(填字母)。
a.容器中混合气体的密度保持不变 b.SO2体积分数保持不变
c.容器中气体的压强不变 d.SO3的生成速率与SO2的消耗速率相等
(2)欲提高SO2的转化率,下列措施可行的是_______(填字母)。
a.向容器中再充人N2 b.向容器中再充入O2
c.改变反应的催化剂 d.降低温度
(3)升高温度,上述反应的平衡常数K______(填“增大”“减小”或“不变”,下同),化学反应速率______。
(4)该温度下,反应2SO2 (g) +O2 (g) ![]() 2SO3(g)的平衡常数K=___________。
2SO3(g)的平衡常数K=___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】切开后的苹果因被空气氧化而会很快变黄,有人戏称苹果“生锈了”,柠檬汁中含有大量维生素C,把它滴在切面上,可减缓苹果“生锈”。这说明维生素C具有
A.酸性 B.氧化性 C.碱性 D.还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】干冰在一定条件下可以形成CO2气体,CO2气体在一定条件下又可以与金属镁反应生成氧化镁和碳,这两个变化过程中需要克服的作用力分别是( )
A. 分子间作用力,化学键B. 化学键,化学键
C. 化学键,分子间作用力D. 分子间作用力,分子间作用力
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下电离方程式错误的是
A. NaOH=Na++OH- B. Fe2(SO4)3=2Fe3++3SO42-
C. MgCl2=Mg2++2Cl- D. NaHCO3=Na++H++CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】要证明某溶液中不含Fe3+而可能含Fe2+,进行如下实验操作时,最佳顺序是
①加入足量氯水②加入足量KMnO4溶液③加入少量KSCN溶液
A.①② B.③② C.②①③ D.③①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数值,下列说法不正确的是
A. 10g D216O中所含中子数为5NA
B. 标准状况下,22.4L乙烷中所含共价键数目为7NA
C. 7.8gNa2O2中所含阴、阳离子总数目为0.4NA
D. 密闭容器中,1molN2和3molH2充分反应后,容器中的分子数一定大于2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com