
【题目】在Na2SO4、NaCl、NaOH的混合溶液中,含有Na+、SO42-、OH-的个数比8:1:2,则溶液中Na2SO4、NaCl、NaOH个数比为
A.1:1:1 B.1:4:2 C.1:2:4 D.1:3:2
科目:高中化学 来源: 题型:
【题目】某同学用含少量硫酸铁的硫酸钠固体,制取芒硝(Na2SO4·10H2O),操作流程图如下所示,请回答下列问题:
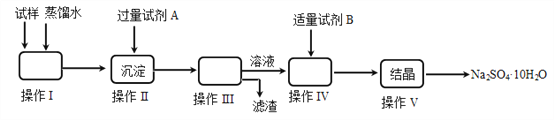
(1)操作I的名称是________;操作III所需的玻璃仪器有________________________。
(2)试剂A为__________;试剂B为__________,加入试剂B的目的是__________________,实验中加入适量试剂B的实验方案为___________________。
(3)操作V的步骤依次是________(用编号填入)
a.过滤 b.冷却 c.蒸发浓缩 d.蒸发至接近蒸干
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应3Cl2 + 6NaOH=5NaCl + NaClO3 + 3H2O,对该反应的下列说法不正确的( )
A. Cl2既是氧化剂,又是还原剂
B. 反应中转移的电子数为5e-
C. 氧化剂与还原剂的质量比是1∶5
D. 被氧化的氯原子数与被还原的氯原子数之比是1∶5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】蜜蜂信息素的成分之一是乙酸异戊酯,它具有香蕉的香味,实验室用乙酸和异戊醇[(CH3)2CHCH2CH2OH]制备乙酸异戊酯的反应、装置示意图和有关数据如下:
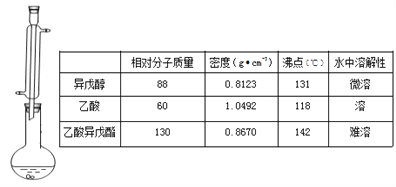
实验步骤:
在A中加入4.4 g的异戊醇,6.0 g的乙酸、数滴浓硫酸和23片碎瓷片,开始缓慢加热A,回流50min,反应液冷至室温后,倒入分液漏斗中,分别用少量水,饱和碳酸氢钠溶液和水洗涤,分出的产物中加入少量无水MgSO4固体,静置片刻,过滤除去MgS04固体,进行蒸馏纯化,收集140143℃馏分,得乙酸异戊酯3.9g.
回答下列问题:
(1)装置B的名称是 ___________,作用是______________。
(2)碎瓷片的作用是______________ 。
(3)欲得到乙酸异戊酯,在洗涤、分液操作中,应充分振荡,然后静置,待分层后__________
a.直接将乙酸异戊酯从分液漏斗上口倒出
b.直接将从分液漏斗下口放出
c.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
d.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口倒出
(4)实验中加入少量无水MgS04的目的是____________ 。
(5)A中的反应方程式为___________________,本实验的产率是____________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜,锌元素的化合物种类很多,我们可以利用所学物质结构与性质的相关知识去认识和理解它们。
(1)CuSO4和Cu(NO3)2是自然界中重要的铜盐。
① CuSO4和Cu(NO3)2中阳离子的基态价层电子排布式为_______________。
② S、O、N三种元素的第一电离能由大到小为_____________。
③ CuSO4的熔点为560℃,Cu(NO3)2的熔点为115℃,CuSO4熔点更高的原因是________。
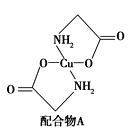
(2)硫酸铜溶液中滴入氨基乙酸钠(H2NCH2COONa)即可得到配合物A,其结构如图所示。请回答下列问题:
① 配合物A中N原子的轨道杂化类型为__________。
② 1 mol配合物A含有σ键的数目为_____________。
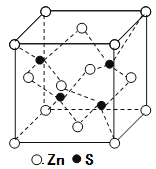
(3)立方ZnS晶体的密度为ρg·cm-3, 其晶胞结构如图。S2-周围等距离且最近的Zn2+、S2-依次为______、______;ZnS晶胞中的晶胞参数a=________nm(列出计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W均为短周期元素,在周期表中位置如图,Y原子的最外层电子数是其次外层电子数的3倍。下列说法正确的是

A. X、Y、Z的原子半径大小:X>Y>Z
B. Y、Z的气态氢化物中,前者更稳定
C. Z、W的最高价氧化物对应水化物的酸性,前者更强
D. X、W的气态氢化物相互反应,生成物中既含离子键又含共价键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com