
常温下,下列叙述错误的是
A.向0.1mol·L-1的醋酸溶液中加水或通入HCl气体都能使 值增大 值增大 |
| B.0.1mol·L-1的醋酸钠溶液20mL与0.1mol·L-1盐酸10mL混合后溶液显酸性,则有c(CH3COO-)>c(Cl-)>c(H+)>c(CH3COOH) |
| C.pH=4的醋酸与pH=10的氢氧化钠溶液等体积混合,所得溶液pH<7 |
D.0.1mol·L-1某一元酸HA溶液中 =1×10-8,则该溶液中由水电离出的c(H+)=1×10-11mol/L =1×10-8,则该溶液中由水电离出的c(H+)=1×10-11mol/L |
B
解析试题分析:A、醋酸是弱酸,存在电离平衡CH3COOH CH3COO-+H+。加入稀释促进醋酸的电离,氢离子的物质的量增加,醋酸的物质的量减少,所以
CH3COO-+H+。加入稀释促进醋酸的电离,氢离子的物质的量增加,醋酸的物质的量减少,所以 值增大。通入氯化氢气体,增大氢离子的浓度,抑制醋酸的电离,但氢离子增大的倍数大于醋酸增大的倍数,所以
值增大。通入氯化氢气体,增大氢离子的浓度,抑制醋酸的电离,但氢离子增大的倍数大于醋酸增大的倍数,所以 值增大,A正确;B、0.1mol·L-1的醋酸钠溶液20mL与0.1mol·L-1盐酸10mL混合后生成醋酸和氯化钠,醋酸钠过量,且三种物质的物质的量相等。由于溶液显酸性,即c(H+)>c(OH-),这说明醋酸的电离程度大于CH3COO-的水解程度,所以c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+),B不正确;C、醋酸是弱酸,存在电离平衡,则.pH=4的醋酸的浓度大于1×10-4mol/L,所以与pH=10的氢氧化钠溶液等体积混合醋酸过量,溶液的pH<7,C正确;D、0.1mol·L-1某一元酸HA溶液中
值增大,A正确;B、0.1mol·L-1的醋酸钠溶液20mL与0.1mol·L-1盐酸10mL混合后生成醋酸和氯化钠,醋酸钠过量,且三种物质的物质的量相等。由于溶液显酸性,即c(H+)>c(OH-),这说明醋酸的电离程度大于CH3COO-的水解程度,所以c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+),B不正确;C、醋酸是弱酸,存在电离平衡,则.pH=4的醋酸的浓度大于1×10-4mol/L,所以与pH=10的氢氧化钠溶液等体积混合醋酸过量,溶液的pH<7,C正确;D、0.1mol·L-1某一元酸HA溶液中 =1×10-8,则根据水的离子积常数可知,溶液中c(OH-)=
=1×10-8,则根据水的离子积常数可知,溶液中c(OH-)=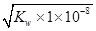 =1×10-11mol/L,因此溶液中由水电离出的c(H+)=1×10-11mol/L,D正确,答案选B。
=1×10-11mol/L,因此溶液中由水电离出的c(H+)=1×10-11mol/L,D正确,答案选B。
考点:考查外界条件对弱电解质电离平衡的影响、溶液中离子浓度大小比较、溶液酸碱性的判断以及溶液中氢离子浓度的计算等


科目:高中化学 来源: 题型:单选题
下列关于电解质溶液的叙述正确的是
| A.常温下,Na2CO3溶液的pH>7 |
| B.0.1mol/L Na2CO3溶液在35℃时碱性比25℃强,说明该水解反应是是放热反应 |
| C.常温下.pH=7的NH4Cl与氨水的混合溶液中各离子浓度的关系为: c(Cl-)=c(NH4+)>c(H+)=c(OH一) |
| D.常温下,中和pH与体积均相同的盐酸和醋酸,消耗NaOH的物质的量相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
化学知识在生活中有重要意义,下列说法不正确的是
| A.草木灰(含有K2CO3)水溶液可以用于洗涤油污 |
| B.乙醇、乙酸和甲醛广泛应用于食品加工 |
| C.捕获排放的CO2能降低地球的温室效应 |
| D.在海轮外壳上镶入锌块,可减缓船体的腐蚀速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
对于常温下0.1mol·L-1 NaHCO3溶液,下列叙述不正确的是( )
| A.c (Na+)="c" (HCO3-) + c (CO32-) + c (H2CO3) |
| B.温度升高,溶液的pH升高,但溶液中的c(H+)与c(OH-)乘积不变 |
| C.与等体积等浓度的CH3COOH溶液反应后,溶液中c(Na+)>c(CH3COO-) |
| D.加入适量的NaOH固体,溶液的pH减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列关于pH=12的Na2CO3溶液说法正确的是
| A.升高溶液温度,溶液pH增大 |
| B.c(Na+) +c(H+)=c(CO32-)+ c(HCO3-)+ c(OH-) |
| C.溶液中c(OH-)>c(HCO3-)> c(H+) |
| D.2c(Na+)=c(CO32-)+ c(HCO3-)+ c(H2CO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
硼酸(H3BO3)溶液中存在如下反应:H3BO3(aq)+H2O(1) [B(OH)4]-(aq)+H+(aq)。
[B(OH)4]-(aq)+H+(aq)。
下列说法正确的是
| 化学式 | 电离常数(298K) |
| 硼酸 | K=5.7×10-10 |
| 碳酸 | K1=4.4×10-7 K=4.7×10-11 |
| 醋酸 | K=1.75×10-5 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
25℃时,有c(CH3COOH)+c(CH3COO-)=" 0." 1 mol·L-1的一组醋酸、醋酸钠混合溶液,溶液中c(CH3COOH)、c(CH3COO-)与pH 的关系如图所示。下列有关溶液中离子浓度关系的叙述正确的是
| A.X点所表示的溶液中:c(Na+)+ c(OH-) = c(CH3COO-) + c(H+) |
| B.W 点所表示的溶液中:c(Na+) +c(H+) -c(OH-) +c(CH3COOH)=" 0." 1mol·L-1 |
| C.该温度下醋酸的电离平衡常数为10-4.75 mol·L-1 |
| D.向X点所表示的溶液中加入等体积的0. 05mol·L-1NaOH溶液:c(H+)= c(CH3COOH)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
向20.00mL稀H2SO4中逐滴加入0.10mol/L的氨水,测得溶液的pH随加入氨水的体积变化如图所示。下列判断正确的是( ) 
| A.x=20 |
| B.稀H2SO4的浓度为0.10mol/L |
| C.b点有:2c(NH4+) = c(SO42-)> c(H+) = c(OH-) |
| D.a点有:c(NH4+) < 2c(SO42-) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
在稀氨水中存在下述电离平衡NH3+H2O NH3 ·H2O
NH3 ·H2O NH4++OH-,分别加入少量下列物质,溶液中c(OH-)如何变化?(填“增大”“减小”或“不变”);平衡移动方向如何?(填“正向”“逆向”或“不移动”)
NH4++OH-,分别加入少量下列物质,溶液中c(OH-)如何变化?(填“增大”“减小”或“不变”);平衡移动方向如何?(填“正向”“逆向”或“不移动”)
| 加入的物质 | 少量(NH4)2SO4固体 | 少量HNO3溶液 | 少量KOH溶液 |
| c(OH-)的变化 | | | |
| 平衡移动方向 | | | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com