
( 9分)重铬酸钾(K2Cr2O7)是重要氧化剂,重铬酸钾的溶解度受温度影响较大,工业上常用铬铁矿(主要成分为FeO?Cr2O3,杂质为SiO2?Al2O3)为原料生产它。实验室模拟工业上用铬铁矿制 K2CrO7的主要工艺流程如下图。涉及“碱熔”的主要反应为:
6 FeO?Cr2O3 + 24NaOH + 7KC1O3 = 12NaCrO4 + 3Fe2O3 + 7KCl + 12H2O
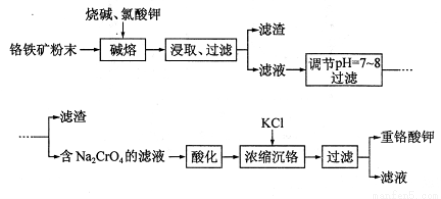
(1)使用粉末状铬铁矿的目的是 。
(2)调节pH后,过滤得到的滤渣是 (填化学式)。
(3)酸化Na2CrO4溶液时,其平衡转化的离子方程式为 。
(4)称取重铬酸钾试样2.500g配成500mL溶液,取出25.00mL于锥形瓶中,加入10 mL2mol/LH2SO4和足量碘化钾(铬的还原产物为Cr3+),放于暗处5min。然后加入100 mL 水,加人3mL淀粉溶液(作指示剂),用0.1200 mol/LNa2S2O3标准溶液滴定( I2 + 2S2O2- 3= 2I-+S4O2- 6),用去20.00mL ,则该样品的纯度为 。
(1)增大接触面积,加快化学反应速率,且使铬铁矿充分反应;(2)Al(OH)3、H2SiO3;
(3)2CrO42-+2H+ Cr2O72-+H2O;(4)0.9408.
Cr2O72-+H2O;(4)0.9408.
【解析】
试题分析:(1)使用粉末状铬铁矿的目的是增大接触面积,加快化学反应速率,且使铬铁矿充分反应;(2)铬铁矿用烧碱、氯酸钾溶解后得到的物质中,难溶性的固体物质有Fe2O3;滤液中含有NaCrO4 、KCl、NaAlO2、Na2SiO3;当调节pH为7~8后,Al、Si就形成Al(OH)3、H2SiO3沉淀经过过滤除去,而在滤液中含有NaCrO4 、KCl;(3)酸化Na2CrO4溶液时,其平衡转化的离子方程式为2CrO42-+2H+ Cr2O72-+H2O;(4)根据电子守恒可得:Cr2O72-~3 I2 ~ 6S2O2- 3;n(S2O32-)= 0.1200 mol/L×0.020L=2.4×10-3mol;所以在25.00mL重铬酸钾试样中含有溶质的物质的量是4×10-4mol,所以重铬酸钾试样2.500g配成500mL溶液中含有溶质的物质的量是(500mL÷25.00mL)×4×10-4mol=8×10-3mol.n(K2Cr2O7)= 8×10-3mol×294g/mol=2.352g,所以该样品的纯度为(2.352g÷2.500g)×100%=94.8%。
Cr2O72-+H2O;(4)根据电子守恒可得:Cr2O72-~3 I2 ~ 6S2O2- 3;n(S2O32-)= 0.1200 mol/L×0.020L=2.4×10-3mol;所以在25.00mL重铬酸钾试样中含有溶质的物质的量是4×10-4mol,所以重铬酸钾试样2.500g配成500mL溶液中含有溶质的物质的量是(500mL÷25.00mL)×4×10-4mol=8×10-3mol.n(K2Cr2O7)= 8×10-3mol×294g/mol=2.352g,所以该样品的纯度为(2.352g÷2.500g)×100%=94.8%。
考点:考查影响化学反应速率的因素、反应条件的选择、守恒法在化学计算中的应用、物质纯度的计算的知识。


科目:高中化学 来源:2015届湖北省高二下学期期中考试化学试卷(解析版) 题型:填空题
某烃类化合物A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双键,核磁共振氢谱表明分子中只有一种类型的氢。
(1)A的结构简式为 ;
(2)A中的碳原子是否都处于同一平面? (填“是”或“不是”);
(3)已知A、B、C有如下转化关系:
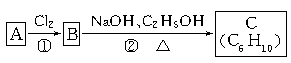
则反应②的化学方程式为 ;C的化学名称是 。
查看答案和解析>>
科目:高中化学 来源:2015届湖北省高三上学期起点考试化学试卷(解析版) 题型:选择题
化学用语在化学学科中作用非常重要,以下有关化学用语描述正确的是:
A.Mg2+的结构示意图: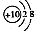 B.Na2S的电子式:
B.Na2S的电子式: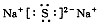
C.氨气的空间结构:三角形 D.乙烯的结构简式:(CH2)2
查看答案和解析>>
科目:高中化学 来源:2015届湖北省襄阳市四校高二下学期期中联考化学试卷(解析版) 题型:选择题
下表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )
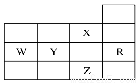
A.W元素最高价含氧酸酸性强于Y元素最高价含氧酸酸性
B.Z的阴离子电子层结构与R原子的相同
C.p能级未成对电子数最多的是Z元素
D.X元素是电负性最大的元素
查看答案和解析>>
科目:高中化学 来源:2015届湖北省新高三起点调研测试化学试卷(解析版) 题型:填空题
(15分) 【化学 ― 选修 3 物质结构与性质】
氮的化合物在无机化工领域有着重要的地位。请回答下列问题:
(1)基态氮原子的价电子排布图为 。
(2)氮的最高价氧化物为无色晶体,它由两种离子构成:已知其阴离子构型为平面正三角形,则其阳离子的构型为 形,阳离子中氮的杂化方式为 。
(3)某氮铝化合物X具有耐高温、抗冲击、导热性好等优良性质,广泛用于陶瓷工业等领域。工业上用氮气、氧化铝和碳在一定条件下反应生成CO和X (X的晶体结构如图所示),工业制备 X 的化学方程式为 。
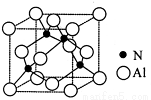
(4)X晶体中包含的化学键类型为 (填字母标号)。
A .离子键 B .共价键 C .配位键 D .金属键
(5)已知氮化硼与X晶体类型相同,且氮化硼的熔点比X高,其原因 是 。
(6)若X的密度为ρg/cm3,则晶体中最近的两个Al 原子的距离为 cm (阿伏加德罗常数用 NA表示,不必化简)。
查看答案和解析>>
科目:高中化学 来源:2015届湖北省新高三起点调研测试化学试卷(解析版) 题型:选择题
常温下,不可能与小苏打溶液反应生成二氧化碳气体的物质是
A.酸溶液 B.碱溶液 C.盐溶液 D.氧化物
查看答案和解析>>
科目:高中化学 来源:2015届湖北省新高三起点调研测试化学试卷(解析版) 题型:选择题
NA表示阿伏加德罗常数的值,下列叙述正确的是
A .84gNaHCO3晶体中含有 NA个 CO2- 3
B.0 . lmol/LK2CO3溶液中,阴离子总数大于 0.1NA
C. 1.8g石墨和C60的混合物中,碳原子数目为 0.15NA
D.标准状况下,22.4 L CCl4中含有的共用电子对数目为 4NA
查看答案和解析>>
科目:高中化学 来源:2015届湖北省高三上学期起点考试化学试卷(解析版) 题型:选择题
类比推理的方法在化学学习与研究中有广泛的应用,但有时会得出错误的结论。以下几种类比推理结论中正确的是( )
A.H2SO4为强酸,推出HClO4为强酸
B.Fe3Cl8可以改写为FeCl2·2FeCl3,推出Fe3I8可以改写为FeI2·2FeI3
C.NH3的沸点高于PH3,推出CH4沸点高于SiH4
D.CO2通入Ba(NO3)2溶液中无沉淀生成,推出SO2通入Ba(NO3)2溶液中无沉淀生成
查看答案和解析>>
科目:高中化学 来源:2015届浙江省温州市十校联合体高二下学期期中联考化学试卷(解析版) 题型:填空题
某有机物A含有C、H、O三种元素,其蒸气密度是相同条件下H2密度的29倍,把1.16g该有机物在O2中充分燃烧,将生成物通过足量碱石灰,碱石灰增重3.72g,又知生成的CO2和H2O的物质的量之比为1:1 。
(1)有机物A的分子式
(2)该有机物的红外光谱显示该分子是有一个羟基,无甲基的链状结构,请写出A的结构简式 。
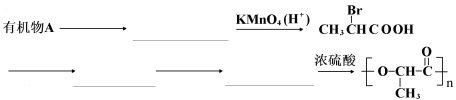
(3)已知聚乳酸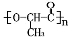 是一种很有前途的可降解高分子材料,可制成袋子替代日常生活中的大部分塑料袋。请完成以有机物A为原料合成聚乳酸的路线(无机试剂任选)
是一种很有前途的可降解高分子材料,可制成袋子替代日常生活中的大部分塑料袋。请完成以有机物A为原料合成聚乳酸的路线(无机试剂任选)

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com