
(15分) 【化学 ― 选修 3 物质结构与性质】
氮的化合物在无机化工领域有着重要的地位。请回答下列问题:
(1)基态氮原子的价电子排布图为 。
(2)氮的最高价氧化物为无色晶体,它由两种离子构成:已知其阴离子构型为平面正三角形,则其阳离子的构型为 形,阳离子中氮的杂化方式为 。
(3)某氮铝化合物X具有耐高温、抗冲击、导热性好等优良性质,广泛用于陶瓷工业等领域。工业上用氮气、氧化铝和碳在一定条件下反应生成CO和X (X的晶体结构如图所示),工业制备 X 的化学方程式为 。
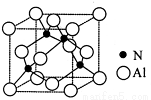
(4)X晶体中包含的化学键类型为 (填字母标号)。
A .离子键 B .共价键 C .配位键 D .金属键
(5)已知氮化硼与X晶体类型相同,且氮化硼的熔点比X高,其原因 是 。
(6)若X的密度为ρg/cm3,则晶体中最近的两个Al 原子的距离为 cm (阿伏加德罗常数用 NA表示,不必化简)。
(1)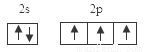 ;(2)直线,sp;(3)Al2O3+N2+3C
;(2)直线,sp;(3)Al2O3+N2+3C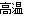 2AlN+3CO;(4)BC;(5)氮化硼与氮化铝均为原子晶体,且硼原子半径小于铝原子半径,B—N键键能大于Al—N键键能;
2AlN+3CO;(4)BC;(5)氮化硼与氮化铝均为原子晶体,且硼原子半径小于铝原子半径,B—N键键能大于Al—N键键能;
(6)
【解析】
试题分析:(1)7号元素N的基态氮原子的价电子排布图为 ;(2)氮的最高价氧化物为无色晶体,它由两种离子构成:已知其阴离子构型为平面正三角形,则其阳离子的构型为直线形;阳离子中氮的杂化方式为sp杂化;(3)某氮铝化合物X具有耐高温、抗冲击、导热性好等优良性质,广泛用于陶瓷工业等领域。工业上用氮气、氧化铝和碳在一定条件下反应生成CO和X (X的晶体结构如图所示),工业制备 X 的化学方程式为Al2O3+N2+3C
;(2)氮的最高价氧化物为无色晶体,它由两种离子构成:已知其阴离子构型为平面正三角形,则其阳离子的构型为直线形;阳离子中氮的杂化方式为sp杂化;(3)某氮铝化合物X具有耐高温、抗冲击、导热性好等优良性质,广泛用于陶瓷工业等领域。工业上用氮气、氧化铝和碳在一定条件下反应生成CO和X (X的晶体结构如图所示),工业制备 X 的化学方程式为Al2O3+N2+3C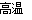 2AlN+3CO;(4)根据X晶体结构示意图可知:在X中包含的化学键类型为共价键、配位键,因此选项是B、C. (5)已知氮化硼与X晶体类型相同,且氮化硼的熔点比X高,其原因是氮化硼与氮化铝均为原子晶体,且硼原子半径小于铝原子半径,B—N键键能大于Al—N键键能,断裂共价键消耗的能量高;(6)若X的密度为ρg/cm3,在晶体中最近的两个Al 原子的距离为晶胞的面对角线的一半,在每个晶胞中含有Al:8×1/8+6×1/3=4;含有N:4个,即在一个晶胞中含有4个AlN,根据密度计算公式ρ=
2AlN+3CO;(4)根据X晶体结构示意图可知:在X中包含的化学键类型为共价键、配位键,因此选项是B、C. (5)已知氮化硼与X晶体类型相同,且氮化硼的熔点比X高,其原因是氮化硼与氮化铝均为原子晶体,且硼原子半径小于铝原子半径,B—N键键能大于Al—N键键能,断裂共价键消耗的能量高;(6)若X的密度为ρg/cm3,在晶体中最近的两个Al 原子的距离为晶胞的面对角线的一半,在每个晶胞中含有Al:8×1/8+6×1/3=4;含有N:4个,即在一个晶胞中含有4个AlN,根据密度计算公式ρ=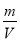 可得V=m÷ρ=
可得V=m÷ρ=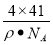 .所以晶胞的边长L=
.所以晶胞的边长L= .则晶体中最近的两个Al 原子的距离为a=
.则晶体中最近的两个Al 原子的距离为a= .
.
考点:考查物质结构、原子的杂化方式、物质制取方程式的书写、晶体中原子之间的距离、物质熔点的比较的知识。


 金钥匙试卷系列答案
金钥匙试卷系列答案科目:高中化学 来源:2015届湖南省高三第一次月考化学试卷(解析版) 题型:选择题
用98%的浓H2SO4(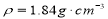 )配制 1mol/L的稀硫酸100mL,按配制溶液时仪器的选用顺序排列,选择正确的是( )
)配制 1mol/L的稀硫酸100mL,按配制溶液时仪器的选用顺序排列,选择正确的是( )
① 玻璃棒 ② 胶头滴管 ③ 100mL容量瓶 ④ 托盘天平 ⑤ 50mL烧杯 ⑥10mL量筒
⑦ 100mL量筒 ⑧ 移液管 ⑨ 滴定管
A.⑥③⑧⑤①② B.⑥⑤③①⑨② C.④⑤③②①⑨ D.⑥⑤①③②
查看答案和解析>>
科目:高中化学 来源:2015届湖北省高三上学期起点考试化学试卷(解析版) 题型:选择题
已知一定条件下A、B、C、D之间的转化关系如下图所示。下列说法正确的是
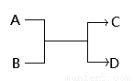
A.若A为Fe,D为氢气,则B一定为酸
B.若A、D为化合物,B为水,则C一定是气体单质
C.若A、B、C、D均为化合物,该反应一定属于复分解反应
D.若A、B、C、D均为10电子微粒,且C是可使湿润的红色石蕊试纸变蓝的气体,则D常温下一定呈液态
查看答案和解析>>
科目:高中化学 来源:2015届湖北省襄阳市四校高二下学期期中联考化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.若把H2S分子写成H3S分子,违背了共价键的饱和性
B.晶体中若有阳离子一定有阴离子
C.金属键存在于任何含金属元素的物质中
D.晶体中一定存在化学键
查看答案和解析>>
科目:高中化学 来源:2015届湖北省襄阳市四校高二下学期期中联考化学试卷(解析版) 题型:选择题
美国科学家合成了含有N5+的盐类,含有该离子的盐是高能爆炸物质,该离子的结构呈“V”形,如图所示。以下有关该物质的说法中正确的是( )
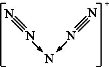
A.每个N5+中含有35个质子和36个电子
B.该离子中有非极性键和配位键
C.该离子中含有2个π键
D.与PCl4+互为等电子体
查看答案和解析>>
科目:高中化学 来源:2015届湖北省新高三起点调研测试化学试卷(解析版) 题型:实验题
( 9分)重铬酸钾(K2Cr2O7)是重要氧化剂,重铬酸钾的溶解度受温度影响较大,工业上常用铬铁矿(主要成分为FeO?Cr2O3,杂质为SiO2?Al2O3)为原料生产它。实验室模拟工业上用铬铁矿制 K2CrO7的主要工艺流程如下图。涉及“碱熔”的主要反应为:
6 FeO?Cr2O3 + 24NaOH + 7KC1O3 = 12NaCrO4 + 3Fe2O3 + 7KCl + 12H2O
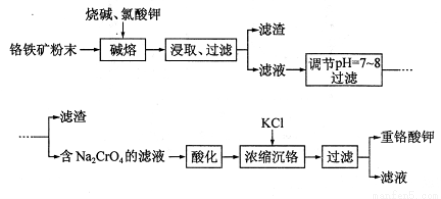
(1)使用粉末状铬铁矿的目的是 。
(2)调节pH后,过滤得到的滤渣是 (填化学式)。
(3)酸化Na2CrO4溶液时,其平衡转化的离子方程式为 。
(4)称取重铬酸钾试样2.500g配成500mL溶液,取出25.00mL于锥形瓶中,加入10 mL2mol/LH2SO4和足量碘化钾(铬的还原产物为Cr3+),放于暗处5min。然后加入100 mL 水,加人3mL淀粉溶液(作指示剂),用0.1200 mol/LNa2S2O3标准溶液滴定( I2 + 2S2O2- 3= 2I-+S4O2- 6),用去20.00mL ,则该样品的纯度为 。
查看答案和解析>>
科目:高中化学 来源:2015届湖北省新高三起点调研测试化学试卷(解析版) 题型:选择题
下列有关实验装置的说法中正确的是
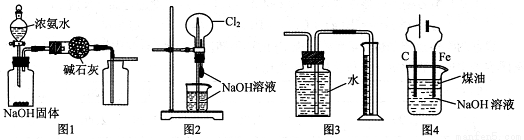
A.图1装置可制取干燥纯净的NH3
B.图2装置可以完成“喷泉”实验
C.图3装置可测量Cu 与浓硝酸反应产生气体的体积
D.图4装置可用于实验室制备Fe (OH)2
查看答案和解析>>
科目:高中化学 来源:2015届湖北省高三上学期起点考试化学试卷(解析版) 题型:选择题
镍镉(Ni—Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为 KOH溶液,其充、放电按下式进行:Cd + 2NiOOH + 2H2O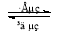 Cd(OH)2 + 2Ni(OH)2
Cd(OH)2 + 2Ni(OH)2
有关该电池的说法正确的是( )
A.充电过程是化学能转化为电能的过程
B.放电时电解质溶液中的OH-向正极移动
C.充电时阳极反应:Ni(OH)2 -e— + OH- == NiOOH + H2O
D.放电时负极附近溶液的碱性不变
查看答案和解析>>
科目:高中化学 来源:2015届浙江省协作体高考摸底测试理科综合化学试卷(解析版) 题型:选择题
已知:常温下浓度为0.1 mol·L-1的下列溶液的pH如表:
溶质 | NaF | NaClO | Na2CO3 |
pH | 7.5 | 9.7 | 11.6 |
下列有关说法正确的是( )。
A.在相同温度下,同浓度的三种酸溶液的导电能力顺序:H2CO3<HClO<HF
B.若将CO2 通入0.1 mol·L-1Na2CO3溶液中至溶液中性,则溶液中
2 c (CO32ˉ)+ c (HCO3ˉ)= 0.1 mol·L-1
C.根据上表, 水解方程式ClOˉ+ H2O HClO + OHˉ的平衡常数K≈10ˉ7.6
HClO + OHˉ的平衡常数K≈10ˉ7.6
D.向上述NaClO 溶液中通HF气体至恰好完全反应时:
c(Na+)>c(Fˉ)>c(H+)>c(HClO)>c(OHˉ)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com