
镍镉(Ni—Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为 KOH溶液,其充、放电按下式进行:Cd + 2NiOOH + 2H2O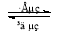 Cd(OH)2 + 2Ni(OH)2
Cd(OH)2 + 2Ni(OH)2
有关该电池的说法正确的是( )
A.充电过程是化学能转化为电能的过程
B.放电时电解质溶液中的OH-向正极移动
C.充电时阳极反应:Ni(OH)2 -e— + OH- == NiOOH + H2O
D.放电时负极附近溶液的碱性不变
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2015届湖北省高三上学期起点考试化学试卷(解析版) 题型:填空题
(8分)氢氧化钾是重要的工业产品。请回答:
(1)铝与氢氧化钾溶液反应的离子方程式是 。
(2)工业品氢氧化钾的溶液中含有某些含氧酸根杂质,可用离子交换膜法电解提纯。电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示。
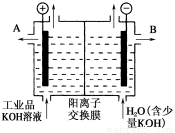
①该电解槽的阳极反应式是 。
②通电开始后,阴极附近溶液pH会增大,请简述原因: 。
③除去杂质后的氢氧化钾溶液从液体出口 (填写“A”或“B”)导出。
查看答案和解析>>
科目:高中化学 来源:2015届湖北省新高三起点调研测试化学试卷(解析版) 题型:填空题
(15分) 【化学 ― 选修 3 物质结构与性质】
氮的化合物在无机化工领域有着重要的地位。请回答下列问题:
(1)基态氮原子的价电子排布图为 。
(2)氮的最高价氧化物为无色晶体,它由两种离子构成:已知其阴离子构型为平面正三角形,则其阳离子的构型为 形,阳离子中氮的杂化方式为 。
(3)某氮铝化合物X具有耐高温、抗冲击、导热性好等优良性质,广泛用于陶瓷工业等领域。工业上用氮气、氧化铝和碳在一定条件下反应生成CO和X (X的晶体结构如图所示),工业制备 X 的化学方程式为 。
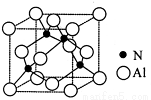
(4)X晶体中包含的化学键类型为 (填字母标号)。
A .离子键 B .共价键 C .配位键 D .金属键
(5)已知氮化硼与X晶体类型相同,且氮化硼的熔点比X高,其原因 是 。
(6)若X的密度为ρg/cm3,则晶体中最近的两个Al 原子的距离为 cm (阿伏加德罗常数用 NA表示,不必化简)。
查看答案和解析>>
科目:高中化学 来源:2015届湖北省新高三起点调研测试化学试卷(解析版) 题型:选择题
NA表示阿伏加德罗常数的值,下列叙述正确的是
A .84gNaHCO3晶体中含有 NA个 CO2- 3
B.0 . lmol/LK2CO3溶液中,阴离子总数大于 0.1NA
C. 1.8g石墨和C60的混合物中,碳原子数目为 0.15NA
D.标准状况下,22.4 L CCl4中含有的共用电子对数目为 4NA
查看答案和解析>>
科目:高中化学 来源:2015届湖北省高三上学期起点考试化学试卷(解析版) 题型:填空题
碳及其化合物有广泛应用。
(1)工业冶炼铝,以石墨为阳极。阳极反应式为 ,可能发生副反应有 。
(2)一氧化碳和空气在酸性介质中构成燃料电池,负极反应式为 。
(3)向75 mL 4 mol?L-1KOH溶液中缓慢通入4480 mL CO2气体(标准状况)恰好完全被吸收。①写出该反应的离子方程式: 。(只用一个离子方程式表示)
②该吸收溶液中离子浓度大小排序为 。
(4)已知:① 2H2(g)+O2(g)=2H2O(l) △H1=—571.6kJ?mol-1
② 2CO(g)+O2(g)=2CO2(g) △H2 = —566.0kJ?mol-1
③ CO(g)+2H2(g) CH3OH(g) △H3 = —90.8kJ?mol-1
CH3OH(g) △H3 = —90.8kJ?mol-1
计算甲醇蒸气的燃烧热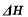 = 。
= 。
(5)某温度下,发生可逆反应:CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g) 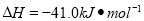
①向某容器中充入1.0 molH2和1.0 molCO2(g),在一定条件下发生上述反应。混合气体中CO的物质的量与时间关系如下列所示:
| 0 | 5 min | 10 min | 15 min | 20 min | 25 min |
I(800℃) | 1.0 | 0.80 | 0.70 | 0.65 | 0.50 | 0.50 |
II(800℃) | 1.0 | 0.7 | 0.60 | 0.50 | 0.50 | 0.50 |
相对实验I,实验II可能改变的条件可能是 ,该温度下,平衡常数= 。
②若开始向绝热容器中投入一定量二氧化碳、氢气在一定条件下发生上述可逆反应。
下列图像正确且说明可逆反应达到平衡状态的是 。(填序号)
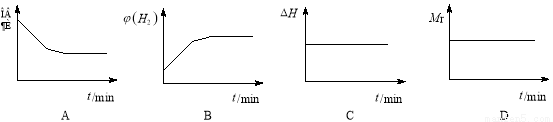
查看答案和解析>>
科目:高中化学 来源:2015届湖北省高三上学期起点考试化学试卷(解析版) 题型:选择题
类比推理的方法在化学学习与研究中有广泛的应用,但有时会得出错误的结论。以下几种类比推理结论中正确的是( )
A.H2SO4为强酸,推出HClO4为强酸
B.Fe3Cl8可以改写为FeCl2·2FeCl3,推出Fe3I8可以改写为FeI2·2FeI3
C.NH3的沸点高于PH3,推出CH4沸点高于SiH4
D.CO2通入Ba(NO3)2溶液中无沉淀生成,推出SO2通入Ba(NO3)2溶液中无沉淀生成
查看答案和解析>>
科目:高中化学 来源:2015届湖北省高三上学期起点考试化学试卷(解析版) 题型:选择题
化学与生活、社会密切相关。下列说法不正确的是( )
A.光导纤维导电能力很强,是一种很好的通讯材料
B.纯碱不仅有较强的去油污能力,还可以用于中和发酵面团中的酸性物质
C.煤的气化和液化都属于化学变化
D.钛被誉为“太空金属”,室温下不与水、稀硫酸、稀硝酸反应,却溶于氢氟酸,可能是因为氟离子易与钛离子形成可溶性难电离物质
查看答案和解析>>
科目:高中化学 来源:2015届湖北省孝感市七校联考高二下学期期中考试化学试卷(解析版) 题型:选择题
已知X、Y元素同周期,且电负性X>Y,下列说法错误的是
A.X与Y形成化合物时,X显负价,Y显正价
B.第一电离能Y一定小于X
C.最高价含氧酸的酸性:X对应的酸性强于Y对应的酸性
D.气态氢化物的稳定性:HmY小于HmX
查看答案和解析>>
科目:高中化学 来源:2015届浙江省温州市十校联合体高三上学期期初联考化学试卷(解析版) 题型:填空题
(12分)甲醇可作为燃料电池的原料。以CH4和H2O为原料,通过下列反应来制备甲醇。
I: CH4(g)+H2O(g)=CO(g) + 3H2(g) △H =+206.0 kJ·mol-1
II:CO(g)+2H2(g)=CH3OH (g) △H =-129.0 kJ·mol-1
(1)CH4(g)与H2O(g)反应生成CH3OH (g)和H2(g)的热化学方程式为 。
(2)将1.0 mol CH4和2.0 mol H2O ( g )通入容积为10 L的反应室,在一定条件下发生反应I,测得在一定的压强下CH4的转化率与温度的关系如下图。
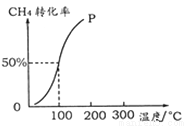
①假设100 ℃时达到平衡所需的时间为5 min,则用H2表示该反应的平均反应速率为 。
②100℃时反应I的平衡常数为 。
(3)在压强为0.1 MPa、温度为300℃条件下,将a mol CO与3a mol H2的混合气体在催化剂作用下发生反应II生成甲醇,平衡后将容器的容积压缩到原来的l/2,其他条件不变,对平衡体系产生的影响是 (填字母序号)。
A.c ( H2 )减少 B.正反应速率加快,逆反应速率减慢
C.CH3OH 的物质的量增加 D.重新平衡c ( H2 )/ c (CH3OH )减小
E.平衡常数K增大
(4)甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是:通电后,将Co2+氧化成Co3+,然后以Co3+ 做氧化剂把水中的甲醇氧化成CO2而净化。实验室用下图装置模拟上述过程:
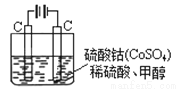
① 写出阳极电极反应式 。
② 写出除去甲醇的离子方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com