
【题目】氮的化合物应用广泛,但氮氧化物是重要的空气污染物,应降低其排放。
(1)用CO2和NH3可合成氮肥尿素[CO(NH3)2]
已知:①2NH3(g)+CO2(g)=NH2CO2NH4 (s) △H=-159.5 kJ·mol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) △H=+116.5 kJ·mol-1
③H2O(l)=H2O(g) △H=+44 kJ·mol-1
用CO2和NH3合成尿素(副产物是液态水)的热化学方程式为______________。
(2)工业上常用如下反应消除氮氧化物的污染:
CH4(g)+2NO2(g)![]() N2(g)+CO2(g)+2H2O(g) △H
N2(g)+CO2(g)+2H2O(g) △H
在温度为T1和T2时,分别将0.40molCH4和1.0molNO2充入体积为1L的密闭容器中,n(CH4)随反应时间的变化如右图所示:
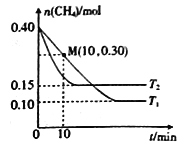
①根据右图判断该反应的△H________0(填“>”、“<”或“=”),理由是______________。
②温度为T1时,0~10min内NO2的平均反应速率v(NO2)=__________,反应的平衡常数K=___(保留三位小数)
③该反应达到平衡后,为在提高反应速率同时提高NO2的转化率,可采取的措施有______(填标号)。
A.改用高效催化剂 B.升高温度
C.缩小容器的体积 D.增加CH4的浓度
(3)利用原电池反应可实现NO2的无害化,总反应为6NO2+8NH3=7N2+12H2O,电解质溶液为NaOH溶液,工作一段时间后,该电池正极区附近溶液pH________(填“增大”、“减小”或“不变”),负极的电极反应式为___________________。
(4)氮的一种氢化物HN3,其水溶液酸性与醋酸相似,则NaN3溶液中各离子浓度由大到小的顺序为________;常温下,将amol·L-1 的HN3与bmol·L-1 的Ba(OH) 2溶液等体积混合,充分反应后,溶液中存在2c(Ba2+)=c(N3-),则该混合物溶液呈_______(填“酸”、“碱”或“中”)性,溶液中c(HN3)=_________ mol·L-1。
【答案】 2NH3(g) +CO2(g)=CO(NH2)2(s)+ H2O (l) < T1<T2,T2时CH4的平衡含量高,说明升高温度,化学平衡向逆反应方向移动,逆反应为吸热反应 0.02 mol ·L-1·min-1 2.025 D 增大 2NH3-6e-+6OH-=N2 + 6H2O c(Na+)>c(N3﹣)>c(OH-)>c(H+) 中 (![]() -b)
-b)
【解析】(1)本题考查盖斯定律的应用,目标反应是CO2+2NH3=CO(NH2)2+H2O,即①+②-③得出2NH3(g) +CO2(g)=CO(NH2)2(s)+ H2O (l) ;(2)考查影响化学平衡移动的因素、化学反应速率的计算和化学平衡常数的计算,①先达到平衡说明反应速率快,即T2>T1,随着温度的升高,甲烷的物质的量增加,说明升高温度,平衡向逆反应方向移动,即正反应方向△H<0;②前10s,消耗甲烷的物质的量为(0.4-0.3)mol=0.1mol,即消耗NO2的物质的量为2×0.1mol=0.2mol,根据化学反应速率的表达式,v(NO2)=0.2/(1×10)mol/(L·min)=0.02 mol/(L·min), CH4(g)+2NO2(g)![]() N2(g)+CO2(g)+2H2O(g)
N2(g)+CO2(g)+2H2O(g)
起始(mol·L-1)0.4 1 0 0 0
变化: 0.3 0.6 0.3 0.3 0.6
平衡: 0.1 0.4 0.3 0.3 0.6 根据化学平衡常数的定义,K=[c2(H2O)×c(CO2)×c(N2)]/[c2(NO2)×C(CH4)]=(0.62×0.3×0.3)/(0.42×0.1)=2.025;③A、使用催化剂,只加快反应速率,对化学平衡无影响,故A错误;B、正反应方向是放热反应,升高温度平衡向逆反应方向移动,NO2的转化率降低,但化学反应速率加快,故B错误;C、缩小容器的体积,增大压强,平衡向逆反应方向进行,NO2的转化率降低,但反应速率加快,故C错误;D、增加CH4的浓度,平衡向正反应方向移动,NO2的转化率增大,化学反应速率加快,故D正确;(3)本题考查电极反应式的书写,正极上发生还原反应,化合价降低,应是NO2参与反应,因此正极反应式为2NO2+4H2O+8e-=N2+8OH-,c(OH-)增大,pH增大;根据电池反应,负极反应式为2NH3-6e-+6OH-=N2 + 6H2O ;(4)醋酸属于弱酸,HN3也属于弱酸,因此N3-发生水解反应,溶液显碱性,但水解程度微弱,即离子浓度大小顺序是 c(Na+)>c(N3﹣)>c(OH-)>c(H+);根据溶液显电中性,即有2c(Ba2+)+c(H+)=c(OH-)+c(N3-),因为2c(Ba2+)=c(N3-),因此c(OH-)=c(H+),溶液显中性;反应后溶液的溶质为Ba(N3)2和HN3,假设溶液体积为1L,则Ba(N3)2的物质的量为bmol,则HN3的物质的量(a-2b)mol,即c(HN3)=(a-2b)2mol·L-1。


科目:高中化学 来源: 题型:
【题目】某学生在如下图所示装置中用苯和液溴制取溴苯,请根据下列实验步骤完成有关问题:
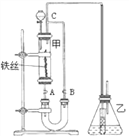
(1)第一步,在分液漏斗中依次加入 10 mL 苯和 5 mL 液溴,使之混合均匀,此时观察到溴溶于苯,不反应,溶液呈深棕红色。
(2)第二步,打开分液漏斗活塞,将苯、溴混合液按一定速率逐滴加入玻 璃管甲中的铁丝上,观察到的现象是剧烈反应,玻璃管甲和导管 C 中有橙红 色 蒸 气 。 从 上 述 两 步 观 察 到 的 现 象 差 异 , 可 得 出 的 结 论 是____________。
(3)第三步,几分钟后,打开胶皮管夹 A 和 B,使反应混合液流入 U 形管中,打开管夹 B 的原因是____________;然后通过分液漏斗向 U 形管中加入适量的NaOH 溶液,目的是(用化学方程式表示)__________。
第四步,关闭胶皮管 A 和 B,连同 A 和 B 一起取下 U 形管,用力振荡并静置后,观察到无色的 溴苯,它在 U 形管中液体的__________填“上”或“下”)层。
(4)要证明上述溴跟苯的反应是取代而不是加成反应,请根据装置乙的作用完成下列各题:
小试管内的液体是____________(填名称)。 锥形瓶内的液体是____________(填名称)。反应后,向锥形瓶内滴加试剂____________(填名称)溶液,作用是____________。
(5)写出上述苯跟溴反应的化学方程式____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.增加反应物的用量一定能增大反应速率
B.化学反应速率只能加快不能减慢
C.决定化学反应速率的主要因素是浓度
D.参加反应物质的性质是决定化学反应速率的主要因素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的SO2(g)和O2(g)分别通入体积为2L的恒容密闭容器中,在不同温度下进行反应:2SO2(g)+ O2(g)![]() 2SO3 △H<0。得到如表中的两组数据,下列说法不正确的是
2SO3 △H<0。得到如表中的两组数据,下列说法不正确的是
实验编号 | 温度/℃ | 平衡常数/mol-1·L | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
SO2 | O2 | SO2 | O2 | ||||
1 | T1 | K1 | 4 | 2 | x | 0.8 | 6 |
2 | T2 | K2 | 4 | 2 | 0.4 | y | t |
A. T1、T2的关系:T1 > T2
B. x= 1.6,y=0.2 ,t<6
C. K1、K2的关系:K2>K1
D. 实验1在前6min的反应速率υ(SO2)=0.2 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是
①标准状况下,1LHCl和1LH2O的物质的量相同;
②标准状况下,11.2 LH2和14gN2所含原子数相同;
③28gCO 的体积约为22.4 L;
④两种物质的物质的量相同,则它们在标准状况下的体积相同;
⑤同温同体积时,气体物质的物质的量越大,则压强越大;
⑥同温同压下,气体的密度与气体的相对分子质量成正比。
A. ⑤⑥ B. ②③⑤⑥ C. ②⑤⑥ D. ①②④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用铁和石墨作电极电解酸性废水,可将废水中的PO43-以FePO4(不溶于水)的形式除去,其装置如图所示。
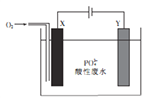
下列说法正确的是
A. 若X、Y电极材料连接反了,则仍可将废水中的PO43-除去
B. X极为石墨,该电极上发生氧化反应
C. 电解过程中Y极周围溶液的pH减小
D. 电解时废水中会发生反应:4Fe2++02-4H++4P043-=4FePO4↓+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2和H2的混和气体加热到1023K时,可建立下列平衡:CO2+H2![]() CO+H2O(g),在该温度下,平衡时有90%的氢气变成水蒸气(平衡常数K=1),则原混合气体中CO2和H2的分子数之比是( )
CO+H2O(g),在该温度下,平衡时有90%的氢气变成水蒸气(平衡常数K=1),则原混合气体中CO2和H2的分子数之比是( )
A. 9:1 B. 1:5 C. 1:10 D. 1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铅蓄电池是典型的可充型电池,电池总反应式为:Pb+PbO2+4H++2SO42-![]() 2PbSO4+2H2O,下列说法正确的是( )
2PbSO4+2H2O,下列说法正确的是( )
A. 放电时,负极的电极反应式是 : PbO2+2e-+4H++SO42-=PbSO4+2H2O
B. 放电时,电解液中H2SO4的浓度将不变
C. 充电时,当外电路通过1mol电子时,原负极板的质量理论上减少48g。
D. 充电时,阳极电极反应式为:PbSO4+2e-=Pb+SO42-,
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的铁粉加入100mL稀硫酸中,为中和过量硫酸,且使Fe2+完全转化为Fe(OH)2,共消耗掉2mol·L-1NaOH溶液150mL。原硫酸溶液的浓度是
A. 0.5mol·L-1 B. 1mol·L-1 C. 1.5mol·L-1 D. 2mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com