
【题目】如图所示是实验室制取SO2并验证SO2某些性质的装置图,试回答:
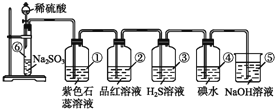
(1)⑥中发生反应的化学方程式为___;
(2)①中实验现象为___,证明SO2是___气体;
(3)②中品红溶液___,证明SO2有___;
(4)③中现象是___,写出SO2与H2O2的化学方程式___;
(5)④中现象是___,证明SO2有___性;
(6)⑤的作用是___,反应的化学方程式为___。
【答案】Na2SO3+H2SO4=Na2SO4+SO2↑+H2O 紫色石蕊溶液变红 酸性 褪色 漂白性 有淡黄色沉淀生成 SO2+H2O2=H2SO4 溶液褪色 溶液褪色 吸收多余的SO2,防止污染空气 2NaOH+SO2=Na2SO3+H2O
【解析】
根据图中反应装置中的反应物的性质书写相关反应方程式;根据实验装置图及实验现象分析二氧化硫的性质,并书写相关反应方程式。
(1)⑥中为亚硫酸钠和稀硫酸反应生成二氧化硫气体,反应的化学方程式为:Na2SO3+H2SO4=Na2SO4+SO2↑+H2O,故答案为:Na2SO3+H2SO4=Na2SO4+SO2↑+H2O;
(2)①中为紫色石蕊试液,二氧化硫溶于水和水反应生成亚硫酸,![]() ,亚硫酸为弱酸,可以使紫色石蕊试液变红,故答案为:紫色石蕊溶液变红;酸性;
,亚硫酸为弱酸,可以使紫色石蕊试液变红,故答案为:紫色石蕊溶液变红;酸性;
(3)②中为品红溶液,二氧化硫与品红化合生成无色物质,能使品红溶液褪色,故二氧化硫具有漂白性,故答案为:褪色;漂白性;
(4)③中![]() 中
中![]() 价S具有氧化性,硫化氢中-2价S具有还原性,二氧化硫能把硫化氢氧化成单质硫,本身被还原成单质硫,反应方程式为SO2+2H2S=3S↓+2H2O,所以③中现象是有淡黄色沉淀生成,过氧化氢具有氧化性,
价S具有氧化性,硫化氢中-2价S具有还原性,二氧化硫能把硫化氢氧化成单质硫,本身被还原成单质硫,反应方程式为SO2+2H2S=3S↓+2H2O,所以③中现象是有淡黄色沉淀生成,过氧化氢具有氧化性,![]() 与
与![]() 反应,二氧化硫具有还原性,两者反应:
反应,二氧化硫具有还原性,两者反应:![]() ,故答案为:有淡黄色沉淀生成;
,故答案为:有淡黄色沉淀生成;![]() ;
;
(5)④中碘水具有氧化性,溶液颜色为紫红色,![]() 中
中![]() 价S具有还原性,两者发生:
价S具有还原性,两者发生:![]() ,溶液褪色,该反应中二氧化硫为还原剂,具有还原性,故答案为:溶液褪色;还原;
,溶液褪色,该反应中二氧化硫为还原剂,具有还原性,故答案为:溶液褪色;还原;
(6)⑤二氧化硫有毒,不能直接排放到空气中,二氧化硫酸性氧化物能够与氢氧化钠反应生成亚硫酸钠和水,所以可以用氢氧化钠溶液吸收二氧化硫,反应的化学方程式为:![]() ,故答案为:吸收多余的
,故答案为:吸收多余的![]() ,防止污染空气;
,防止污染空气;![]() 。
。


科目:高中化学 来源: 题型:
【题目】实验室制取Cl2的化学方程式为MnO2+ 4HCl![]() MnCl2+ Cl2↑+ 2H2O,当有146.0克HCl完全参加反应时,有多少摩尔氧化剂被还原?有多少摩尔还原剂被氧化?还原产物为多少克?生成的氧化产物在标准状况下的体积是多少升?(每问3 分)
MnCl2+ Cl2↑+ 2H2O,当有146.0克HCl完全参加反应时,有多少摩尔氧化剂被还原?有多少摩尔还原剂被氧化?还原产物为多少克?生成的氧化产物在标准状况下的体积是多少升?(每问3 分)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铍铜是广泛应用于制造高级弹性元件的良好合金。某科研小组从某度旧铍铜元件(含25%BeO、71%CuS、少量FeS和SiO2)中回收铍和铜两种金属的工艺流程如下:

已知:I.铍、铝元素化学性质相似;
Ⅱ.常温下部分难溶物的溶度积常数如下表:

(1)滤液A的主要成分除NaOH外,还有_____________(填化学式),写出反应I中含铍化合物与过量盐酸反应的离子方程式:_______________________________________________。
(2)①滤液C中含NaCl、BeCl2和少量HCl,为提纯BeCl2,最合理的实验步骤顺序为_______(填字母)
a.加入过量的氨水 b.通入过量的CO2
c.加入过量的NaOH d.加入适量的HCl e.洗涤 f.过滤
(3)MnO2能将金属硫化物中的硫元素氧化为硫单质.写出反应Ⅱ中CuS发生反应的化学方程式:____________________________________________。
(4)滤液D中c(Cu2+)=2.2mol·L-1、c(Fe3+)=0.008mol·L-1、c(Mn2+)=0.01mol·L-1,逐滴加入稀氨水调节pH可将其依次分离,首先沉淀的是___________(填离子符号),为使铜离子开始沉淀,常温下应调节溶液的pH大于___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上利用氨氧化获得的高浓度NOx气体(含NO、NO2)制备NaNO2、NaNO3,工艺流程如下: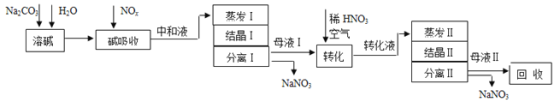
已知:Na2CO3+NO+NO2=2NaNO2+CO2
(1)中和液所含溶质除NaNO2及少量Na2CO3外,还有__________(填化学式)。
(2)中和液进行蒸发Ⅰ操作时,应控制水的蒸发量,避免浓度过大,目的是_______。蒸发Ⅰ产生的蒸气中含有少量的NaNO2等有毒物质,不能直接排放,将其冷凝后用于流程中的_______(填操作名称)最合理。
(3)母液Ⅰ进行转化时加入稀HNO3的目的是_______。母液Ⅱ需回收利用,下列处理方法合理的是________。
a.转入中和液 b.转入结晶Ⅰ操作
c.转入转化液 d.转入结晶Ⅱ操作
(4)若将NaNO2、NaNO3两种产品的物质的量之比设为2:1,则生产1.38吨NaNO2时,Na2CO3的理论用量为______吨(假定Na2CO3恰好完全反应)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验过程中,下列溶液的导电能力变化不大的是
A. ![]() 溶液中滴入
溶液中滴入![]() 溶液至过量
溶液至过量
B. 醋酸溶液中滴入氨水至过量
C. 澄清石灰水中通入![]() 至过量
至过量
D. ![]() 溶液中加入适量的NaOH固体
溶液中加入适量的NaOH固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 分子式为C2H6O的有机化合物性质相同
B. 相同条件下,等质量的碳按a、b两种途径完全转化,途径a比途径b放出更多热能途径a:![]() ,途径b:
,途径b:![]()
C. 在氧化还原反应中,还原剂失去电子总数等于氧化剂得到电子的总数
D. 通过化学变化可以直接将水转变为汽油
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍的抗腐蚀性佳,主要用于合金和电镀,也可用作良好的催化剂。现准确称量8g粗镍(含有少量Fe、Cu以及难与酸、碱反应的杂质)进行如下提纯。
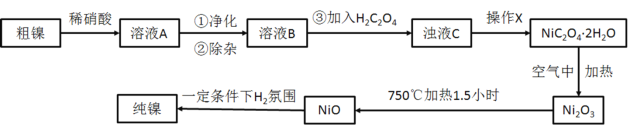
请回答下列问题:
(1)写出稀硝酸溶解镍的离子方程式___。
(2)在溶液A的净化除杂中,首先将溶液A煮沸,调节pH=5.5,继续加热煮沸5min,加热过程中补充适量的水保持溶液的体积不变,静止一段时间后,过滤出Fe2O3、FeO(OH)。
①写出煮沸过程中生成FeO(OH)的离子方程式___。
②控制溶液的pH,可利用___。
a.pH试纸 b.石蕊指示剂 c.pH计
③为了得到纯净的溶液B,还需要加入以下物质___(填字母)进行除杂。(已知:Ksp(CuS)=8.8×10-36;Ksp(NiS)=3.2×10-19;Ksp[Cu(OH)2]=2.2×10-20;Ksp[Ni(OH)2]=5.4×10-16)
a.NaOH b.Na2S C.H2S d.NH3·H2O
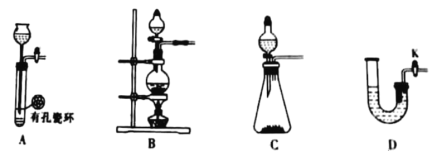
(3)在快速搅拌下缓慢向溶液B中滴加12%的H2C2O4溶液,溶液中即可析出NiC2O4·2H2O,搅拌下煮沸2min冷却。操作X包括:过滤、洗涤和烘干,采用如图的装置进行过滤(备注:该图是一个通过水泵减压过滤的装置)。这种抽滤其优点是___,装置B的主要作用是___,若实验过程中发现倒吸现象,应采取的措施是___。
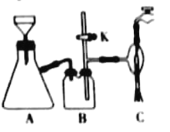
(4)在该生产过程中需要纯净的H2。若实验室要制备纯净的H2,发生装置不可以选择___(选填代号)。
(5)用电子天平称取0.5000g的NiO样品,加入一定体积的6mol/L的盐酸恰好完全溶解,将所得到的溶液配制成250mL的溶液。取出20mL加入锥形瓶,按照如下滴定原理进行沉淀滴定,最终得到干燥的固体mg,则镍元素的质量分数为___。(写出表达式即可)
[一定条件下丁二酮肟(![]() ,简写为C4N2H8O2)能和Ni2+反应生产鲜红色的沉淀,其方程式为:Ni2++2C4N2H8O2+2NH3·H2O=Ni(C4N2H7O2)2↓+2NH4++2H2O,Ni(C4N2H7O2)2的摩尔质量为289g/mol]。Ni2+能与CO32-、C2O42-、S2-等离子形成沉淀,但为什么很多情况下选用丁二酮肟有机沉淀剂?___。
,简写为C4N2H8O2)能和Ni2+反应生产鲜红色的沉淀,其方程式为:Ni2++2C4N2H8O2+2NH3·H2O=Ni(C4N2H7O2)2↓+2NH4++2H2O,Ni(C4N2H7O2)2的摩尔质量为289g/mol]。Ni2+能与CO32-、C2O42-、S2-等离子形成沉淀,但为什么很多情况下选用丁二酮肟有机沉淀剂?___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常用(NH4)2SO3溶液吸收废气中的SO2,室温下测得溶液中lgY[Y=![]() 或
或![]() ],与pH的变化关系如图所示。则下列说法一定错误的是( )
],与pH的变化关系如图所示。则下列说法一定错误的是( )
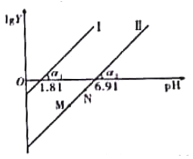
A.通入少量SO2的过程中,直线Ⅱ中的N点向M点移动
B.α1=α2一定等于45°
C.当对应溶液的pH处于1.81<pH<6.91时,溶液中的微粒浓度一定存在c(HSO3-)>c(SO32-)>c(H2SO3)
D.直线Ⅱ中M、N点一定存在c2(HSO3-)>c(SO32-)·c(H2SO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种化合物的结构如图所示,其中X、Y、Z、Q、W为原子序数依次增大的五种短周期主族元素,Q核外最外层电子数与Y核外电子总数相同,X的原子半径是元素周期表中最小的。下列叙述正确的是

A.WX的水溶液呈碱性
B.元素非金属性的顺序为:Y>Z>Q
C.由X、Y、Q、W四种元素形成的化合物的水溶液一定呈碱性
D.该化合物中与Y单键相连的Q不满足8电子稳定结构
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com