
���� ����Һ�ܸ���������Ӧ�ų�H2��Ϊ�����������ǿ����Һ����������֮�䲻�ܽ�����ɳ��������塢ˮ�ȣ����ܷ���������ԭ��Ӧ�ȣ������Ӵ������棬�Դ������
��� �⣺����Һ�ܸ���������Ӧ�ų�H2��Ϊ�����������ǿ����Һ��
��1��������Al3+ʱ����Һ�����ԣ��������ӷ�Ӧ�IJ��ܴ���SO32-��CO32-��OH -��Cu2+Ϊ��ɫ���ɵ���غ��֪������һ������Cl-���ܸ���������Ӧ�ų�����һ������H+�����ܴ���Ag+���ɴ��ڵ�����ΪMg2+��Ba2+��
�ʴ�Ϊ��Cl-��H+��Mg2+��Ba2+��
��2��������AlO2-ʱ����Һ�Լ��ԣ������������ӷ�Ӧ��Mg2+��Cu2+��H+��Ag+���ܴ��ڣ��ɵ���غ��֪һ������Ba2+������Ba2+��Ӧ��CO32-��SO32-���ܴ��ڣ�����Һ�пɴ���Cl-��
�ʴ�Ϊ��Ba2+��OH-��
���� ���⿼�����ӹ�����жϣ�Ϊ�߿��ĸ�Ƶ�⣬�����е��Ѷȵ����⣬ע����ȷ���Ӳ��ܴ��������һ��������ܷ������ֽⷴӦ������֮�䣻�ܷ���������ԭ��Ӧ������֮�䣻�ܷ�����Ϸ�Ӧ������֮�䣨�� Fe3+�� SCN-���ȣ���Ӧ��ע����Ŀ���������������磺��Һ������ԣ��ݴ����ж���Һ���Ƿ��д����� H+��OH-����Һ����ɫ������ɫʱ���ų� Cu2+��Fe2+��Fe3+��MnO4-����ɫ���ӵĴ��ڣ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Mg�����ᷴӦ | B�� | NH4Cl�ķֽⷴӦ | ||
| C�� | Na��Cl2ȼ�� | D�� | NaOH��Һ��CH3COOH��Һ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 6��8 | B�� | 19��16 | C�� | 12��17 | D�� | 7��8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
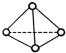 ��ѧ�Ҽ�����˼��������о������N4���ӣ���ṹΪ���������ͣ���ͼ��ʾ����������ÿ����ԭ��������Ӳ㶼����8���ӽṹ����֪����1mol N-N������192kJ����������1mol N-N������946kJ��������������������ȷ���ǣ�������
��ѧ�Ҽ�����˼��������о������N4���ӣ���ṹΪ���������ͣ���ͼ��ʾ����������ÿ����ԭ��������Ӳ㶼����8���ӽṹ����֪����1mol N-N������192kJ����������1mol N-N������946kJ��������������������ȷ���ǣ�������| A�� | 1molN4����ת��ΪN2ʱҪ����206 kJ���� | |
| B�� | N4��һ�ֱ�N2���ȶ��ķ��� | |
| C�� | 1molN4����ת��ΪN2ʱҪ�ų�740 kJ���� | |
| D�� | N4��N2��ͬλ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ҹ��Ŵ����ס��칤������ء���������KNO3������������ʯ�ʣ��༤�����������ɲ⡱����ΪKNO3����ȼ | |
| B�� | �ô�����Һ�����������ϴ��¯�е������ | |
| C�� | �����°���������õ�����������Ҷľ��ԭ�ϵ���Ҫ�ɷ�����ά�� | |
| D�� | ����ӫ�⵰���Թ۲ϸ���Ļ��ӫ�⵰����һ�ָ߷��ӻ��������ܷ���ˮ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
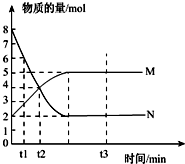 ��1��һ���¶��£����ݻ�ΪV L���ܱ������н��з�Ӧ��aN��g��?bM��g����M��N�����ʵ�����ʱ��ı仯������ͼ��ʾ��
��1��һ���¶��£����ݻ�ΪV L���ܱ������н��з�Ӧ��aN��g��?bM��g����M��N�����ʵ�����ʱ��ı仯������ͼ��ʾ���鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com