
取20 mL NaOH溶液平均分成两份,分别放入A、B两支试管中。向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1mol/L的盐酸,标准状况下产生的CO2气体体积与所加的盐酸溶液体积之间的关系如下表所示:
| 盐酸体积(单位:mL) | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 |
| A产生CO2的体积 | 0 | 0 | 0 | 0 | 0 | 22.4 | 44.8 | 44.8 | 44.8 |
| B产生CO2的体积 | 0 | 0 | 22.4 | 44.8 | 67.2 | 89.6 | x | x | x |
(1)CO2+2OH-=CO32-+H2O;CO2+NaOH=NaHCO3(2)NaOH、Na2CO3(3)0.7(4)112
解析试题分析:(1)CO2与NaOH反应为①CO2+NaOH=NaHCO3,②CO2+2NaOH=Na2CO3+H20,故少量CO2与NaOH溶液反应的离子方程式CO2+2OH-=CO32-+H2O;过量CO2与NaOH溶液反应的化学方程式CO2+NaOH=NaHCO3(2)当n(CO2):n(NaOH)≥1,反应按①进行,等于1时,CO2、NaOH恰好反应生成NaHCO3;大于1时,生成生成NaHCO3,CO2有剩余;当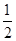 <n(CO2):n(NaOH)<1,反应按①②进行,CO2、NaOH反应,无剩余,生成物为NaHCO3、Na2CO3;当n(CO2):n(NaOH)≤
<n(CO2):n(NaOH)<1,反应按①②进行,CO2、NaOH反应,无剩余,生成物为NaHCO3、Na2CO3;当n(CO2):n(NaOH)≤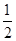 ,反应按②进行,等于
,反应按②进行,等于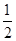 ,时,CO2、NaOH恰好反应生成Na2CO3;小于
,时,CO2、NaOH恰好反应生成Na2CO3;小于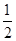 时,生成Na2CO3,NaOH有剩余;,A中通入CO2后所得溶液的溶质为Na2CO3,NaOH(3)加入70ml盐酸时二氧化碳的体积达最大,此时溶液为氯化钠溶液.根据氯离子、钠离子守恒,所以n(NaOH)=n(NaCl)=n(HCl)=0.07ml×0.1mol/L=0.007mol,所以c(NaOH)=
时,生成Na2CO3,NaOH有剩余;,A中通入CO2后所得溶液的溶质为Na2CO3,NaOH(3)加入70ml盐酸时二氧化碳的体积达最大,此时溶液为氯化钠溶液.根据氯离子、钠离子守恒,所以n(NaOH)=n(NaCl)=n(HCl)=0.07ml×0.1mol/L=0.007mol,所以c(NaOH)= 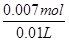 =0.7mol/L,故答案为:0.7mol/L;(4)由曲线B可知从20ml到70ml为碳酸氢钠与盐酸反应生成二氧化碳,反应方程式为NaHCO3+HCl=NaCl+CO2↑+H2O,所以n(CO2)=n(HCl)=(0.07ml-0.02ml)×0.1mol/L=0.005mol,所以CO2气体体积为0.005mol×22.4L/mol=0.112L=112mL,故答案为112。
=0.7mol/L,故答案为:0.7mol/L;(4)由曲线B可知从20ml到70ml为碳酸氢钠与盐酸反应生成二氧化碳,反应方程式为NaHCO3+HCl=NaCl+CO2↑+H2O,所以n(CO2)=n(HCl)=(0.07ml-0.02ml)×0.1mol/L=0.005mol,所以CO2气体体积为0.005mol×22.4L/mol=0.112L=112mL,故答案为112。
考点:化学反应方程式的有关计算


 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案科目:高中化学 来源: 题型:填空题
将一支盛有a mL NO 和b mL NO2气体的试管倒立于水槽中,然后通过a mL O2,请回答以下小题:
(1)若a=b,则充分反应后试管内气体体积为_________mL。
(2)若a<b,则充分反应后试管内气体体积为_________mL。
(3)若a>b,则充分反应后试管内气体体积为_________mL。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
无机化合物A中含有金属Li元素,遇水强烈水解,主要用于有机合成和药物制造,是具有良好前景的储氢材料。在一定条件下,2.30g固体A与5.35gNH4Cl固体恰好完全反应,生成固体B和4.48L气体C (标准状况)。已知气体C极易溶于水得到碱性溶液, 电解无水B可生成金属单质D和氯气。
回答下列问题:
(1)A的化学式是 , C的电子式是 。
(2)写出化合物A与盐酸反应的化学方程式: 。
(3)某同学通过查阅资料得知物质A的性质:
Ⅰ.工业上可用金属D与液态的C在硝酸铁催化下反应来制备A物质,纯净的A物质为白色固体,但制得的粗品往往是灰色的。
Ⅱ.物质A熔点390℃,沸点430℃,密度大于苯或甲苯,不溶于煤油,遇水反应剧烈,也要避免接触酸和酒精。在空气中化合物A缓慢分解,对其加强热则猛烈分解,但不会爆炸.在750~800℃分解为化合物E和气体C。
①物质A在750~800℃分解的方程式为: 。
②久置的物质A可能大部分变质而不能使用,需将其销毁。遇到这种情况,可用苯或甲苯将其覆盖,然后缓慢加入用苯或甲苯稀释过的无水乙醇,试解释其化学原理 。
(4)工业制备单质D的流程图如下:
①步骤①中操作名称: 。
②试用平衡原理解释步骤②中减压的目的: 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
闪锌矿(主要成份为ZnS)是含锌主要矿物之一,空气中高温加热闪锌矿生成ZnO和SO2。ZnO用于冶炼金属锌,SO2可制亚硫酸盐或硫酸。回答下列问题(以下计算保留2位小数)
(1)取1.56 g闪锌矿样品,在空气中高温加热(杂质不反应),充分反应后,冷却,得到残留
固体的质量为1.32 g,样品中含硫化锌的质量分数是_________。
(2)取1.95 g锌加入到12.00 mL 18.4 mol/L的浓硫酸中(反应中只生成一种还原产物),充分反应后,小心地将溶液稀释到1000 mL,取出15.00 mL,以酚酞为指示剂,用0.25 mol/L的NaOH溶液中和余酸,耗用NaOH溶液的体积为21.70 mL。
①反应后溶液中多余的硫酸是____________ mol。
②通过计算确定浓硫酸被还原的产物是________________________。
(3)将标况下4.48 L SO2气体慢慢通入200 mL一定浓度NaOH溶液中,SO2气体全部被吸收,将反应后的溶液在空气中小心蒸干(不考虑酸式盐的分解),得到不超过两种物质的无水晶体26.8g。通过计算确定所得晶体的成分与物质的量。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
根据下列数据确定元素X的相对原子质量。
(1) 1.01×105 Pa,273 ℃时气态单质Xn的密度为d g/L,则X的相对原子质量为_____。
(2)相同状况下,一定体积的X的气态氢化物HmX的质量是等体积NH3的2倍。则X的相对原子质量为_____。
(3)a个X原子的总质量为b g,则X的相对原子质量可表示为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
向10mLNa2CO3和Na2SO4的混合溶液中加入足量的氯化钡溶液,生成沉淀的质量为6.27g,向所得沉淀中加入足量稀盐酸,沉淀质量减少到2.33g,并放出气体,试计算:
(1)原混合物中Na2SO4的物质的量浓度为 mol?L-1;
(2)在标准状况下产生气体的体积为 L。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
实验室配制500 mL 0.2 mol·L-1的Na2SO4溶液,实验操作步骤有:
A.在天平上称出14.2 g硫酸钠固体,把它放在烧杯中,用适量的蒸馏水使它完全溶解并冷却 至室温。
B.把制得的溶液小心地转移到容量瓶中。
C.继续向容量瓶中加蒸馏水至液面距刻度线1~2 cm处,改用胶头滴管小心滴加蒸馏水至溶液凹液面最低处与刻度线相切。
D.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心注入容量瓶,并轻轻振荡。
E.将容量瓶瓶塞塞紧,充分摇匀后装瓶。
请填写下列空白:
(1)操作步骤的正确顺序为(填序号)____ _。
(2)本实验用到的基本仪器已有烧杯、天平(带砝码、镊子)、玻璃棒,还缺少的仪器是________、________。
(3)下列情况会使所配溶液浓度偏高的是(填序号)______ __。
A.容量瓶使用前内壁沾有水珠 B.没进行上述的操作步骤D
C.加蒸馏水时,不慎超过了刻度线 D.砝码上沾有杂质
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(1)0.5molCH4的质量是 g,在标准状况下的体积为 L;含 有约 个氢原子。
将标准状况下22.4 L的HCl溶于水配成200 mL的溶液,所得溶液的物质的量浓度为 ;配制300 mL 0.5 mol·L-1氯化钠溶液,需要1.5 mol·L-1的氯化钠溶液的体积是 mL。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
0.5mol H2SO4的质量是________g,含______________个分子,含________mol氧原子,能和________mol NaOH完全反应,该硫酸所含氢元素的质量与________g中所含氢元素的质量相同。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com