
【题目】在25 ℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
物质 | X | Y | Z |
初始浓度/(mol·L-1) | 0.1 | 0.2 | 0 |
平衡浓度/(mol·L-1) | 0.05 | 0.05 | 0.1 |
下列说法错误的是:
A. 反应达到平衡时,X的转化率为50%
B. 反应可表示为X+3Y![]() 2Z,其平衡常数为1600
2Z,其平衡常数为1600
C. 增大压强使平衡向生成Z的方向移动,平衡常数增大
D. 改变温度可以改变此反应的平衡常数
【答案】C
【解析】试题分析:A.反应达到平衡时,Y的转化率为:(0.2mol/L0.05mol/L)/0.2mol/L×100%=75%,A错误;B.根据反应速率之比等于浓度变化量之比等于化学计量数之比可知:△c(X):△c(Y):△c(Z)=0.05:0.15:0.1=1:3:2,则反应的方程式为X+3Y![]() 2Z,K=c2(Z)/c(X)c3(Y)=(0.1mol/L)2/(0.05mol/L)×(0.05mol/L)3=1600(mol/L)-2,B正确;C.平衡常数只受温度的影响,压强改变时,化学平衡常数仍然不变,C错误;D.平衡常数只受温度的影响,温度改变时,化学平衡常数一定改变,D正确,答案选C。
2Z,K=c2(Z)/c(X)c3(Y)=(0.1mol/L)2/(0.05mol/L)×(0.05mol/L)3=1600(mol/L)-2,B正确;C.平衡常数只受温度的影响,压强改变时,化学平衡常数仍然不变,C错误;D.平衡常数只受温度的影响,温度改变时,化学平衡常数一定改变,D正确,答案选C。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】对于反应2SO2+O2![]() 2SO3,下列判断正确的是
2SO3,下列判断正确的是
A. 2 mol SO2和5 mol O2充分反应可生成2 mol SO3
B. 2 mol SO2和1mol O2达到化学平衡时SO2、O2、SO3的分子数之比一定为2∶1∶2
C. 达到化学平衡时SO2的消耗速率必定等于O2的生成速率的2倍
D. 三种物质的浓度相等时,说明反应达到了化学平衡。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国古代化学成绩斐然,下列说法错误的是
A. 古代造纸是以木材等为原料,用去除杂质后的纤维素制成的,纤维素属子天然高分子
B. 火药是由硫磺、木炭、硝酸钾按照一定比例混合制得的
C. “China”来源于闻名于世的我国陶瓷,陶瓷是一种硅酸盐产品
D. 司母戊鼎是商朝铸造的青铜器,它是由纯铜制作的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合物X由A12O3、Fe2O3、Cu、SiO2中的一种或几种物质组成。某校课外兴趣小组以两条途径分别对X进行如下实验探究。

下列有关说法不正确的是:
A. 由Ⅰ可知X中一定存在Fe2O3、Cu B. 无法判断,混合物中是否含有Al2O3
C. 原混合物中m(Fe2O3) : m(Cu) = 1:1 D. 1.92g固体成分为Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用氨水吸收烟气中的二氧化硫,其相关反应的主要热化学方程式如下:
SO2(g)+NH3·H2O(aq)=NH4HSO3(aq)△H1=akJ·mol-1
NH3·H2O(aq)+NH4HSO3(aq)=(NH4)2SO3(aq)+H2O(l)△H2=bkJ·mol-1
2(NH4)2SO3(aq)+O2(g)=2(NH4)2SO4(aq)△H3=ckJ·mol-1
⑴反应2SO2(g)+4NH3·H2O(aq)+O2(g)=2(NH4)2SO4(aq)+2H2O(l)的△H=_____kJ·mol-1。
⑵空气氧化(NH4)2SO3的速率随温度的变化如图所示,当温度超过60℃时,(NH4)2SO3氧化速率下降的原因可能是_______。

⑶以磷石膏废渣和碳酸铵为原料制备硫酸铵,不仅解决了环境问题,还使硫资源获得二次利用。反应的离子方程式为CaSO4(s)+CO32—(aq)SO42—(aq)+CaCO3(s),该反应的平衡常数K=____。[已知Ksp(CaCO3)=2.9×10-9,Ksp(CaSO4)=9.1×10-6]
⑷(NH4)2SO4在工农业生产中有多种用途。
①将黄铜精矿(主要成分Cu2S)与硫酸铵混合后在空气中进行焙烧,可转化为硫酸铜同时产生氨气。该反应的化学方程式为________。

②研究硫酸铵的分解机理有利于对磷石膏的开发。在500℃下硫酸铵分解过程中得到4种产物,其含氮物质随时间变化关系如图甲所示。写出该条件下硫酸铵分解的化学方程式,并用单线桥标出电子转移的方向及数目:_____________。
③(NH4)2SO4是工业制备K2SO4的重要原料。根据图乙中相关物质的溶解度曲线,简述工业上制备K2SO4晶体的设计思路:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关垃圾处理的方法不正确的是 ( )
A.垃圾处理常用的方法是卫生填埋、焚烧、堆肥
B.将垃圾分类回收是垃圾处理的发展方向
C.填埋垃圾不需处理,只深埋即可
D.焚烧垃圾产生大量污染空气的物质,故不易采用此方法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】太阳能电池板材料除单品硅外,还有铜、铟、稼、硒、硅等化学物质。
(1)硒、硅与氢元素形成的组成最简单的氢化物中,若“Si-H”中共用电子对偏向氢元素,氢气与硒反应时单质硒是氧化剂,则硒与硅的电负性相对大小为Se____Si(填“>”、“<”)。人们把硅与氢元素形成的一类化合物叫硅烷(SinH2n+2)。硅烷的沸点与相对分子质量的关系如图所示,呈现这种变化的原因是______________。

(2)①已知高温下CuO→Cu2O+O2,从铜原子价层电子结构(3d 和4s轨道上应填充的电子数)变化角度来看,能生成Cu2O的原因是___________。
② 金属Cu单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应,反应的离子方程式为___________________。
③ 铜晶体为面心立方最密堆积,铜的原子半径为127.8pm,计算晶体铜的密度_____g/cm3。
(3)稼的基态原子的电子排布式是_______。与铟、稼元家处于同一主族的硼元素具有缺电子性(价电子数少于价层轨道数),其化合物可与具有孤对电子的分子或离子生成配合物.如BF3能与NH3反应生成BF3·NH3。BF3·NH3中B原子的杂化轨道类型为______,B与N之间形成______键;硼酸(H3BO3)在水溶液中能与水反应生成[B(OH)4]-而体现一元弱酸的性质.其电离方程式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,在体积为2L的恒容密闭容器中,某一反应中X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,下列
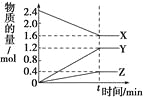
表述中正确的是
A. 反应的化学方程式为2X = 3Y + Z
B. t时,正、逆反应都不再继续进行,反应达到化学平衡
C. 若t=4,则0~t的X的化学反应速率为0.1 molL-1min-1
D. 温度、体积不变,t时刻充入1 mol He使压强增大,正、逆反应速率都增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com