
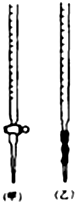
 乙二酸俗名草酸,下面是化学学习小组的同学对草酸晶体(H2C2O4•xH2O)进行的探究性学习的过程,请你参与并协助他们完成相关学习任务.
乙二酸俗名草酸,下面是化学学习小组的同学对草酸晶体(H2C2O4•xH2O)进行的探究性学习的过程,请你参与并协助他们完成相关学习任务.分析 (1)高锰酸钾可氧化橡胶;
(2)高锰酸钾溶液为紫色,滴定终点时溶液显紫色;
(3)结合2MnO4-+5H2C2O4+6H+═2Mn2++10CO2↑+8H2O及H2C2O4•xH2O的质量计算x;
①若滴定终点时俯视滴定管,消耗高锰酸钾溶液的体积偏小;
②若滴定时所用的酸性KMnO4溶液因久置而导致浓度变小,消耗高锰酸钾溶液的体积偏大,以此来解答.
解答 解:(1)KMnO4标准溶液具有强氧化性,应装在酸式滴定管中,选甲,故答案为:甲;
(2)本实验滴定达到终点的标志是:最后一滴高锰酸钾滴入后,锥形瓶内的溶液突然呈现紫色(或紫红色),且半分钟内溶液不褪色,
故答案为:当滴入最后一滴酸性KMnO4溶液时,溶液由无色变为紫色,且半分钟内不褪色,即达滴定终点;
(3)由题给化学方程式及数据可知,1.260g纯草酸晶体中含H2C2O4的物质的量为0.1000 mol/L×10.00 mL×10-3L/mL×5/2×100 mL/25 mL=0.0100 mol,则1.260 g H2C2O4•xH2O中含H2O的物质的量为$\frac{1.260g-0.0100mol×90g/mol}{18g/mol}$=0.0200 mol,则x=2,
故答案为:2;
①若滴定终点时俯视滴定管,则所得消耗酸性KMnO4溶液的体积偏小,由此所得n(H2C2O4)偏小,则n(H2O)偏大,x偏大,故答案为:偏大;
②若滴定时所用的酸性KMnO4溶液因久置而导致浓度变小,则消耗其体积偏大,所得x值偏小,故答案为:偏小.
点评 本题考查物质含量的测定实验,为高频考点,把握仪器的使用、氧化还原反应、实验技能为解答关键,侧重分析与实验能力的考查,注意结合反应计算,题目难度不大.


 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 2个 | B. | 3个 | C. | 4个 | D. | 5个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molN2与4molH2反应生成的NH3分子数为2NA | |
| B. | 14g乙烯和丙烯混合气体中的氢原子数为2NA | |
| C. | 1 molFe溶于过量硝酸,电子转移数为2NA | |
| D. | 标准状况下,2.24LCCl4含有的共价键数为0.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 碱式碳酸铜是一种化工原料,化学式用mCu(OH)2•nCuCO3表示.实验室以废铜屑为原料制取碱式碳酸铜的步骤如下:
碱式碳酸铜是一种化工原料,化学式用mCu(OH)2•nCuCO3表示.实验室以废铜屑为原料制取碱式碳酸铜的步骤如下:查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验次数 | 初读数(mL) | 末读数(mL) |
| 1 | 0.00 | 18.50 |
| 2 | 0.00 | 22.45 |
| 3 | 0.00 | 18.48 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com