
����Ŀ��ij�о���ѧϰС��̽���������Һ���������������ʵ�顣
(1)ȡһ�����ı���������250 mL 0.5000 mol��L-1������Һʱ��Ҫ�õ��IJ�����������Ͳ���ձ�����������___________��___________��
(2)��ѧϰС����pH��ֽ������0.5000 mol��L-1������Һ������pH�ⶨ��������������pH��ֽ��ʹ�÷���______��
(3)������0.5000 mol��L-1�Ĵ�����Һ�ٽ���ϡ�ͣ�Ϊ�ⶨϡ�ͺ������Һ��ȷŨ�ȣ���0.2000 mol��L-1��NaOH��Һ��25.00 mL������Һ���еζ������εζ�����NaOH��Һ��������£�
ʵ����� | 1 | 2 | 3 | 4 |
����NaOH��Һ�����(mL) | 25.05 | 25.00 | 23.80 | 24.95 |
��ô�����Һ��Ũ��Ϊ________________��
(4)ʵ��(2)�У��ζ�������pH�仯������ͼ��ʾ(����������)��

�ٵζ������У����μ�12.50mLNaOHʱ�����û����Һ������Ũ���ɴ�С˳��Ϊ____________��
�ڵ��μ�25.00mLNaOHʱ����Ӧ���û����Һ��pH=9��������Һ�У�ˮ�ĵ�����Ǵ�ˮ��_____����
(5)�ڵζ������У����в�������ɽ��ƫ�ߵ���________��
A.�ζ��յ�ʱ���ζ��ܼ��촦�а������δ��
B.��ȡNaOH��Һ���ʱ����ʼ���Ӷ������ζ��������Ӷ���
C.�ζ�����������ƿ�м�ˮ
D.�ζ���ˮϴ��δ�ñ�Һ��ϴ
���𰸡�250mL����ƿ ��ͷ�ι� ȡһС��pH��ֽ���ڱ��������Ƭ�ϣ���մ�д���Һ�IJ�������ͷ�ιܵ�����ֽ���в����۲���ɫ�ı仯���ɫ���Ա� 0.2000mol/L c(CH3COO-)>c(Na+)>c(H+)>c(OH-) 100 A D
��������
(1)��������һ�����ʵ���Ũ����Һ��ʵ�����������жϣ�
(2)����pH��ֽ��ʹ�÷������н��
(3)����c(��)V(��)=c(��)V(��)���м��㣻
(4)�����кͷ�Ӧc(��)V(��)��c(��)V(��)��ϵ���з����жϣ�
(5)����c(��)= ������������
������������
(1)����250mL0.5000mol/L������Һʱ��Ҫ�õ��IJ��������У���Ͳ���ձ�����������250mL����ƿ�ͽ�ͷ�ιܣ�
(2)pH��ֽ��ʹ�÷����ǣ�ȡһpHС����ֽ�ڱ��������Ƭ�ϣ���մ�д���Һ�IJ�������ͷ�ιܵ�����ֽ���в����۲���ɫ�ı仯���ɫ���Աȣ��ʴ𰸣�ȡһС��pH��ֽ���ڱ��������Ƭ�ϣ���մ�д���Һ�IJ�������ͷ�ιܵ�����ֽ���в����۲���ɫ�ı仯���ɫ���Աȣ�
(3)���ݱ����е����ݵ�3��ʵ���������̫������ȥ���������β�����ȥ����������Һ��ƽ�����Ϊ25.00mL������c(��)V(��)=c(��)V(��)����ô�����Һ��Ũ��c=![]() =0.2000mol/L��
=0.2000mol/L��
(4)���μ�12.50mLNaOHʱ���õ���Ũ�ȵĴ����ƺʹ���Ļ����Һ��pH<7�����ԣ�˵������ĵ���̶ȴ��ڴ�������ӵ�ˮ��̶ȣ���Һ������Ũ���ɴ�С˳��Ϊ��c(CH3COO-)>c(Na+)>c(H+)>c(OH-)��
���μ�25.00mLNaOHʱ����Ӧ��õ���������ҺpH=9����Һ��ˮ�ĵ������������������Ũ��Ϊ��![]() =10-5mol/L�������´�ˮ�ĵ���̶���10-7mol/L��������Һ��ˮ�ĵ���̶��Ǵ�ˮ�ĵ���̶�
=10-5mol/L�������´�ˮ�ĵ���̶���10-7mol/L��������Һ��ˮ�ĵ���̶��Ǵ�ˮ�ĵ���̶�![]() =100����
=100����
(5)A���ζ��յ�ʱ���ζ��ܼ��촦�а������δ���Һ�壬����NaOH��Һ���������ɲ������ƫ�ߣ���A�������⣻
B����ȡNaOH��Һ���ʱ����ʼ���Ӷ������ζ��������Ӷ�����ʹ�ö�ȡNaOH��Һ���ƫС�����´����Ũ�ȼ�С����ɽ��ƫ�ͣ���B���������⣻
C���ζ�����������ƿ�м�ˮ����Ӱ����ͼ�����ʵ��������ԶԲ��������Ӱ�죬��C���������⣻
D���ζ���ˮϴ��δ�ñ�Һ��ϴ����ɱ�ҺŨ�Ƚ��ͣ����ƫ���´����Ũ��������ɲ������ƫ�ߣ���D�������⣻
�ʴ𰸣�AD��


 ���ĺ����Ͼ�������ϵ�д�
���ĺ����Ͼ�������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�ϴ�����![]() ��ZnS��CuS��������
��ZnS��CuS��������![]() ��ijʵ��С���Էϴ���Ϊԭ�ϣ�����п��ͭ�����ʵ���������£���֪��CuS�Ȳ�����ϡ���ᣬҲ����ϡ���ᷴӦ������˵����ȷ����
��ijʵ��С���Էϴ���Ϊԭ�ϣ�����п��ͭ�����ʵ���������£���֪��CuS�Ȳ�����ϡ���ᣬҲ����ϡ���ᷴӦ������˵����ȷ����
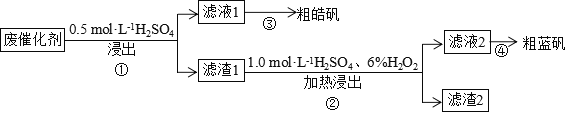
A.��Һ1���Ƿ���![]() ������ѡ��KSCN�����Ƶ���ˮ����
������ѡ��KSCN�����Ƶ���ˮ����
B.����![]() �����У��ȼ�
�����У��ȼ�![]()
![]() ���ڲ��Ͻ����£��ټ���
���ڲ��Ͻ����£��ټ���![]()
![]()
C.����1�ɷ���![]() ��CuS������2�ɷ�һ����
��CuS������2�ɷ�һ����![]()
D.����![]() �����У����ɵ���������NaOH��Һ��
�����У����ɵ���������NaOH��Һ��![]() ��Һ����
��Һ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�ֽ�1mol H2O2�ų�����98kJ���ں�����I- ����Һ�У�H2O2�ֽ�Ļ���Ϊ��H2O2+I-��H2O+IO-���������� H2O2+IO-��H2O+O2+I-���죩�������йظ÷�Ӧ��˵������ȷ���ǣ�������
A.��������ֽ���������ڷ�Ӧ���Ģ�
B.![]() �ķֽ��������
�ķֽ��������![]() Ũ���й�
Ũ���й�
C.�÷�Ӧ�Ĵ�����![]() ��������
��������![]()
D.���ڴ����ļ��뽵���˷�Ӧ�Ļ�ܣ�Ҳ�ı��˸÷�Ӧ�ķ�Ӧ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪ��ⱥ��ʳ��ˮװ�ã������й�˵������ȷ����

A. ���缫�Ϸ���������Ӧ
B. �Ҳ����ɵ�������ʹʪ��ĵ��۵⻯����ֽ����
C. ���һ��ʱ���B���ų�NaOH��Һ
D. ��ⱥ��ʳ��ˮ�����ӷ���ʽ�� 2Cl����2H2O![]() 2OH����H2����Cl2��
2OH����H2����Cl2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�����в�����SO2��NOֱ���ŷŽ��Դ������������Ⱦ�����õ绯ѧԭ������SO2��NO��ͬʱ��� Na2S2O4�� NH4NO3��Ʒ�Ĺ�������ͼ���£�CeΪ��Ԫ�أ���
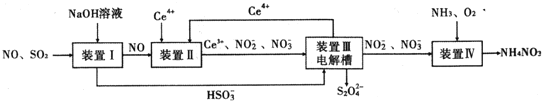
��ش��������⣮
��1��װ������NO����������������NO2-�����ӷ���ʽ______��
��2�����������H2SO3��![]() ��
��![]() ��������SO2��NaOH��Һ��Ӧ�����Һ�У����ǵ����ʵ�������������ҺpH�Ĺ�ϵ��ͼ1��ʾ��
��������SO2��NaOH��Һ��Ӧ�����Һ�У����ǵ����ʵ�������������ҺpH�Ĺ�ϵ��ͼ1��ʾ��
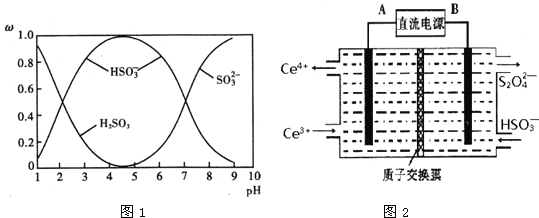
������˵����ȷ����______�����ţ���
A��pH=7ʱ����Һ��c��Na+��=3c��![]() ��
��
B����ͼ�����ݣ����Թ����H2SO3�ĵڶ�������ƽ�ⳣ��Ka2��10-7
C��Ϊ��þ����ܴ��� NaHSO3��Ӧ����Һ��pH������ 4��5Ϊ��
D��pH=9ʱ��Һ��c��OH-��=c��H+��+c��![]() ��+c��H2SO3��
��+c��H2SO3��
����1L1mol/L��NaOH��Һ��ȫ����13.44L������£�SO2����Ӧ�������ӷ���ʽΪ______��
��ȡװ�����е�����ҺVmL����cmol/L�����Ը��������Һ�ζ������Ը��������ҺӦװ��______��������ʽ��������ʽ�����ζ����У��жϵζ��յ�ķ�����______
��3��װ����������֮һ������Ce4+����ԭ����ͼ2��ʾ��ͼ��AΪ��Դ��______�������������������������Ҳ෴Ӧ���з�������Ҫ�缫��ӦʽΪ______��
��4����֪����װ��������Һ��NO2-��Ũ��Ϊ 0.4mol/L��Ҫʹ 1m3����Һ�е�NO2-��ȫת��Ϊ NH4NO3����������װ������ͨ���״���µ� O2�����Ϊ______ L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ϩ����Ҫ�Ļ���ԭ�ϡ���ʵ�����Ʊ��������£�
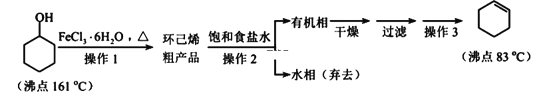
�ش��������⣺
��.����ϩ���Ʊ����ᴿ
(1)ԭ�ϻ������������������ʣ������Լ�Ϊ____________������Ϊ__________________��
(2)����1��װ����ͼ��ʾ(���Ⱥͼг�װ������ȥ)��
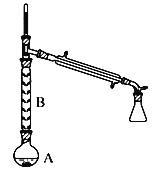
����ƿA�н��еĿ��淴Ӧ��ѧ����ʽΪ___________________��Ũ����Ҳ�����÷�Ӧ�Ĵ�����ѡ��FeCl36H2O������Ũ�����ԭ��Ϊ________________(�����)��
a.Ũ������ʹԭ��̿��������SO2
b. FeCl36H2O��ȾС����ѭ��ʹ�ã�������ɫ��ѧ����
c.ͬ�������£���FeCl36H2O��Ũ�����ƽ��ת���ʸ�
������B������Ϊ____________��
(3)����2�õ��IJ���������____________��
(4)������3(����)�IJ��貹�룺��װ����װ�ã��������������ʺͷ�ʯ��____________����ȥǰ��֣��ռ�83�����֡�
��.����ϩ�����IJⶨ
��һ�������£���ag����ϩ��Ʒ�м��붨���Ƶõ�bmolBr2���뻷��ϩ��ַ�Ӧ��ʣ���Br2������KI��������I2����cmolL-1��Na2S2O3����Һ�ζ����յ�ʱ����Na2S2O3����Һvml (�������ݾ��ѿ۳���������)��
�ⶨ�����У������ķ�Ӧ���£�
��Br2+![]() ��
��![]()
��![]()
��![]()
(5)��Ʒ�л���ϩ����������Ϊ___________(����ĸ��ʾ)��
(6)��������ᵼ�²ⶨ���ƫ�͵���____________(�����)��
a.��Ʒ�к��б�������
b.�ڲⶨ�����в��ֻ���ϩ�ӷ�
c. Na2S2O3����Һ���ֱ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ������˵����ȷ����
A.�����£�1 molŨ����������Al��Ӧ��ת�Ƶ�����Ϊ3NA
B.��״���£�5.6 L Cl2��ȫ�ܽ���ˮ���1 L��Һ����Һ��Cl����Ϊ0.5NA
C.20 gH218O���е�������Ϊ10NA
D.1 L 0.5 mol��L��1 Al2(SO4)3��Һ�����������������Ϊ3NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���Cl2����ͨ��һ������ˮ�������ͣ�Ȼ�������ñ�����ˮ����μ���0.1mol��L-1������������Һ������������pH�仯��ͼ��ʾ�������й�������ȷ����
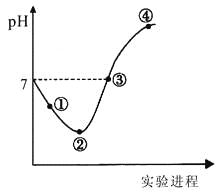
A.������㴦ˮ�ĵ���̶������pH��ֽ�ⶨ��ҺpH
B.����֮ǰ��������Ӧ�����ӷ���ʽΪCl2+H2O=2H++Cl-+ClO-
C.����~��ˮ��ϵ�У�c��H������c��Cl2�� ��c��HClO����c��ClO����
D.������ʾ��Һ�У�c��Na+�� = c��Cl-��+c��ClO-��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л���������ȷ����
A. 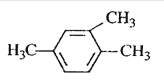 1,3,4-���ױ�
1,3,4-���ױ�
B. 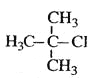 2-��-2-�ȱ���
2-��-2-�ȱ���
C. 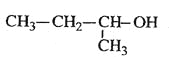 2-��-1-����
2-��-1-����
D. 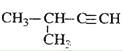 2-��-3-��Ȳ
2-��-3-��Ȳ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com