
【题目】如图为电解饱和食盐水装置,下列有关说法不正确的是

A. 左侧电极上发生氧化反应
B. 右侧生成的气体能使湿润的淀粉碘化钾试纸变蓝
C. 电解一段时间后,B口排出NaOH溶液
D. 电解饱和食盐水的离子方程式: 2Cl-+2H2O![]() 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
科目:高中化学 来源: 题型:
【题目】在0.1 L由NaCl、MgCl2、BaCl2组成的混合溶液中,部分离子浓度大小如图所示,下列对该溶液成分说法不正确的是( )
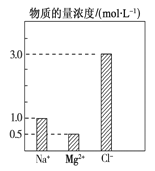
A. NaCl的物质的量为0.1mol
B. 该混合液中BaCl2的物质的量为0.05mol
C. 溶质MgCl2的质量为9.5 g
D. 将该混合液加水稀释至体积为1 L,稀释后溶液中的Na+物质的量的浓度为0.1mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A.《化学与生活》
(1)为减轻大气污染、遏制火灾隐患,今年扬州市区全面禁燃烟花爆竹。据市环境监测中心提供的数据显示,春节禁放期间,AQI(空气质量指数)改善明显,空气质量明显优于去年同期。
①“禁止燃放烟花爆竹”的标识是_____。

②AQI评价的主要污染物为PM2.5、_____、二氧化硫、二氧化氮、臭氧、一氧化碳。
③扬州市2月6日至2月11日空气质量如表,结合表判断扬州空气质量等级达优的有_____天。
AQI | 0~50 | 51~100 | 101~150 | 151~200 |
空气质量等级 | 优 | 良 | 轻微污染 | 轻度污染 |
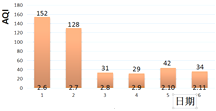
④燃放烟花爆竹时不仅会造成噪音污染,而且会释放出大量的有毒有害气体,如SO2、NO2等,产生空气污染。SO2和NO2可以在一定条件下反应生成NO和另一种氧化物,造成二次空气污染。写出该反应的化学方程式_____。
(2)“蒌蒿满地芦芽短,正是河豚欲上时”是扬州春天真实的写照。
①蒌蒿清香、鲜美,脆嫩爽口,含有丰富的维生素C、维生素A、钙、铁等。其中属于人体所需微量元素的是_____(填元素符号)。
②蒌蒿中含有的维生素A属于_____维生素(填“水溶性”或“脂溶性”)。
③河豚肉质鲜美,蛋白质丰富。蛋白质在人体内水解的最终产物是_____。
(3)2018年10月,世界上最长的跨海大桥—港珠澳大桥正式开通,创造多项世界之最。

①港珠澳大桥采用了世界首创深插式钢圆筒快速成岛技术。深埋在海水中的钢圆筒易发生_____腐蚀,下列保护钢圆筒的措施不合理的是_____(填字母)
a.采用铜质扣件固定保护
b.使用抗腐蚀性强的合金
c.在钢管表面喷镀环氧乙烷树脂镀层
②港珠澳大桥使用了世界最大尺寸高阻尼橡胶隔震支座。为使橡胶性能更好,天然橡胶需要_____处理以增强其机械性能。
③世界首创主动止水的海底沉管隧道使用的超级抗裂钢筋混凝土属于_____(填字母)。
a.金属材料 b.有机高分子材料 c.复合材料
④港珠澳大桥全线夜景照明全部采用LED光源。LED光源与传统光源比较,其优点有_____。(写一种)
⑤港珠澳大桥钢结构混凝土预制件吊装采用超高分子质量聚乙烯(UHMWPE)纤维,是目前世界上强度最高的纤维。请写出由乙烯合成聚乙烯的化学方程式:_____。
B.《有机化学基础》
(1)根据分子中所含官能团可预测有机化合物的性质。
① 测定某有机物的相对分子质量,常用的方法是_____(填字母)。
a.质谱法 b.燃烧法 c.核磁共振氢谱法
② 下列有机物中核磁共振氢谱只有1个峰的是_____(填字母)。
a.甲苯 b.新戊烷 c.乙醚
③ 1mol下列物质完全燃烧时,消耗5mol O2的是_____(填字母)。
a.乙炔 b.丁烷 c.乙酸乙酯
(2)咖啡酸具有止血、镇咳、祛痰等疗效,其结构为:
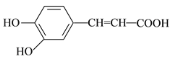
①咖啡酸分子中的含氧官能团的名称为_____、_____。
②有关咖啡酸性质的叙述错误的是_____。
a.在浓硫酸、加热条件下能发生消去反应
b.既能和浓溴水发生加成反应也能发生取代反应
c.能与酸性高锰酸钾溶液反应
d.1 mol 咖啡酸在一定条件下最多能与4 mol 2发生加成反应
(3)四苯基乙烯(TFE)及其衍生物具有诱导发光特性,在光电材料等领域应用前景广泛。以下是TFE的一种合成路线(部分试剂及反应条件省略):
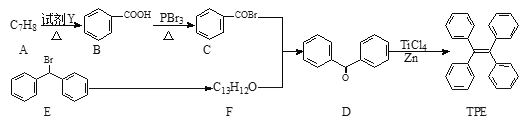
①A的结构简式为_____。
②A![]() B的反应类型为_____反应;E
B的反应类型为_____反应;E![]() F的反应类型为_____反应。
F的反应类型为_____反应。
③生成D的化学方程式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温、恒压下,1 mol A和1 mol B在一个容积可变的容器中发生如下反应:A(g)+2B(g) ![]() 2C(g)。一段时间后达到平衡,生成a mol C。下列说法不正确的是
2C(g)。一段时间后达到平衡,生成a mol C。下列说法不正确的是
A. 起始时刻和达到平衡后容器中的压强比为1:1
B. 物质A、B的转化率之比一定是1:2
C. 若起始放入3 mol A和3 mol B,则达到平衡时生成3a mol C
D. 当v正(A)=v逆(B)时,可断定反应达到平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.实验室里需要氯化钠溶液,但实验室只有混有硫酸钠、碳酸氢铵的氯化钠固体。某学生设计了如下方案进行提纯:

已知:碳酸氢铵受热容易分解,生成二氧化碳、氨气和水。
(1)操作②能否改为加硝酸钡溶液,___(填“能”或“否”),理由___。
(2)进行操作②后,如何判断SO42-已除尽,方法是___。
Ⅱ.硫酸亚铁铵(NH4)2SO4·FeSO4·6H2O为浅绿色晶体,实验室中常以废铁屑为原料来制备,其步骤如下:
步骤1:将废铁屑放入碳酸钠溶液中煮沸除油污,分离出液体,用水洗净铁屑。
步骤2:向处理过的铁屑中加入过量的3mol/L H2SO4溶液,在60℃左右使其反应到不再产生气体,趁热过滤,得FeSO4溶液。
步骤3:向所得FeSO4溶液中加入饱和(NH4)2SO4溶液,经过“一系列操作”后得到硫酸亚铁铵晶体。
请回答下列问题:
(1)在步骤1中,分离操作,所用到的玻璃仪器有___。(填仪器编号)
①漏斗 ②分液漏斗 ③烧杯 ④广口瓶 ⑤铁架台 ⑥玻璃棒
(2)在步骤3中,“一系列操作”依次为__、___和过滤、洗涤、干燥。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列物质:①氢氧化钡固体②KHSO4③HNO3④稀硫酸⑤二氧化碳气体⑥铜⑦碳酸钠粉末⑧蔗糖晶体⑨熔融氯化钠⑩CuSO4·5H2O晶体。
请用序号填空:
(1)上述状态下可导电的是___。
(2)属于电解质的是___。
(3)属于非电解质的是___。
(4)②在水溶液中的电离方程式为___,①与②以物质的量之比为1:2在溶液中反应的离子方程式为___。
(5)③与⑥可以发生如下反应:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,还原产物是___(填名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是利用废铜屑(含杂质铁)制备胆矾(硫酸铜晶体)的流程。
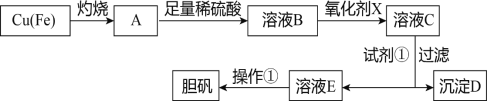
部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
开始沉淀 | 2.7 | 7.5 | 4.4 |
完全沉淀 | 3.7 | 9.7 | 6.7 |
请回答:
(1)溶液B中含有的阳离子有____________________(填离子符号)。
(2)下列物质中最适宜做氧化剂X的是__________(填字母)。
a.NaClO b.H2O2 c.KMnO4
(3)加入试剂①是为了调节pH,要调整pH范围是_____________,则试剂①可以选择______________(填化学式)。
(4)沉淀D加入盐酸和铁粉,可以制得FeCl2溶液,实验室保存FeCl2溶液,需加入过量的铁粉,其原因是____________________________________(用离子方程式表示)。
(5)溶液E经过操作①可得到胆矾,操作①为________________________、过滤、洗涤。
(6)已知溶液中c(Cu2+)与pH的关系为lgc(Cu2+)=8.6-2pH,若溶液中c(Cu2+)为1mol/L,此时溶液中的Fe3+能否沉淀完全:___________(填“能”或“否”) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】本题为选做题,包括A、B两题。选学《化学与生活》模块的考生答A题,选学《有机化学基础》模块的考生答B题,每位考生只可选做1题。若两题都作答,则以A题计分。
A. 《化学与生活》

(1) 营养均衡是保证健康的重要方面。某种食品的配料标签如图所示,根据该食品的配料填空。
①该食品配料中,富含糖类的物质是____。
②该食品配料中,苯甲酸钠的作用是____。
③该食品配料中,碳酸氢钠的作用是____。
(2) 材料是社会经济发展的物质基础。
①钢铁在生活中的应用十分广泛,在潮湿的空气中容易发生____腐蚀。
②普通玻璃的主要成分是Na2SiO3、CaSiO3和 ____(填化学式)。____(填化学式)对玻璃有腐蚀作用,可用于在玻璃仪器上标注刻度及文字。
③聚氯乙烯塑料的结构简式为________,玻璃钢属于________(填“无机非金属材料”“功能高分子材料”或“复合材料”)。
(3)化学与技术的发展是解决环境问题的有效路径。
①减少燃煤产生气体SO2的排放,能够有效控制______(填“硝酸型酸雨”“硫酸型酸雨”或“光化学烟雾”)的形成;向燃煤中加入适量的____(填名称)可减少燃煤烟气中的SO2排放。
②燃煤产生的CO2用氨水吸收可得到氮肥碳铵(NH4HCO3),写出该反应的化学方程式______________。工业上通常采用沉淀法除去废水中的重金属离子,需要控制废水的_____使重金属离子以氢氧化物的形式沉淀出来。
③工业上采用将CO在500 ℃、铝矾催化作用下还原SO2,反应得到两种产物,其中一种产物在常温下是固体。该项技术可大大降低燃煤烟气中SO2的含量,反应的化学方程式为____________________。
B.《有机化学基础》
(1) 有机物的结构决定了其所具有的性质。
①下列有机物不溶于水的是____(填字母)。
a. 乙醛 b. 乙醇 c. 乙酸乙酯
②下列化合物中,不能与新制氢氧化铜悬浊液反应的是____(填字母)。
a. 福尔马林 b. 乙烯 c. 乙酸
③下列试剂中,可用于鉴别苯和甲苯的是____(填字母)。
a. 水 b. 溴水 c. 酸性KMnO4溶液
(2)水杨酸是一种柳树皮提取物,是天然的消炎药,其结构为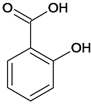 。
。
①水杨酸苯环上的一氯代物有____种。
②水杨酸需密闭保存,其原因是__________。
③水杨酸与足量NaHCO3溶液反应,所得有机产物的结构简式为______。
(3)化合物C是一种医药中间体,由甲苯制备化合物C的路线如下:
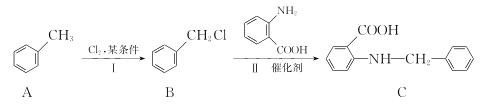
①A→B的反应类型是____。
②B分子中化学环境不同的氢原子有____种。
③D是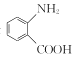 的一种同分异构体,D分子中只有一种官能团,苯环上的一氯代物有2种。则D的结构简式为________。
的一种同分异构体,D分子中只有一种官能团,苯环上的一氯代物有2种。则D的结构简式为________。
④B→C的反应中能生成化合物E,E和C的相对分子质量相同,写出生成化合物E的化学方程式_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(14分) 现有25 ℃时0.1 mol/L的氨水。请回答以下问题:
(1)若向氨水中加入少量硫酸铵固体,此时溶液中 c(OH-) / c(NH3·H2O) ______ (填“增大”“减小”或“不变”);
(2)若向氨水中加入稀硫酸,使其恰好中和,写出反应的离子方程式:
_____________________________________________________________________;
所得溶液的pH________7(填“>”“<”或“=”),用离子方程式表示其原因:
_________________ 。
(3)若向氨水中加入稀硫酸至溶液的pH=7,此时c(NH4+)=a mol/L,则c(SO42-)=________;
(4)若向氨水中加入pH=1的硫酸,且氨水与硫酸的体积比为1∶1,则所得溶液中各离子物质的量浓度由大到小的关系是______________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com