
����Ŀ����Ԫ��Ҳ��̼Ԫ��һ������һϵ���⻯��,��NH3��N2H4��N3H5��N4H6�ȡ���ش������й����⣺
��1����������ϵ���⻯���ͨʽΪ____________��
��2����֪��2H2(g)+O2(g)=2H2O(g) ��H=-483.6kJ��mol-1,�����������ϣ���ѧ���������±���
��ѧ�� | H-H | N=N | N-H |
E/kJ��mol-1 | 436 | 946 | 391 |
�����ֽⷴӦNH3(g)![]()
![]() N2(g)+
N2(g)+ ![]() H2(g)�Ļ��Ea1=300kJ��mol-1����ϳɰ���Ӧ
H2(g)�Ļ��Ea1=300kJ��mol-1����ϳɰ���Ӧ![]()
![]() N2(g)+
N2(g)+ ![]() H2(g)
H2(g)![]() NH3(g)�Ļ��Ea2=___________��
NH3(g)�Ļ��Ea2=___________��
��������ȫȼ�����ɵ�������̬ˮ���Ȼ�ѧ����ʽΪ__________________________��
������ͼ�ǰ���ȼ�ϵ��ʾ��ͼ��a�缫�ĵ缫��ӦʽΪ________________��
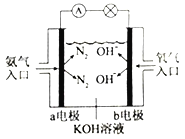
��3����֪NH3��H2OΪһԪ���N2H4��H2OΪ��Ԫ�����ˮ��Һ�е�һ�����뷽��ʽ��ʾΪ��N2H4��H2O+H2O![]() N2H5��H2O++OH-�����������������(N2H6Cl2)��һ��ˮ������ӷ���ʽΪ__________________;��Һ������Ũ���ɴ�С������˳��Ϊ___________________��
N2H5��H2O++OH-�����������������(N2H6Cl2)��һ��ˮ������ӷ���ʽΪ__________________;��Һ������Ũ���ɴ�С������˳��Ϊ___________________��
��4��ͨ�������ж�(NH4)2SO3��Һ�������(д���������)________________________��(��֪����ˮKb=1.8��10-5;H2SO3 Ka1=1.3��10-2Ka2=6.3��10-8)��
���𰸡� NnH(n+2) 254kJ��mol-1 4NH3(g)+3O2(g)=2N2(g)+6H2O(g)��H=-1266.8kJ��mol-1 NH3+6OH--6e-=N2��+6H2O N2H62++H2O![]() N2H5��H2O++H+ [Cl-]>[N2H62+]>[H+]>[N2H5��H2O+]>[OH-] O32-��ˮ�ⳣ��Kh1=
N2H5��H2O++H+ [Cl-]>[N2H62+]>[H+]>[N2H5��H2O+]>[OH-] O32-��ˮ�ⳣ��Kh1=![]() =
=![]() =
=![]() ��10-7��NH4+��ˮ�ⳣ��Kh=
��10-7��NH4+��ˮ�ⳣ��Kh=![]() =
=![]() =
=![]() ��10-10��Kh1>Kh����SO32-ˮ������Ҫ���ö��ʼ���
��10-10��Kh1>Kh����SO32-ˮ������Ҫ���ö��ʼ���
����������1��ͨ���۲��֪��������ԭ�������2����ͨʽΪNnH(n+2)����ȷ�𰸣�NnH(n+2)��
��2����NH3(g)![]()
![]() N2(g)+
N2(g)+ ![]() H2(g)����H=��Ӧ����ܼ���-��������ܼ���=3��391-1/2��946-3/2��436=+46 kJ��mol-1; ��H= Ea1- Ea2=46��300- Ea2=46��Ea2=254kJ��mol-1��
H2(g)����H=��Ӧ����ܼ���-��������ܼ���=3��391-1/2��946-3/2��436=+46 kJ��mol-1; ��H= Ea1- Ea2=46��300- Ea2=46��Ea2=254kJ��mol-1��
�� 2H2(g)+O2(g)=2H2O(g) ��H=-483.6kJ��mol-1, NH3(g)![]()
![]() N2(g)+
N2(g)+ ![]() H2(g)����H==+46 kJ��mol-1;
H2(g)����H==+46 kJ��mol-1;
���ݸ�˹����������ʽ��������ɺ���4NH3(g)+3O2(g)=2N2(g)+6H2O(g) ��H=1266.8kJ��mol-1����ȷ����4NH3(g)+3O2(g)=2N2(g)+6H2O(g) ��H=1266.8kJ��mol-1��
�� ����ȼ�ϵ������������������������������Ӧ��ʧȥ�������ڼ��Ի���������Ϊ����������ӦΪNH3+6OH--6e-=N2��+6H2O����ȷ��Ϊ��NH3+6OH--6e-=N2��+6H2O��
��3��N2H4H2OΪ��Ԫ���N2H6Cl2Ϊǿ�������Σ�ˮ�������ԣ���һ��ˮ������ӷ���ʽΪN2H62++H2O![]() N2H5��H2O++H+����Һ�е�������Cl-��N2H62+��H+��OH-��N2H5��H2O+
N2H5��H2O++H+����Һ�е�������Cl-��N2H62+��H+��OH-��N2H5��H2O+
������ˮ����ɣ���Һ������Ũ�ȴ�С����˳��Ϊ��c(Cl-)>c(N2H62+)>c(H+)>c(N2H5��H2O+)
>c(OH-)����ȷ����c(Cl-)>c(N2H62+)> c(H+)>c(N2H5��H2O+)>c(OH-)��
��4������ˮ��ƽ�ⳣ��Kh=KW/Ka ������KWΪ���ӻ���KaΪ���������ĵ���ƽ�ⳣ����
��֪����ˮKb=1.8��10-5;H2SO3 Ka1=1.3��10-2 Ka2=6.3��10-8)��NH4+��ˮ�ⳣ��Kh1=![]() =
=![]() =
=![]() ��10-10��SO32-��ˮ�ⳣ��Kh2=
��10-10��SO32-��ˮ�ⳣ��Kh2=![]() =
=![]() =
=![]() ��10-7��Kh1<Kh��ƽ�ⳣ��Խ��ˮ��������Խǿ����SO32-ˮ������Ҫ���ö��ʼ��ԣ���ȷ�𰸣����ԣ���֪����ˮKb=1.8��10-5;H2SO3 Ka1=1.3��10-2 Ka2=6.3��10-8)��NH4+��ˮ�ⳣ��Kh1=
��10-7��Kh1<Kh��ƽ�ⳣ��Խ��ˮ��������Խǿ����SO32-ˮ������Ҫ���ö��ʼ��ԣ���ȷ�𰸣����ԣ���֪����ˮKb=1.8��10-5;H2SO3 Ka1=1.3��10-2 Ka2=6.3��10-8)��NH4+��ˮ�ⳣ��Kh1=![]() =
=![]() =
=![]() ��10-10��SO32-��ˮ�ⳣ��Kh2=
��10-10��SO32-��ˮ�ⳣ��Kh2=![]() =
=![]() =
=![]() ��10-7��Kh1<Kh��ƽ�ⳣ��Խ��ˮ��������Խǿ����SO32-ˮ������Ҫ���ö��ʼ��ԣ�
��10-7��Kh1<Kh��ƽ�ⳣ��Խ��ˮ��������Խǿ����SO32-ˮ������Ҫ���ö��ʼ��ԣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ϳɰ������Ĵ����������˹��̵�����Ҫ;�������о�������ȷ������ָ�����ϳɰ���Ӧ��ƽ�ⳣ��Kֵ���¶ȵĹ�ϵ�����
�� �ȣ����� | 360 | 440 | 520 |
Kֵ | 0.036 | 0.010 | 0.0038 |
��1�������ϱ����ݿ�֪�÷�Ӧ����H_____ 0����������������=��������������
�����д�ʩ������������ԭ��������_____������ţ���
a������ѹǿ�����ںϳɰ� b��ʹ�ú��ʵĴ��������ڿ������ɰ�
c����������Ҫ�����¶���500��C���� d����Ҫʹ�ù�����N2�����H2ת����
��2��0.2mol NH3����ˮ�����뺬��0.2mol H2SO4��ϡ��Һ��ȫ��Ӧ����Q kJ���������Ȼ�ѧ����ʽ��ʾ�䷴Ӧʽ��___________________________________��
��3������ʱ����a mol��������ˮ����ͨ��b mol�Ȼ��⣬��Һ���Ϊ1L����c��NH4+��=c��Cl��������һˮ�ϰ��ĵ���ƽ�ⳣ��Kb=_____����ab��ʾ����
��4��ԭ����H2��ͨ����Ӧ CH4��g��+H2O ��g��![]() CO��g��+3H2��g�� ��ȡ����֪�÷�Ӧ�У�����ʼ������е�
CO��g��+3H2��g�� ��ȡ����֪�÷�Ӧ�У�����ʼ������е�![]() �㶨ʱ���¶ȡ�ѹǿ��ƽ������CH4������Ӱ����ͼ��ʾ��
�㶨ʱ���¶ȡ�ѹǿ��ƽ������CH4������Ӱ����ͼ��ʾ��
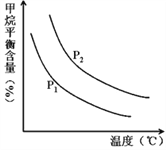
��ͼ�У��������߱�ʾѹǿ�Ĺ�ϵ�ǣ�P1_____P2��������������=��������������
����������һ���������¶ȣ������IJ��ʻ�______������������������С����С�������������䣩��
��5��ԭ����H2����ͨ����ӦCO��g��+H2O��g��![]() CO2��g��+H2��g����ȡ��
CO2��g��+H2��g����ȡ��
��T��ʱ�����ݻ��̶�Ϊ5 L�������г���1mol H2O��g����1mol CO�� ��Ӧ��ƽ����CO��Ũ��0.08 mol/L�����¶��·�Ӧ��ƽ�ⳣ��KֵΪ_____��
�ڱ����¶���ΪT�����ݻ����Ϊ5L���ı�ˮ������CO�ij�ʼ���ʵ���֮�ȣ������������з�Ӧ�����������ܹ�˵����ϵ����ƽ��״̬����_____������ţ���
a��������ѹǿ����ʱ��ı�
b�����������ܶȲ���ʱ��ı�
c����λʱ��������a mol CO2��ͬʱ����a mol H2
d���������n��CO����n��H2O����n��CO2����n��H2��=1��16��6��6
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л���������Щ�������(����)
��CuSO4��5H2O����K2PtCl6����KCl��CuCl2��Cu(NH2CH2COO)2����KCl��MgCl2��6H2O��Cu(CH3COO)2
A. �٢ۢܢ� B. �ڢۢ� C. �٢� D. �٢ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������ȡ��ԭ�����ؽṹ����ͼ��ʾ������������ԣ��翹���������ɻ���������ȣ��ɷ�ֹ������֬�����������ɻ��IJ����������������ȶ��ּ������й�ԭ�����ص�����˵������ȷ����(����)

A. �����ʼȿɿ������࣬Ҳ�ɿ�������
B. 1 mol�����ʿ���4 mol Br2��Ӧ
C. 1 mol�����ʿ���7 mol NaOH��Ӧ
D. 1 mol�����ʿ���7 mol Na��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A.����SO2�ɱ�����������SO3
B.���ȵ���˿��Cl2�о���ȼ�գ���������
C.Ũ������ʹ����̿����ڣ�˵��Ũ���������ˮ��
D.���ڿ�����ȼ�յõ���ɫ����Na2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʽ̼��ͭ������������;�㷺�Ļ���ԭ�ϡ�
��1����ҵ�Ͽ������Կ�ʴ��Һ����Ҫ�ɷ���Cu2+��Fe2+��Fe3+��H+��Cl���Ʊ���ʽ̼��ͭ�����Ʊ��������£�
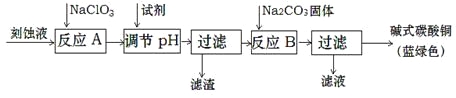
��֪��Cu2+��Fe2+��Fe3+���ɳ�����pH���£�
���� | Cu(OH)2 | Fe (OH)2 | Fe (OH)3 |
��ʼ����pH | 4.2 | 5.8 | 1.2 |
��ȫ����pH | 6.7 | 8.3 | 3.2 |
�������Ƶ������� ��
����ӦA�������Һ��pH��ΧӦΪ ��
����һ�ι��˵õ��IJ�Ʒϴ��ʱ������ж��Ѿ�ϴ���� ��
���������ɫ��Ʒ�л���CuO���ʵ�ԭ���� ��
��2��ijѧϰС����ʵ������������ͼ��ʾװ����ȡ������̽�������ʡ�

��ʵ�����ö������̺�Ũ���������ȡ����������������Ҫ��©���� ��
����C��Ʒ����Һ��ɫ���ܷ�֤��������ˮ��Ӧ�IJ�����Ư���ԣ�˵��ԭ�� ����ʱBװ���з�����Ӧ�����ӷ���ʽ��___________ _____��
��д��A��Һ�о���ǿ���������Ļ�ѧʽ ������A��Һ�м���NaHCO3��ĩ����۲쵽�������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������pAg=-lgc(Ag+),pCl=-lgc(Cl-),���ݲ�ͬ�¶����Ȼ���������Һ��pAg��pCl�ɻ���ͼ����ͼ��ʾ,����֪�Ȼ������ܽ�����¶ȵ����߶�����,���ݸ�ͼ��,���б�����ȷ����

A. A���ʾ����T1�¶��µIJ�������Һ
B. ��A�����Һ����,���ܵõ�C��ı�����Һ
C. ��B������ʾ����Һ�м����Ȼ�����Һ,��Һ���ܸı���D��
D. T3>T2>T1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��EΪ������Ԫ�أ�ԭ��������������������֮��Ϊ40��B��Cͬ���ڣ�A��Dͬ���壬A��C���γ�����Һ̬������A2C��A2C2��E�ǵؿ��к������Ľ���Ԫ�����ʣ�
��1��BԪ�������ڱ��е�λ��Ϊ_________________��
��2��D�ĵ���Ͷ��A2C�еõ�һ����ɫ��Һ��E�ĵ����ڸ���ɫ��Һ�з�Ӧ�����ӷ���ʽΪ_____________________��
��3���õ���ʽ��ʾ��A��C��Ԫ����ɵ��ĺ�18���ӵĹ��ۻ�������γɹ���_____________��
��4���������յ�·����ͭ�ķ���������ʹͭת��Ϊ����ͭ�����������ܽ⡣�ָ���A2C2��ϡ������ݼȴﵽ������Ŀ�ģ��ֱ����˻������÷�Ӧ�Ļ�ѧ����ʽΪ___________________��
��5���Ҵ���C2H5OH��ȼ�ϵ�أ�PtΪ�缫������KOHΪ�������Һ��д�������缫��Ӧʽ__________����ת�Ƶ���1.2molʱ������������������Ϊ______________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com