
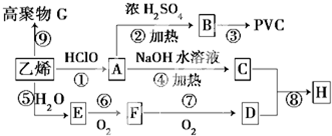
 ,乙烯与水发生加成反应生成E为CH3CH2OH,乙醇在催化剂条件下发生氧化反应生成F为CH3CHO,CH3CHO可进一步氧化得到D为CH3COOH,反应①为乙烯与次氯酸发生加成反应生成A为HOCH2CH2Cl,A发生水解反应生成C为HOCH2CH2OH,(5)中C与D按物质的量之比为1:2反应生成H,则H为CH3COOCH2CH2OOCCH3,A发生消去反应生成B为CH2=CHCl,B在发生加聚反应得到PVC为
,乙烯与水发生加成反应生成E为CH3CH2OH,乙醇在催化剂条件下发生氧化反应生成F为CH3CHO,CH3CHO可进一步氧化得到D为CH3COOH,反应①为乙烯与次氯酸发生加成反应生成A为HOCH2CH2Cl,A发生水解反应生成C为HOCH2CH2OH,(5)中C与D按物质的量之比为1:2反应生成H,则H为CH3COOCH2CH2OOCCH3,A发生消去反应生成B为CH2=CHCl,B在发生加聚反应得到PVC为 ,据此解答.
,据此解答. ,乙烯与水发生加成反应生成E为CH3CH2OH,乙醇在催化剂条件下发生氧化反应生成F为CH3CHO,CH3CHO可进一步氧化得到D为CH3COOH,反应①为乙烯与次氯酸发生加成反应生成A为HOCH2CH2Cl,A发生水解反应生成C为HOCH2CH2OH,(5)中C与D按物质的量之比为1:2反应生成H,则H为CH3COOCH2CH2OOCCH3,A发生消去反应生成B为CH2=CHCl,B在发生加聚反应得到PVC为
,乙烯与水发生加成反应生成E为CH3CH2OH,乙醇在催化剂条件下发生氧化反应生成F为CH3CHO,CH3CHO可进一步氧化得到D为CH3COOH,反应①为乙烯与次氯酸发生加成反应生成A为HOCH2CH2Cl,A发生水解反应生成C为HOCH2CH2OH,(5)中C与D按物质的量之比为1:2反应生成H,则H为CH3COOCH2CH2OOCCH3,A发生消去反应生成B为CH2=CHCl,B在发生加聚反应得到PVC为 ,
, ,故答案为:CH2=CHCl;
,故答案为:CH2=CHCl; ;
;| Cu |
| △ |
| Cu |
| △ |
| 浓硫酸 |
| △ |
| 浓硫酸 |
| △ |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
A、
| ||||
| B、Ba(OH)2?Ba2++2OH- | ||||
| C、HCO3-+H2O?H2O++CO32- | ||||
| D、NaHCO3?Na++H++CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验序号 | 1 | 2 | 3 |
| 消耗NaOH溶液的体积(mL) | 20.05 | 20.00 | 19.95 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、中和滴定实验中的锥形瓶使用前应该用待装液洗涤 |
| B、用25 mL滴定管进行滴定实验时,消耗某溶液体积为21.70 mL |
| C、在托盘天平的托盘上各垫一张洁净的纸片直接称量NaOH固体 |
| D、用广泛pH试纸测得某溶液的pH为2.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
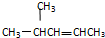
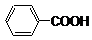
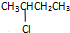
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、可用托盘天平和称量纸称取10.2g NaOH |
| B、某实验需要900ml 0.1mol/L的硫酸铜溶液,则配制该溶液需称取22.5g胆矾晶体 |
| C、用10 mL量筒量取5.2 mL硫酸,仰视时实际量得的液体体积大于5.2 mL |
| D、焰色反应实验中,连续做两个样品时,应将铂丝用硫酸洗净并灼烧到无特殊焰色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com