
����Ŀ��ѧ��Ԫ����������֮��ijͬѧ��̽����̼����Ԫ�طǽ����Ե����ǿ�����������ʵ�飺 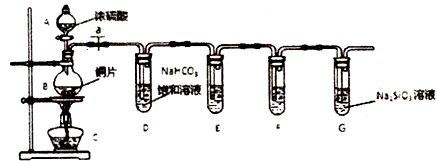
�ش��������⣺
��1����д��ʾ�������ƣ�A��B ��
��2��ʵ�鲽�裺��������������ҩƷ��a��Ȼ�����Ũ���ᣬ���ȣ���ƿ�з�Ӧ�Ļ�ѧ����ʽΪ ��
��3������̽����
���Թ�D�з�����Ӧ�����ӷ���ʽ�� ��
�ڼ�ͬѧ����װ��E����ʢƷ����Һ��ɫ�����Ա仯��F����ʢ����ʯ��ˮ����ǣ��ݴ��϶���Ԫ�صķǽ�����ǿ��̼������ͬѧ��ͬ��Ĺ۵㣬�������� ��
��װ��G�г��ֵ�ʵ������Ϊ �� ����֤��̼Ԫ�صķǽ�����ǿ�ڹ�Ԫ�أ�
���𰸡�
��1����Һ©����Բ����ƿ
��2�����װ�õ������ԣ�Cu+2H2SO4��Ũ�� ![]() CuSO4+SO2��+2H2O
CuSO4+SO2��+2H2O
��3��2HCO3��+SO2=2CO2+SO32��+H2O����������������������Ӧˮ���������ǿ��̼���˵����ķǽ�����ǿ���а�ɫ��������
���������⣺��1������A�Ƿ�Һ©������Һ©���ܿ���Һ�����٣�B��Բ����ƿ��
���Դ��ǣ���Һ©����Բ����ƿ��
��2.�������ӵ�ʵ��װ���ڼ���ҩƷǰҪ���������Լ��飬����ʵ�鲻�ɹ�����ƿ��Cu��Ũ���ᷴӦ��������ͭ�����������ˮ���䷴Ӧ����ʽΪ��Cu+2H2SO4��Ũ�� ![]() CuSO4+SO2��+2H2O�����Դ��ǣ�����װ�������ԣ�Cu+2H2SO4��Ũ��
CuSO4+SO2��+2H2O�����Դ��ǣ�����װ�������ԣ�Cu+2H2SO4��Ũ�� ![]() CuSO4+SO2��+2H2O�� ��3.���ٶ��������̼�����Ʒ�Ӧ�����������ơ�������̼��ˮ���䷴Ӧ�����ӷ���ʽΪ��2HCO3��+SO2=2CO2+SO32��+H2O�����Դ��ǣ�2HCO3��+SO2=2CO2+SO32��+H2O����Ԫ�صķǽ�����Խǿ��������������ˮ��������Խǿ��ǿ���ܺ������η�Ӧ�������ᣬ��������ͨ��Dװ�÷���2HCO3��+SO2=2CO2+SO32��+H2O��˵������������Դ���̼�ᣬ���������������������ˮ������Բ��ܸ�����������̼����������жϷǽ����ԣ����Դ��ǣ���������������������Ӧˮ���������ǿ��̼���˵����ķǽ�����ǿ��������ǿ�����ܺ������η�Ӧ�������ᣬ������̼�����Ʒ�Ӧ���������ԵĹ��ᣬ����G����Һ����ǣ�����˵��̼�����Դ��ڹ��ᣬ��̼Ԫ�صķǽ�����ǿ�ڹ�Ԫ�أ�
CuSO4+SO2��+2H2O�� ��3.���ٶ��������̼�����Ʒ�Ӧ�����������ơ�������̼��ˮ���䷴Ӧ�����ӷ���ʽΪ��2HCO3��+SO2=2CO2+SO32��+H2O�����Դ��ǣ�2HCO3��+SO2=2CO2+SO32��+H2O����Ԫ�صķǽ�����Խǿ��������������ˮ��������Խǿ��ǿ���ܺ������η�Ӧ�������ᣬ��������ͨ��Dװ�÷���2HCO3��+SO2=2CO2+SO32��+H2O��˵������������Դ���̼�ᣬ���������������������ˮ������Բ��ܸ�����������̼����������жϷǽ����ԣ����Դ��ǣ���������������������Ӧˮ���������ǿ��̼���˵����ķǽ�����ǿ��������ǿ�����ܺ������η�Ӧ�������ᣬ������̼�����Ʒ�Ӧ���������ԵĹ��ᣬ����G����Һ����ǣ�����˵��̼�����Դ��ڹ��ᣬ��̼Ԫ�صķǽ�����ǿ�ڹ�Ԫ�أ�
���Դ��ǣ��а�ɫ�������ɣ�
�����㾫����������Ҫ�����˷ǽ�����Ԫ�����ڱ��е�λ�ü������ʵݱ�Ĺ��ɵ����֪ʶ�㣬��Ҫ������Ŀǰ��֪��112��Ԫ���У��ǽ���Ԫ����22�֣���H��ǽ���Ԫ�ض�λ�����ڱ������Ϸ���H�����Ϸ�����F�Ƿǽ�������ǿ��Ԫ�ز�����ȷ�����⣮


 �ǻ�С��ϰϵ�д�
�ǻ�С��ϰϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��E��Ϊ������Ԫ�أ�A�����ԭ��������С��Ԫ�أ�B��+1�������Ӻ�C�ĩ�1�������Ӷ�����ԭ�Ӿ�����ͬ�ĵ��Ӳ�ṹ��D��C����һ���ڣ�����B�γ�BD�����ӻ����E��CΪͬһ����Ԫ�أ�������������Ӧ��ˮ����Ϊһ��ǿ�ᣮ�����������Ϣ�ش��������⣮
��1��BԪ����Ԫ�����ڱ��е�λ���ǵ������壮
��2������DԪ�ص�ԭ�ӽṹʾ��ͼ ��
��3����E���⻯�������������������ȵķ���������һ�����ѧʽ����ͬ���������� ��
��4��A��C�γɵĻ������к��л�ѧ���������� ��
��5��D�ĵ�����B������������Ӧ��ˮ�������Һ������Ӧ�����ӷ���ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����к�̼�Ļ������У�̼Ԫ�صĻ��ϼ���ͬ��һ����
A. CO2��Na2CO3 B. CO��CO2
C. CO��H2CO3 D. CH4��CO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Ԥ����ȷ����
A. ����ˮ���Լ���ױ���CCl4����ȩ������
B. ���к��б��ӣ����Լ���Ũ��ˮȻ����˳�ȥ
C. ���������к���������Լ�������������Һ��ȥ
D. Ϊ���ᴿ�����ʣ���������Һ�м�NaOH��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A.ú��ȼ����Ҫ���ȵ�ȼ���������ȷ�Ӧ
B.����ʯ��ʯ����ʯ���Ƿ��ȷ�Ӧ
C.��C��s��ʯī��=C��s�����ʯ����H=+1.9 kJmol-1��֪�����ʯ��ʯī�ȶ�
D.�������������������ֱ���ȫȼ�գ�ǰ�߷ų���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʾ��ͼ�У����������ԭ�ӣ����������ԭ�ӣ�������������������м���һ���������»����ĸ��壨���������Բ��ƣ��������ܱ�ʾ�������������뺤�����ǣ� ��
A.
B.
C.
D.
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л����������ȷ���� ( )
A. 1,2-�������� B. 2-�һ����� C. 3-������ D. 3,4-��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A. ����������һ���Ƿǽ���������
B. ����������һ���ǽ���������
C. �����ͳ�������Ԫ�صIJ�ͬ����
D. H2 D2 T2 ��Ϊͬλ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ�֪����ҵ���ǵϹ�˾�����˾��ж���ר����﮷���������ε��,��ɱ��ϵ����Ի�������Ⱦ�������ܶ�ԶԶ�����������������ܷ�ӦΪV2O5 + xLi![]() LixV2O5������˵����������( )
LixV2O5������˵����������( )
A. ����ڷŵ�ʱ��Li+���ƶ�
B. ��ڷŵ�ʱ�����������ʱ������
C. �õ�س��ʱ�����ķ�ӦΪLixV2O5 - xe- ��V2O5 + xLi+
D. V2O5ֻ��﮷�����Ӧ�����壬�������ط�Ӧ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com