
����Ŀ��������ȾӰ���������棬������Ⱦ�ǻ�ѧ�������о�����Ҫ���⡣
��1������CO��H2�ϳɼ״�(CH3OH)����֪CO��CH3OH(l)��H2��ȼ���ȷֱ�Ϊ:a kJ��mol-1��b kJ��mol-1��c kJ��mol-1����д���ϳ�CH3OH(l)���Ȼ�ѧ����ʽ��___________________________________��
��2����Ӧ��FeO(s)+CO(g)![]() Fe(s)+CO2(g)���ݻ��̶����ܱ������н��У���ƽ�ⳣ��K���¶�T�Ĺ�ϵ��ͼ��ʾ��
Fe(s)+CO2(g)���ݻ��̶����ܱ������н��У���ƽ�ⳣ��K���¶�T�Ĺ�ϵ��ͼ��ʾ��
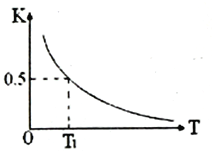
�ٸ÷�Ӧ��________������ȡ����ȡ�����Ӧ��
��һ�������£�������˵���÷�Ӧ�ﵽƽ��״̬����__________
a.���������ܶȲ��ٱ仯 b.������ѹǿ���ٱ仯
c. v(CO2)=v(CO) d. CO�ڻ�����е������������ֲ���
��д���÷�Ӧ��ƽ�ⳣ������ʽ______________________________________��T1�¶��£�����FeO��CO��Ӧ��ƽ��ʱCO��ת����Ϊ ________________________________��
��3���ٰѺ���������Ĺ�ҵ����ͨ�뺬Cr2O72-��Cr3+�����Ե�Ʒ�Һ�У�Cr2O72-����ԭΪCr3+��Cr3+��ˮ�⣩��д���÷�Ӧ�����ӷ���ʽ��_________________________��
�ڷ�Ӧһ��ʱ���ʼ����Cr(OH)3�������ñ�Ҫ�����ӷ���ʽ�����֣���������������ԭ��____________________________________��
���𰸡� CO(g)+2H2(g)=CH3OH(l) ��H=-(a+2c-b)KJ��mol-1 ���� ad K=[CO2]/[CO] 33.3% 3SO2+Cr2O72-+2H+=3SO42-+2Cr3++H2O Cr3+��ˮ��Һ�д���Cr3++3H2O![]() Cr(OH)3+3H+��������Ӧ������H+,ʹ����ƽ�������ƶ�������Cr(OH)3����
Cr(OH)3+3H+��������Ӧ������H+,ʹ����ƽ�������ƶ�������Cr(OH)3����
����������1����֪CO��CH3OH(l)��H2��ȼ���ȷֱ�Ϊ:a kJ��mol-1��b kJ��mol-1��c kJ��mol-1�����У�
��H2(g)��![]() O2(g)=H2O(l) ��H1����c kJ��mol��1
O2(g)=H2O(l) ��H1����c kJ��mol��1
��CO(g)��![]() O2(g)=CO2(g) ��H2����a kJ��mol��1
O2(g)=CO2(g) ��H2����a kJ��mol��1
��CH3OH(l)��![]() O2(g)=CO2(g)��2H2O(l) ��H3����b kJ��mol��1
O2(g)=CO2(g)��2H2O(l) ��H3����b kJ��mol��1
���ݸ�˹�����ɢ١�2+�ڣ��۵ã� CO(g)��2H2(g)= CH3OH(l) ��H��2��H1+��H2-��H3������2c-a+b��kJ��mol��1��(b-2c-a) kJ��mol��1����2���ٸ���ͼ����Ϣ��֪�������¶ȵ����ߣ�Kֵ��С����Ӧ���淴Ӧ�����ƶ����淴ӦΪ���ȷ�Ӧ��������ӦΪ���ȷ�Ӧ���ڷ�ӦFeO(s)+CO(g)![]() Fe(s)+CO2(g) ���ݻ��̶����ܱ������н��У�a.����ӦΪ������������ķ����������ܶȲ��ٱ仯��֤��������������ֲ��䣬�ﵽƽ��״̬��b.�÷�Ӧ�������������ķ�Ӧ��������ѹǿʼ�ղ��䣬ѹǿ����ʱ��һ���ﵽƽ��״̬��c. v(CO2)=v(CO)��û��˵������Ӧ���ʻ����淴Ӧ���ʣ���ȷ������һ����ƽ��״̬��d. CO�ڻ�����е������������ֲ��䣬˵���Ѵ�ƽ��״̬���ʴ�ѡad���۸÷�Ӧ��ƽ�ⳣ������ʽΪK=
Fe(s)+CO2(g) ���ݻ��̶����ܱ������н��У�a.����ӦΪ������������ķ����������ܶȲ��ٱ仯��֤��������������ֲ��䣬�ﵽƽ��״̬��b.�÷�Ӧ�������������ķ�Ӧ��������ѹǿʼ�ղ��䣬ѹǿ����ʱ��һ���ﵽƽ��״̬��c. v(CO2)=v(CO)��û��˵������Ӧ���ʻ����淴Ӧ���ʣ���ȷ������һ����ƽ��״̬��d. CO�ڻ�����е������������ֲ��䣬˵���Ѵ�ƽ��״̬���ʴ�ѡad���۸÷�Ӧ��ƽ�ⳣ������ʽΪK=![]() ��T1�¶��£�����FeO��CO��Ӧ��ƽ��ʱK=0.5����CO��ת����Ϊx����
��T1�¶��£�����FeO��CO��Ӧ��ƽ��ʱK=0.5����CO��ת����Ϊx����
FeO(s)+CO(g)![]() Fe(s)+CO2(g)
Fe(s)+CO2(g)
��ʼʱ��Ũ��/mol/L 1 0
�ı��Ũ��/mol/L x x
ƽ��ʱ��Ũ��/mol/L 1-x x
K=![]() =
=![]() =0.5�����x=33.3%��
=0.5�����x=33.3%��
��3���ٶ���������Cr2O72-��Ӧ��Cr2O72-����ԭΪCr3+��������������Ϊ��������ӣ���Ӧ�����ӷ���ʽΪ��3SO2+Cr2O72-+2H+=3SO42-+2Cr3++H2O���ڷ�Ӧһ��ʱ���ʼ����Cr(OH)3������ԭ��Cr3+��ˮ��Һ�д���Cr3++3H2O![]() Cr(OH)3+3H+��������Ӧ������H+,ʹ����ƽ�������ƶ�������Cr(OH)3������
Cr(OH)3+3H+��������Ӧ������H+,ʹ����ƽ�������ƶ�������Cr(OH)3������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��H2Sȼ�ϵ��Ӧ��ǰ���dz��������õ��ʾ��ͼ���¡�����˵����ȷ���ǣ� ��
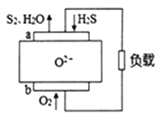
A. �缫a������ B. O2-�ɵ缫a����缫b
C. �缫 a �ķ�ӦʽΪ��2H2S+2O2--4e-=S2+2H2O D. ��ͨ��1.12LO2��ת�Ƶ�����0.2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��Ϊ������Ԫ�أ�A��Bͬ���ڣ�A��C����ͼ������ӷֱ�ΪA2����C����A2�����Ӱ뾶����C����B2����C��������ͬ�ĵ��Ӳ�ṹ������������һ������ȷ���ǣ� ��
A.���ǵ�ԭ������A��B��C B.���ǵ�ԭ�Ӱ뾶C��B��A
C.���ǵ����Ӱ뾶A2����C����B2��D.���ǵ�����������C��A��B
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������Һ�ı���������
A. �ܷ���������ЧӦ B. �ܷ��ȶ�����
C. ��ɢ�����ӵĴ�С��ͬ D. ��ɢ����ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ϊ����ѧ��Ӧԭ��(ѡ��4)��ѡ���⡣
(1)��һ�̶��ݻ����ܱ������н������·�Ӧ��CO2(g)��H2(g)![]() CO(g)��H2O(g)����ƽ�ⳣ��K���¶�T�Ĺ�ϵ���£�
CO(g)��H2O(g)����ƽ�ⳣ��K���¶�T�Ĺ�ϵ���£�
T/�� | 700 | 800 | 850 | 1 000 | 1 200 |
K | 2.6 | 1.7 | 1.0 | 0.9 | 0.6 |
��K�ı���ʽΪ____________________��
�ڸ÷�Ӧ������ӦΪ__________��Ӧ(�����ȡ����ȡ�)��
������ѡ���У����жϸ÷�Ӧ�Ѿ��ﵽ��ѧƽ��״̬����____________(����ĸ����)��
A��������ѹǿ����
B�����������COŨ�Ȳ���
C��v��(H2)��v��(H2O)
D��c(CO2)��c(CO)
(2)���л������HCl����NaOH����CH3COOH����NH3��H2O����CH3COONa����NH4Cl����Һ�ʼ��Ե���__________(�����)��������0.01 mol/L HCl��Һ��pH��________��pH��11��CH3COONa��Һ����ˮ���������c(OH��)��________��
(3)��֪��Cu2����Mg2����Fe2��Ũ����ͬ����Һ�У��俪ʼ����ʱ��pH���£�
���� | Fe2�� | Cu2�� | Mg2�� |
pH | 7.6 | 5.2 | 10.4 |
���������Һ�еμ�NaOH��Һ�����ȳ������� ____________(�����ӷ���)��
���ж�Ksp[Fe(OH)2] ____________Ksp[Mg(OH)2](�����������������)��
(4)���װ����ͼ��ʾ��

�ٵ��ö��Ե缫���ʱ��d�缫�ķ�ӦʽΪ____________________��
�����ô�װ�ý������϶�ͭ����֪�Ʋ�������ô�ͭ�ҵ��ǰ���缫����������ȣ����һ��ʱ���Ե缫���г�����������������Ϊ16 g�����·��ת�Ƶĵ���Ϊ____________mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ⱦ�����Чȥ������Դ�ij�������ǻ�ѧ�츣�������Ҫ���⡣ij�о�С���������̿���Ҫ�ɷ�ΪMnO2��������������������ͭ�����Ƚ���������)���������ͨ�����¼����̼��ѳ�ȼúβ���е�SO2�����Ƶõ�ز��� MnO2����Ӧ������ʡ�ԣ���
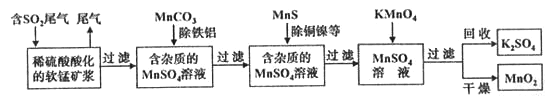
��ش��������⣺
��1��������������ʵ����____________(ѡ��������ĸ���)��
a����������ۺ����� b����ɫ��Ⱦ�ļ��� c������ļ���
��2��KMnO4+MnSO4��MnO2�ķ�Ӧ�У��������뻹ԭ�������ʵ���֮��Ϊ____________��
��3����֪��25�桢101kPa ʱ��Mn(s)+O2(g)=MnO2(s) ��H=-520kJ��mol-1
S(s)+O2(g)=SO2(g) ��H=-297 kJ��mol-1
Mn(s)+S(s)+2O2(g)= MnSO4(s) ��H=-1065 kJ��mol-1
SO2��MnO2��Ӧ������ˮMnSO4���Ȼ�ѧ����ʽΪ��_______________________________��
��4��MnO2�����������������ϡ��ö��Ե缫���MnSO4��Һ���Ƶ�MnO2�������ĵ缫��Ӧʽ��__________________________________________________��
��5��MnO2�Ǽ���п�̵�ص��������ϡ�����п�̵�طŵ�ʱ�������ĵ缫��ӦʽΪ��____________________________________________________�����Ըõ��Ϊ��Դ����ʯī���缫���CuSO4��Һ����������ͭ������������___________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���й���ͳ�Ļ��������������������ݸ�Ŀ���������¼��أ���(��ҩ)������(KNO3)����ơ�ɼľ̿���ϣ���Ϊ����糧���ҩ��������������KNO3���������� ��
A. ��ȼ�� B. �ȶ��� C. ��ԭ�� D. ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com